
- •Загальна хімія
- •Основні закони й поняття хімії
- •Предмет і завдання хімії
- •Місце хімії серед природничих наук
- •Фізичні та хімічні явища
- •Хімічна символіка. Знаки хімічних елементів та хімічні формули
- •Валентність
- •Визначення валентності за формулами хімічних сполук
- •Складання формул сполук з використанням валентності
- •Основні фізичні величини, які використовують у хімії
- •Основні кількісні закони хімії
- •Чисті речовини й суміші
- •Основні методи розділення сумішей
- •Перші спроби класифікації хімічних елементів
- •Періодичний закон Д. І. Менделєєва
- •Періодична система хімічних елементів
- •Будова атома
- •Склад атома
- •Ізотопи
- •Ядерні перетворення
- •Рух електронів в атомі. Орбіталі
- •Будова електронних оболонок та властивості хімічних елементів
- •Хімічний зв’язок і будова речовини
- •Умови виникнення хімічного зв’язку
- •Ковалентний зв’язок
- •Полярний і неполярний ковалентний зв’язок. Властивості хімічного зв’язку
- •Йонний зв’язок
- •Ступінь окиснення
- •Металічний зв’язок
- •Будова твердих речовин та їхні властивості
- •Хімічні реакції та закономірності їх перебігу
- •Класифікація хімічних реакцій
- •Тепловий ефект хімічної реакції. Термохімічні рівняння
- •Швидкість хімічної реакції
- •Каталіз і каталізатори
- •Хімічна рівновага
- •Розчини
- •Поняття про розчини
- •Розчинність. Кристалогідрати
- •Способи кількісного вираження складу розчинів
- •Електроліти та електролітична дисоціація
- •Сильні та слабкі електроліти
- •Йонні рівняння реакцій
- •Окисники й відновники
- •Електроліз розчинів та розплавів електролітів
- •Основні класи неорганічних сполук
- •Оксиди
- •Класифікація оксидів
- •Добування оксидів
- •Хімічні властивості оксидів
- •Кислоти
- •Хімічні властивості кислот
- •Добування кислот
- •Основи
- •Хімічні властивості основ
- •Добування основ
- •Витискувальний ряд металів
- •Генетичний зв’язок між класами неорганічних сполук
- •Хімія елементів
- •Гідроген. Водень. Вода
- •Гідроген
- •Вода
- •Галогени
- •Характеристика хімічних елементів
- •Прості речовини
- •Деякі сполуки галогенів
- •Оксигеновмісні кислоти хлору
- •Хлороводень і хлоридна кислота
- •Оксиген. Сульфур
- •Характеристика хімічних елементів
- •Прості речовини
- •Гідроген пероксид
- •Сірководень
- •Оксиди сульфуру
- •Сульфатна кислота
- •Сульфати
- •Нітроген. Фосфор
- •Характеристика хімічних елементів
- •Прості речовини
- •Хімічні властивості простих речовин
- •Методи добування простих речовин
- •Застосування простих речовин
- •Амоніак
- •Оксиди нітрогену
- •Нітратна кислота
- •Нітрати
- •Кругообіг Нітрогену в природі
- •Оксиди Фосфору
- •Ортофосфатна кислота
- •Мінеральні добрива
- •Карбон. Силіцій
- •Характеристика хімічних елементів
- •Прості речовини
- •Хімічні властивості простих речовин
- •Методи добування простих речовин
- •Застосування вуглецю та кремнію
- •Оксиди карбону та силіцію
- •Карбонати
- •Силікати
- •Кругообіг карбону в природі
- •Загальна характеристика металів
- •Загальні фізичні властивості металів
- •Загальні хімічні властивості металів
- •Загальні способи добування металів
- •Корозія металів
- •Сплави. Доменне виробництво чавуну
- •Деякі представники металів
- •Загальна характеристика лужних металів
- •Натрій і калій
- •Кальцій
- •Алюміній
- •Ферум
- •Органічна хімія
- •Розмаїття і класифікація органічних речовин
- •Виникнення органічної хімії
- •Поняття про органічні речовини
- •Класифікація органічних сполук
- •Загальна характеристика органічних сполук
- •Порівняльна характеристика органічних і неорганічних сполук
- •Хімічна структура та хімічна будова
- •Брутто, структурні та електронні формули сполук
- •Явище ізомерії
- •Ізомери
- •Класифікація органічних сполук
- •Насичені вуглеводні. Алкани
- •Гомологічний ряд алканів
- •Ізомерія алканів
- •Номенклатура вуглеводнів
- •Будова алканів
- •Фізичні властивості алканів
- •Хімічні властивості алканів
- •Методи добування алканів
- •Алкени
- •Гомологічний ряд алкенів
- •Ізомерія алкенів
- •Номенклатура алкенів
- •Будова алкенів
- •Фізичні властивості алкенів
- •Добування алкенів
- •Хімічні властивості алкенів
- •Поняття про полімери
- •Гомологічний ряд алкінів
- •Ізомерія й номенклатура
- •Будова алкінів
- •Фізичні властивості алкінів
- •Добування алкінів
- •Хімічні властивості алкінів
- •Ароматичні вуглеводні (Арени)
- •Поняття про ароматичні сполуки
- •Будова бензену
- •Гомологічний ряд аренів
- •Номенклатура та ізомерія
- •Фізичні властивості аренів
- •Добування аренів
- •Хімічні властивості аренів
- •Правила орієнтації (заміщення) у бензеновому кільці
- •Природні джерела і застосування вуглеводнів
- •Спирти й феноли
- •Гомологічний ряд спиртів
- •Ізомерія та класифікація спиртів
- •Номенклатура спиртів
- •Фізичні властивості спиртів
- •Методи добування спиртів
- •Хімічні властивості спиртів
- •Застосування спиртів
- •Вплив спиртів на організм людини
- •Поняття про феноли
- •Фізичні властивості фенолу
- •Добування фенолів
- •Хімічні властивості фенолів
- •Застосування фенолу
- •Альдегіди
- •Поняття про альдегіди
- •Гомологічний ряд і номенклатура альдегідів
- •Фізичні властивості альдегідів
- •Хімічні властивості альдегідів
- •Добування альдегідів
- •Застосування альдегідів
- •Карбонові кислоти
- •Поняття про карбонові кислоти
- •Класифікація карбонових кислот
- •Гомологічний ряд і номенклатура карбонових кислот
- •Фізичні властивості карбонових кислот
- •Хімічні властивості карбонових кислот
- •Застосування карбонових кислот
- •Естери, жири та мило
- •Поняття про естери
- •Фізичні властивості та застосування естерів
- •Добування естерів та їхня номенклатура
- •Хімічні властивості естерів
- •Жири
- •Хімічні властивості жирів
- •Мило
- •Вуглеводи
- •Поняття про вуглеводи та їхня класифікація
- •Глюкоза
- •Хімічні властивості глюкози
- •Сахароза
- •Крохмаль і целюлоза
- •Штучні волокна
- •Нітрогеновмісні сполуки
- •Амінокислоти й білки
- •Номенклатура та ізомерія амінокислот
- •Фізичні властивості амінокислот
- •Хімічні властивості амінокислот
- •Добування амінокислот
- •Будова білків
- •Хімічні властивості білків
- •Біологічна роль білків
- •Нуклеїнові кислоти
- •Словник термінів

1.Процес зв’язування вуглекислого газу атмосфери живою біомасою рослин у результаті процесу фотосинтезу. Зокрема, завдяки цьому процесу можливе життя на нашій планеті. Під час цього процесу вуглекислий газ переходить у складні органічні сполуки — вуглеводи.
2.Процес споживання рослин у їжу травоїдними тваринами й, зокрема, людиною. При цьо-
му форма вмісту Карбону кардинально не змінюється.
3 та 4. Процеси дихання тварин і рослин, у результаті чого вуглекислий газ виводиться з організму.
5 та 6. Деякі залишки мертвих рослин і тварин за відсутності кисню підлягають мінералізації, процесу, завдяки якому з’явилися поклади нафти, природного газу, вугілля тощо.
7.Цей процес супроводжує процес вивітрювання гірських порід, при якому алюмосилікати металів переходять у відповідні карбонати та гідрокарбонати. У такий спосіб щорічно зв’язуються близько 2 млрд тонн вуглекислого газу.
8.Повільний й на перший погляд несуттєвий процес, пов’язаний з дією природних кислотних опадів на карбонати металів.
На жаль, сучасний кругообіг Карбону посутньо відрізняється від описаного вище. Така відмінність пов’язана з активною діяльністю людини. Спалюючи паливо, вирубуючи ліси, активно видобуваючи корисні копалини, люди порушують ту крихку рівновагу, яка встановлювалася в природі впродовж сотень мільйонів років.
загальна характеристика металів
загальні фізичні властивості металів
Металічні елементи займають в основному ліву нижню частину Періодичної системи хімічних елементів Д. І. Менделєєва. До металічних елементів належать ті елементи, в чиїх атомах на зовнішньому електронному рівні перебуває невелике (від одного до чотирьох) число електронів, які атоми можуть легко віддавати.
Метали мають низку загальних фізичних властивостей:
—добру електропровідність;
—добру теплопровідність;
—металічний блиск;
—добру пластичність (ковкість);
—зазвичай високу твердість;
—найчастіше перебувають у твердому агрегатному стані.
Про приналежність речовини до металів не можна судити тільки за однією ознакою. Так, деякі неметали можуть проводити електричний струм (графіт), мають металічний блиск (йод), мають пластичність (пластична сірка). Таким чином, відносити ту чи іншу просту речовину до металів або неметалів можна тільки за сукупністю ознак.
Загальні фізичні властивості металів (електропровідність, теплопровідність, блиск тощо) пояснюються наявністю рухливих електронів, інакше кажучи, особливим характером металічного зв’язку. Однак різні метали все-таки мають різні фізичні властивості, такі, як температура плавлення, густина тощо. Ці властивості багато в чому залежать від кристалічних структур металів.
Завдяки металічному зв’язку окремі шари
вкристалах металів можуть зміщуватися відносно один одного. Це надає металам пластичності (ковкості) — здатності змінювати свою форму без розриву хімічних зв’язків. Наприклад, найбільш ковким металом є золото — з 1 г золота можна витягнути дріт завдовжки 2,4км і завтовшки
вкількасот разів менший від товщини волосся. Водночас метал сурма дуже крихкий — його навіть можна розтирати на порошок у ступці.
Оскільки різні метали мають подібні металічні зв’язки, а в ряді випадків утворюють подібні металічні кристали, то багато з них при переході
врозплавлений стан можуть змішуватися один з одним, утворюючи сплави. Сплави мають більш різноманітні властивості порівняно з металами, тому в промисловості рідко використовують чисті метали. У більшості випадків для виготовлення деталей різних машин та приладів застосовують сплави. Так, мідь, олово й цинк — це м’які метали, тимчасом як сплав на їхній основі — бронза — дуже твердий, тому бронзу люди здавна використовували для виготовлення зброї, плугів та інших виробів, де потрібна підвищена твердість. Сплав олова зі свинцем (третник) застосовують при паянні, тому що він має порівняно низьку температуру плавлення. Найпоширенішими зі сплавів є чавун і сталь — сплав заліза з вуглецем та іншими неметалами.
загальні хімічні властивості металів
В атомах металів на зовнішній електронній оболонці утримується невелике число електронів. Ці електрони порівняно легко можуть відриватися від атомів. Така особливість металів є причиною не тільки їхніх фізичних, але й хімічних властивостей. Виходячи з того, що метали здатні тільки віддавати електрони зовнішнього електронного
143

рівня, можна зробити висновок, що в хімічних реакціях метали здатні проявляти тільки властивості відновника.
Основний процес, який характеризує хімічні властивості металів, можна записати у вигляді такої схеми:
Me0 −ne → Me+n .
взаємодія металів з неметалами
Більшість металів активно реагують із неметалами, при цьому метали виконують роль відновника, а неметали — окисника. У результаті реакцій утворюються бінарні сполуки: солі безок-
сигенових кислот: |
|
|
|
|
|
|
|||||||
2 |
|
|
|
|
|
2 |
|
|
|
|
|||
ex2 |
e |
||||||||||||
|
|
|
|
|
|
|
+2 −2 |
|
|
|
|
|
+2 −2 |
|
|
|
|
|
|
|
|
|
|
|
|||
2Mg+O2 = 2MgO |
Fe+S= FeS |
||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|||
ex2 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
+3 −2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2Al+3I2 = 2Al I3 . |
|
|
|
|
|
|
|||||||
Або в загальному вигляді: ne
|
|
|
|
|
= Me+nнеMe−n |
|
|
|
|
|
+ неMe0 |
|
|
||||
Me0 |
|
|
||||||
відновник |
окиснювач |
|
сіль безкисневої |
|
|
|||
|
|
|
|
|
|
кислоти |
|
|
взаємодія металів з водою |
|
|
||||||
|
|
|
|
|
|
|||
метали |
|
хімічні процеси при |
|
продукти |
||||
|
|
|
|
реакції з водою |
|
реакції |
||
|
|
|
|
|
|
|||
Лужні мета- |
|
Me0 +HOH → |
Н2 |
і Me(OH)n |
||||
ли, а також |
→ Me+n (OH)n +H2 ↑ |
|
|
|||||
Cа та Ва |
|
|
|
|||||
Mg, Al, Mn, |
|
Me |
0 |
+HOH → |
Н2 |
і МеО |
||
Zn, Cr, |
Fe, |
|
|
|
|
|||
Ni, Pb |
|
→ Me+nO−2 +H2 ↑ |
|
|
||||
Cu, Ag, Au |
З водою не взаємодіють |
|||||||
|
|
|
|
|
|
|
|
|
взаємодія металів з кислотами
Активні метали, які розташовані в ряді напруг до водню, витискують Гідроген із розчинів кислот. Метали, які розташовані в ряді напруг після водню, з розчинами кислот (окрім нітратної та сульфатної) не взаємодіють:
Zn +2HCl = ZnCl2 +H2 ↑,
Zn0 + 2H+ =Zn2+ +H2 ↑,
Cu +HCl ≠ не взаємодіють.
Якщо метал здатний проявляти кілька ступенів окиснення, то при взаємодії з безоксигеновою кислотою утворюється сіль, у якій метал, як правило, має нижчий ступінь окиснення, наприклад:
Fe +2HCl = FeCl2 +H2 ↑,
Fe0 +2H+ = Fe2+ +H2 ↑.
взаємодія металів із солями
Більш активні метали здатні витісняти менш
активні з їхніх солей: |
|
Fe0 +Cu2+ → Fe2+ +Cu0 ; |
Cu0 +Fe2+ ≠ |
Zn0 +Fe2+ →Zn2+ +Fe0 ; |
Fe0 +Zn2+ ≠ |
загальні способи добування металів
лабораторні методи добування
а) відновлення оксидів металів воднем; таким способом зазвичай добувають не дуже активні метали, які не взаємодіють із воднем:
CuO +H2 → Cu +H2O;
WO3 +3H2 → W +3H2O;
б) розкладання оксидів важких металів:
2HgO t→2Hg +O2;
в) витіснення металів з їхніх солей більш активними металами:
Fe +CuSO4 → FeSO4 +Cu;
Zn +HgCl2 →ZnCl2 +Hg.
добування металів у промисловості
а) відновлення оксидів металів вуглецем або кремнієм:
2CuO +C → Cu +CO2 ;
2FeO +Si → Fe +SiO2 ;
б) відновлення оксидів металів карбон монооксидом:
Fe2O3 +CO →2Fe +3CO2 ;
в) відновлення металів з оксидів більш активними металами в розплавах:
3V2O5 +10Al →6V +5Al2O3 ; MnO2 +Mg → Mn +2MgO.
Відновлення металів з оксидів більш активними металами називають металотермічним методом. Найпоширенішим металом, що його використовують як відновник, є алюміній (алюмінотермія).
корозія металів
Корозією зазвичай називають мимовільне руйнування металів у результаті їхньої хімічної й електрохімічної взаємодії із зовнішнім середовищем та перетворення їх у стійкі сполуки (оксиди, гідроксиди, солі).
Власне кажучи, корозія являє собою сукупність окисно-відновних процесів, які відбуваються при контакті металів з агресивним середовищем, що призводить до руйнування металевих виробів. Під агресивним середовищем мають на увазі окисну атмосферу (присутність кисню в атмосфері Землі робить її окисною), особливо в присутності води або розчинів електролітів.
144
За механізмом процесу розрізняють хімічну та
електрохімічну корозію металів. Хімічна корозія
являє собою звичайну хімічну реакцію між атомами металів і різних окисників. Прикладами хімічної корозії є високотемпературне окиснення металів киснем, окиснення поверхні алюмінію на повітрі, взаємодія металів із хлором, сіркою, сірководнем H2S тощо.
Електрохімічна корозія протікає в розчинах, тобто, в основному, при контакті металів з розчинами електролітів, особливо у тих випадках, коли метали перебувають у контакті з менш активними металами. Швидкість корозії істотно залежить від активності металів, а також від концентрації й природи домішок у воді. У чистій воді метали майже не піддаються корозії, а в контакті з більш активними металами навіть у розчинах електролітів не кородують.
причина корозії металів
Багато металів, зокрема й Ферум, перебувають у земній корі у вигляді оксидів. Перехід від металу до оксиду — енергетично вигідний процес, інакше кажучи, оксиди більш стійкі сполуки, ніж метали. Для того щоб провести зворотний процес і добути метал з руди, необхідно затратити багато енергії, тому залізо виявляє тенденцію перетворюватися знову в оксид — як кажуть, залізо іржавіє. Іржавіння — це термін для позначення корозії, тобто процесу окиснення металів під дією навколишнього середовища.
Кругообіг металів у природі можна зобразити за допомогою такої схеми:
добування з руди
(відновлення)
оксид металів |
метал |
(окиснювання) корозія
Металеві вироби іржавіють тому, що сталь, з якої вони зроблені, реагує з киснем та водою, котрі містяться в атмосфері. При корозії заліза або сталі утворюються гідратовані форми
ферум(III) оксиду різного складу (Fe2O3 xH2O) . Оксид проникний для повітря та води й не утворює захисного шару на поверхні металу. Тож корозія металу продовжується й під шаром іржі, що утворилася.
Коли метали контактують із вологим повітрям, вони завжди підлягають корозії, однак на швидкість іржавіння впливає дуже багато факторів. З-поміж них можна назвати такі: наявність домішок у металі; присутність кислот або інших електролітів у розчинах, що стикаються з поверхнею заліза; кисень, який міститься в цих розчинах.
механізм електрохімічної корозії металевої поверхні
У більшості випадків корозія являє собою електрохімічний процес. На поверхні металу утворюються електрохімічні комірки, в яких різні ділянки діють як області окиснення та області відновлення.
Нижче наведені дві напівреакції окисно-від- новного процесу іржавіння:
Fe0 (тверд) −3e →Fe3+ (розчин),
O2 (газ) +2H2O +4e →4OH− (розчин).
Сумарне рівняння реакції корозії заліза можна записати так:
4Fe +3O2 +6H2O →4Fe(OH)3 .
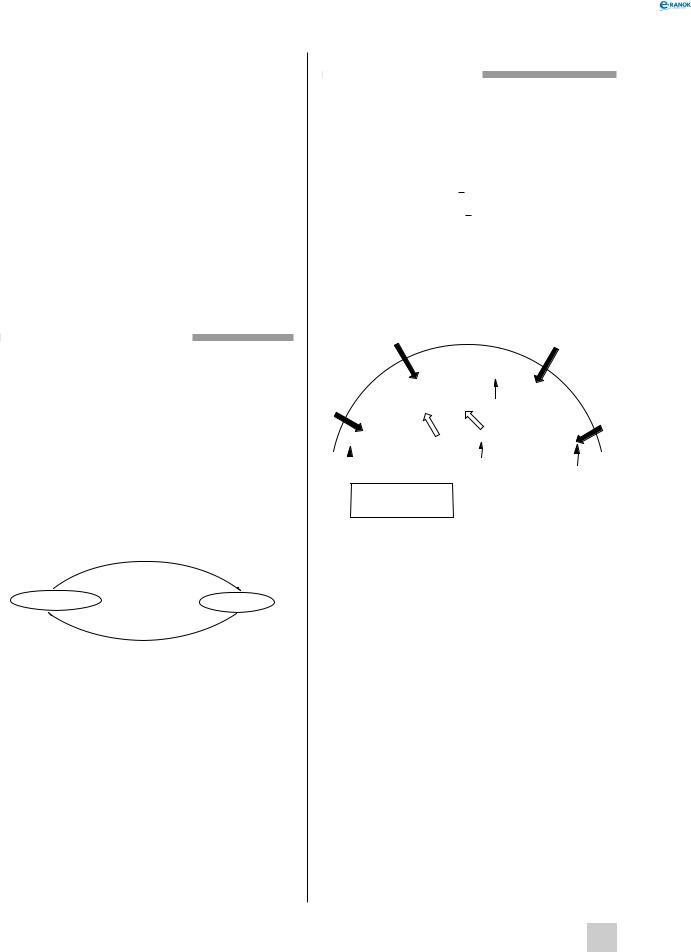
Схематично процеси, які відбуваються на поверхні заліза або сталі при контакті з водою, можна подати так:
|
O2 |
повітря |
|
O2 |
|
|
||||
|
|
крапля води |
|
|
|
|
||||
|
|
Fe2O3 ·xH2O |
іржа |
|
|
|||||
|
|
|
|
|
|
O2 |
|
|
|
|
O2 |
2OH– + Fe2+= Fe(OH) |
2 |
|
O2 |
||||||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
– |
+ H2O = 2OH |
– |
|
Fe2+ |
|
|
|
|
||
2e + 1/2O 2 |
|
|
|
|
|
|
|
|
||
|
|
– |
|
|
|
|
– |
|
|
|
|
|
e |
|
|
Fe |
|
e |
|
|
|
|
потік електронів |
|
|
потік електронів |
|
|
|
|||
|
Відновлення: |
|
|
|
|
|
|
|
||
|
|
|
|
Окиснення: |
|
|
||||
|
кисень відновлюється |
|
залізо окиснюється, |
|
|
|||||
|
до гідроксид йонів |
|
й йони переходять у розчин |
|
|
|||||
|
|
залізо або сталь |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
Концентрація кисню, розчиненого в краплі води, визначає те, які області на поверхні металу є місцем відновлення, а які — місцем окиснення.
По краях краплі, де концентрація розчиненого кисню вища, кисень відновлюється до гідрок- сид-іонів.
Необхідні для відновлення кисню електрони переміщаються із центра краплі, де вони вивільняються при окисненні Феруму й де концентрація розчиненого кисню мала. Йони Феруму переходять у розчин. Вивільнювані електрони по поверхні металу переміщаються до країв краплі.
Сказане вище пояснює, чому корозія найбільшою мірою проявляється в центрі краплі води або під шаром фарби: це області, в які надходження кисню обмежене. Тут утворюються так звані «раковини», в яких Ферум переходить у розчин.
Іржа як така виникає в результаті послідовності вторинних процесів у розчині, куди дифундують із поверхні металу йони Феруму та гідроксид-йони. Захисний шар на поверхні не утворюється.
Активність протікання реакції відновлення Оксигену залежить від кислотності середовища,
145
тому в кислому середовищі корозія прискорюється. Будь-які примісні солі, наприклад, натрій хлорид у бризах морської води, сприяють утворенню іржі, оскільки збільшують електропровідність води.
Можливо, проблему корозії ніколи не вдасться розв’язати повністю, і найбільше, на що можна розраховувати,— це уповільнити її, але не зупинити.
методи захисту від корозії
На сьогодні існує кілька способів запобігання корозії.
Відокремлення металу від агресивного середовища — фарбування, змащування маслами, покриття неактивними металами або емаллю (І). Приведення поверхні металів у контакт із більш активними металами (ІІ). Використання речовин, що сповільнюють корозію (інгібітори корозії), та сплавів, стійких до корозії (ІІІ).
I.Найпростіший спосіб захистити сталь від корозії — це ізолювати метал від атмосферного повітря. Це можна зробити за допомогою масляного, жирового змащування або нанесення захисного шару фарби.
Зараз широко застосовують захисні покриття
зорганічних полімерів. Покриття можна робити різних кольорів, і це досить гнучке розв’язання проблеми корозії. Навіть побіжний погляд на речі, які оточують нас у побуті, дає масу прикладів такого розв’язання: холодильник, сушарка для посуду, піднос, велосипед тощо.
II.Іноді залізо покривають тонким шаром іншого металу. Деякі виробники виготовляють кузови автомобілів зі сталі з гальванічним цин ковим покриттям. При такій обробці утворюється міцно зчеплений з основою шар цинк оксиду, і якщо гальванічне покриття не ушкоджене, воно добре захищає від іржі.
Навіть якщо таке покриття має вади, сталевий корпус машини все ж таки захищений від швидкого руйнування, тому що в цій системі переважно кородує цинк, а не залізо, оскільки цинк більш активний метал, аніж залізо. У да-
ному разі цинк приносять у жертву. Одна з найперших пропозицій щодо використання протекторних («жертовних») металів була зроблена в 1824 році для захисту від корозії металевої обшивки корпусів морських човнів.
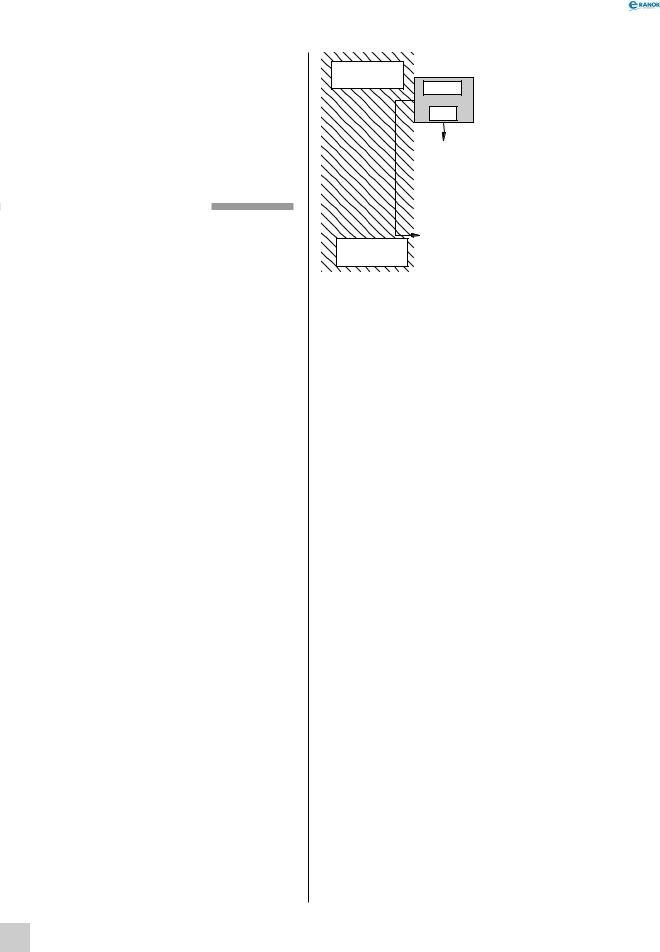
Сьогодні цинкові блоки використовують для захисту від корозії нафтовидобувних платформ у морях: корозія з дорогих складних сталевих конструкцій переводиться на шматки металу, які легко замінити. У чому ж полягає принцип такого захисту? Проілюструємо його за допомогою схеми.
сталева |
морська вода |
|
|
опора |
Цинк |
|
|
Zn |
|
Окиснення: |
|
Zn2+ переважно окиснюється |
– |
Цинк, та йони переходять |
у розчин |
|
e |
|
|
– |
– |
|
потік |
2e |
+ 1/2O2 + H2 O = 2OH |
|
Відновлення: |
|||
електронів |
|||
Оксиген відновлюється |
|||
|
до гідроксид йонів |
||
Через певні проміжки вздовж усієї опори, що перебуває в морі, прикріплені цинкові блоки. Оскільки цинк активніший, аніж залізо (розташований лівіше в електрохімічному ряді напруг), то переважно окиснюється цинк, а залізна поверхня переважно залишається недоторканою. У принципі, будь-який метал, розташований лівіше заліза в електрохімічному ряді напруг, може бути використаний для захисту сталевих виробів.
Аналогічний принцип використовують для захисту залізобетонних конструкцій житлових будинків, в яких усі залізні прути з’єднані один з одним і з’єднуються зі шматком магнію, заритим у землю.
III. Дуже розповсюдженим розв’язанням проблеми захисту від корозії є використання іржостійких сплавів. Багато зі сталевих виробів, використовуваних у побуті, особливо ті, що перебувають у постійному контакті з водою: кухонний посуд, ложки, виделки, ножі, бак пральної машини тощо — виготовлені з іржостійкої сталі, яка не вимагає додаткового захисту.
Іржостійку сталь винайшов у 1913 році хімік із Шеффілда Гаррі Бріарлі. Він досліджував швидке зношування нарізки збройових стволів і вирішив спробувати сталь із високим вмістом хрому, щоб подивитися, чи не можна в такий спосіб продовжити життя зброї.
Зазвичай при проведенні аналізу сталі зразок розчиняли в кислоті. Бріарлі, проводячи такий аналіз, зіштовхнувся з несподіваними труднощами. Його сталь, із високим вмістом хрому, не розчинялася. Він також помітив, що залишені в лабораторії зразки зберігали первісний блиск. Бріарлі відразу ж зметикував, що він винайшов сталь, стійку до корозії.
Винахід Гаррі Бріарлі наштовхнувся на деякі забобони. Один з головних виробників металевого посуду в Шеффілді вважав саму ідею Бріарлі такою, «що суперечить природі», а інший заявив, що «стійкість до корозії — не таке вже й велике
146
