
Гранкiна Т. М., Іщенко Т. В. Хімія за тиждень. Класи неорганічних сполук. Гідроліз. Книга 4
.pdf
Розклад занять
Äåíü 1
Класифікуємо неорганічні сполуки.
Продовжуємо вчитися розв’язувати задачі. . . . . . . . . . . . . . . . . . . . 4
Äåíü 2
Вивчаємо оксиди, їх хімічні властивості й одержання . . . . . . . . 11
Äåíü 3
Вивчаємо кислоти, їх хімічні властивості й одержання . . . . . . . 19
Äåíü 4
Вивчаємо основи, амфотерні гідроксиди, їх хімічні властивості й одержання. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 28
Äåíü 5
Вивчаємо солі, їх хімічні властивості й одержання . . . . . . . . . . . 36
Äåíü 6
Генетичний зв’язок між класами неорганічних сполук.
Гідроліз солей . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 44
3

День 1
Класифікуємо неорганічні сполуки. Продовжуємо вчитися розв’язувати задачі
Перев³рте сво¿ знання |
|
|
хвилин |
||||||||||
1 |
Відповідно до реакції можна одержати: |
|
|
10 |
|
|
|
||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|||||||
1) |
Кислоту |
|
а) CuO + 2HNO3 = Cu(NO3 )2 + H2O |
||||||||||
|
2) |
Оксид |
|
б) SO3 + H2O = H2SO4 |
|||||||||
|
3) |
Соль |
|
в) CaO + H2O = Ca(OH)2 |
|||||||||
|
4) |
Основу |
|
г) 4Na + O2 |
= 2Na2O |
||||||||
2 |
Оберіть правильне твердження. |
|
|
|
|
|
|
|
|
|
|||
а) |
Кислотний оксид — речовина, яку отримують під час згоряння металу. |
||||||||||||
|
б) |
Для одержання кислоти використовують основний оксид і воду. |
|||||||||||
|
в) |
Солі розподіляють на кислі, основні й середні. |
|||||||||||
|
г) |
Луги — нерозчинні основи. |
|
|
|
|
|
|
|
|
|
||
3 |
Оберіть помилкове твердження. |
|
|
|
|
|
|
|
|
|
|||
а) |
У складі одноосновної кислоти міститься один атом Гідрогену. |
||||||||||||
|
б) |
Кислоти — речовини, які складаються з атома Гідрогену й кислот- |
|||||||||||
|
|
|
ного залишку. |
|
|
|
|
|
|
|
|
|
|
|
в) |
У складі основ містяться гідроксигрупи. |
|
|
|
|
|
|
|
||||
|
г) |
Трьохосновні кислоти складаються із трьох атомів різних речовин. |
|||||||||||
4 |
У правому й лівому стовпчиках наведено твердження. Визначте які |
||||||||||||
з них правдиві «+», а які — ні «–». Якщо твердження в правому стовп- |
|||||||||||||
|
чику є логічним продовженням твердження з лівого стовпчика, постав- |
||||||||||||
|
те між ними знак рівності. |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CuSO4 — середня сіль |
|
Середні солі складаються |
|
|
|
||||
|
|
|
|
|
|
з атомів металу й кислотного |
|
|
|
||||
|
|
|
|
|
|
залишку |
|
|
|
|
|
|
|
|
|
|
|
HBr — безоксигенова |
|
Безоксигенові кислоти не |
|
|
|
||||
|
|
|
|
кислота |
|
містять атомів Оксигену |
|
|
|
||||
|
|
|
|
CuO — кислотний оксид |
|
Кислотні оксиди — це оксиди, |
|
|
|
||||
|
|
|
|
|
|
які утворюються в результаті |
|
|
|
||||
|
|
|
|
|
|
реакції води з кислотами |
|
|
|
||||
|
|
|
|
HBr — двохосновна |
|
У складі одноосновних кислот |
|
|
|
||||
|
|
|
|
кислота |
|
міститься один атом Гідрогену |
|
|
|
||||
|
|
|
|
Na2O — основний оксид |
|
Основні оксиди утворюють |
|
|
|
||||
|
|
|
|
|
|
тільки метали |
|
|
|
||||
4
Неорган³чн³ сполуки. Розв’язування задач День 1
|
Це необх³дно знати |
|
хвилин |
|
1 |
Ми вже говорили про те, що речовини бувають прості |
|
60 |
|
|
||||
|
|
|
||
|
|
|
||
|
|
|
||
й складні. Прості речовини можуть бути металами або |
|
|
|
|
|
неметалами. Неорганічні складні речовини для зруч- |
|
|
|
|
ності вивчення підрозділяють на класи. Підґрунтям |
|
|
|
|
класифікації є подібність їхньої будови й хімічних |
|
|
|
|
властивостей. |
|
|
|
2 |
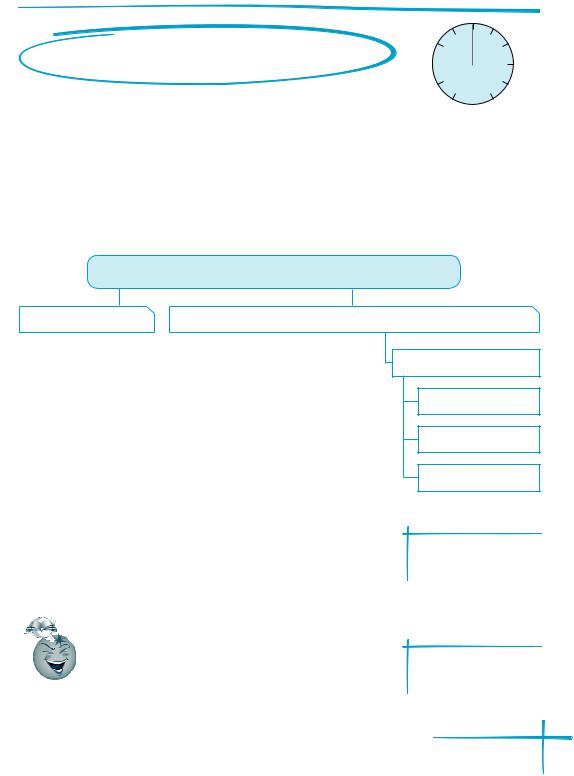
Виділяють такі основні класи неорганічних сполук: |
|
|
|
оксиди, основи, кислоти й солі. |
|
|
|
|
Речовини
|
Прості |
|
|
|
|
|
Складні |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метали |
|
|
Оксиди |
|
|
Солі |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Неметали |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Зараз ми дамо характеристику кожному класу неорганічних сполук, навчимося розрізняти їх з першого погляду за хімічною формулою.
3 Оксиди — це бінарні сполуки, у яких один з елементів — Оксиген (наприклад, CO2 — карбон(IV) оксид). Зверніть увагу, що символ атома Оксигену пишуть на другому місці. Назви й властивості оксидів ми розглянемо детальніше наступного дня (див. День 2).
Оксиди, у свою чергу, класифікують за хімічними властивостями так:
Основні. Утворені металами зі ступенем окиснення +1, +2 (Na2O, CaO, CuO).
Амфотерні. Утворені металами зі ступенем окис-
нення, в основному, +3, +4. Також можливі ступені окиснення +2 і +5 (Al2O3 , ZnO, Fe2O3 , MnO2 ).
Гідроксиди
Кислоти
Основи
Амфотерні основи
Згадаємо, що бінарними називають сполуки, які складаються з атомів двох елементів.
Лужні й лужноземельні метали утворюють основні оксиди.
5

День 1
Кислотні оксиди можуть утворювати деякі метали побічних підгруп і метали IV–VI груп.
Давайте потренуємося впізнавати речовини за форму-
лами: Cu(OH)2 , KOH, Ca(OH)2 — спочатку символ металічного елемента, а потім — гідроксигрупи. Отже, це основи. Так само виглядають і амфотерні гідроксиди: Al(OH)3 , Zn(OH)2 . А тепер формули, на початку яких записано символ Н: HCl, H2SO3 H2SO4 — звичайно, це кислоти. Щоби підкреслити роль гідроксигруп у властивостях основ, їх формули пишуть не так, як формули кислот, наприклад Ca(OH)2
(але не H2CaO2 ).
У назвах основ і амфотерних гідроксидів є слово «гідроксид»: натрій гідроксид. У назвах кислот — кислота.
Неорган³чн³ сполуки. Розв’язування задач
Кислотні. Утворені неметалами SO2 , P2O5 , NO2 або
деякими металами з вищим ступенем окиснення — +5, +6, +7 (Sb2O5 , CrO3 , Mn2O7 ).
Несолетворні. Утворені деякими неметалами з нижчим ступенем окиснення. Це N2O, NO, CO.
4 |
Гідроксиди — це клас неорганічних сполук, у складі |
|||||||||||||
яких міститься група OH− . Якщо із цією групою по- |
||||||||||||||
|
єднані неметалічні елементи, то отримані речовини на- |
|||||||||||||
|
зивають кислотами, якщо метали в нижчих ступенях |
|||||||||||||
|
окиснення +1, +2, то це основи, а якщо в цих сполуках |
|||||||||||||
|
метали проявляють ступені окиснення +3, +4 (можли- |
|||||||||||||
|
ві +2, +5) — це амфотерні гідроксиди. |
|
|
|
|
|
||||||||
|
H |
|
|
O |
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
S |
|
Na |
|
OH |
Al |
|
O |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|||||
|
|
|
|
|
|
|
|
|||||||
|
H |
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
O |
H |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
сульфатна кислота |
натрій гідроксид |
амоній гідроксид |
|||||||||||
|
|
|
|
|
|
(основа) |
(амфотерний гідроксид) |
|||||||
|
|
Як же відрізнити їх формули? Усе |
дуже |
просто. |
||||||||||
|
|
В основ і амфотерних гідроксидів прийнято запису- |
||||||||||||
|
|
вати спочатку символ металічного елемента, а потім |
||||||||||||
|
|
гідроксигрупи, а в кислот — спочатку символ атома |
||||||||||||
|
|
Гідрогену, а потім решту (тобто кислотний зали- |
||||||||||||
|
|
шок). Продовжимо класифікувати гідроксиди. |
||||||||||||
5 |
Основи бувають розчинними й нерозчинними. |
|
|
|||||||||||
|
|
Розчинні основи називають лугами. Вони утворені |
||||||||||||
|
|
лужними (Li, Na, K, Rb, Cs) і лужноземельними (Ca, Sr, |
||||||||||||
|
|
Ba) металами. |
|
|
|
|
|
|
|
|
|
|||
Кислотність основ визначається кількістю в їхній сполуці гідроксигруп.
NaOH — однокислотна основа Cu(OH)2 — двокислотна основа
6 Кислоти класифікують за їх складом, зокрема за вмістом атомів Оксигену.
Таблиця 1
Класифікація кислот за складом
Оксигеновмісні кислоти |
Безоксигенові кислоти |
|
|
|
|
H2SO4 |
— сульфатна |
HF — флуоридна |
HNO3 |
— нітратна |
H2S — сульфідна |
|
|
|
6





