
- •Г.А.Рябов синдромы критических состояний
- •Синдромы критических состояний
- •214000, Г. Смоленск, пр. Им. Ю. Гагарина, 2.
- •Предисловие
- •Введение
- •Глава 1 синдромы расстройств водно-электролитного баланса
- •1.1. Общая вода организма и водные среды
- •1.2. Электролитный состав организма
- •1.3. Осмотическое состояние биологических жидкостей
- •1.4. Механизмы поддержания внутриклеточного объема жидкости и внутриклеточного ионного состава
- •1.5. Механизмы поддержания внеклеточного объема жидкости, и внеклеточного ионного состава
- •1.6. Контроль водно-электролитного баланса
- •1.7. Центральное венозное давление
- •1.8. Клинические варианты водно-электролитного дисбаланса
- •I * ' в клеточное пространство
- •I____ с низкой Мочевина, этанол, свободно
- •1.9. Обмен электролитов и его патология
- •1.10. Клинические аспекты терапии расстройств водно-электролитного баланса
- •Программа лечения больного с. На первые 12 ч
- •Программа лечения больного с. На следующие 12 ч
- •Синдромы расстройств кислотно-основного состояния
- •2.1. Физико-химические факторы кислотно-основного состояния организма
- •2.2. Механизмы поддержания кислотно-основного состояния организма
- •2.3. Показатели кислотно-основного состояния крови и методы их определения
- •2.4. Варианты расстройств кислотно-основного состояния организма
- •Глава 3 нарушения метаболизма в критических состояниях
- •3.1. Изменения обмена в критических состояниях
- •3.2. Эндокринная регуляция метаболизма
- •3.3. Энергетический метаболизм
- •3.4. Клинические аспекты патологии метаболизма
- •3.5. Метаболизм в условиях голодания
- •Глава 4 синдромы острой дыхательной недостаточности
- •4.1. Синдром дыхательных расстройств взрослых
- •4.2. Синдром астматического состояния (астматический статус)
- •4.3. Аспирационный пневмонит (синдром Мендельсона)
- •4.4. Послеоперационная пневмония
- •Глава 5 синдромы шока и полиорганная недостаточность
- •5.1. Общие механизмы основных вариантов шоковых состояний
- •5.2. Элементы патофизиологии шока
- •5.3. Полиорганная недостаточность при шоке
- •5.4. Современная концепция необратимого шока
- •5.5. Клиническая диагностика шока
- •5.6. Принципы лечения шока
- •Глава 6 синдромы расстройств гемостаза [коагулопатии, двс-синдром]
- •6.1. Физиология гемостаза
- •6.2. Общие тесты свертывания крови
- •6.3. Варианты расстройств системы гемостаза
- •6.4. Синдром диссеминированного внутрисосудистого свертывания
- •6.5. Антитромботическая активность, ингибиторы коагуляции
- •6.6. Проблемы гемокоагуляции в связи с гемотрансфузией
- •6.7. Патологический фибринолиз
- •6.8. Антикоагулянтная и тромболитическая терапия
- •Глава 7 коматозные состояния и энцефалопатии. Смерть мозга
- •7.1. Этиологические и патогенетические основы комы
- •7.2. Классификация комы
- •7.3. Общая оценка состояния коматозного больного и элементы клинического обследования
- •7.4. Оценка данных дифференцированного обследования
- •7.5. Клинические варианты комы
- •7.6. Смерть мозга (запредельная кома)
- •7.7. Дифференциальная диагностика смерти мозга
- •Глава 8 острый нефротический синдром (острая почечная недостаточность)
- •8.1. Общие вопросы
- •8.2. Преренальная олигурия
- •8.3. Острый некроз почечных канальцев
- •8.4. Гепаторенальный синдром
- •8.5. Клиническое течение опн и принципы терапии
- •Глава 9 иммунология критических состояний
- •9.1. Иммунная недостаточность и сепсис
- •9.2. Иммунологические нарушения при экстремальных состояниях
- •Глава 10 питание больных в критических состояниях
- •Глава 1. Синдромы расстройств водно-электролитного баланса . . 10
- •Глава 7. Коматозные состояния и энцефалопатии. Смерть мозга . 267
- •Глава 8. Острый нефротический синдром (острая почечная недостаточность) ................305
- •Глава 9. Иммунология критических состояний. Ю. И. Зимин . . 325
- •Глава 10. Питание больных в критических состояниях.....343
1.6. Контроль водно-электролитного баланса
Поступление воды. Человек должен потреблять воды столько, сколько необходимо, чтобы возместить суточную ее потерю через почки и внепочечными путями. Нормальная сбалансированная потребность человека в воде колеблется от 1000 до 2500 мл/сут и зависит от массы тела, возраста, пола и ряда других факторов.
В процессе обмена и утилизации всех трех главных метаболических компонентов — белков, углеводов и жиров — одним из конечных продуктов является вода. Следовательно, организм в состоянии частично покрыть свои потребности за счет использования образующейся в нем эндогенной воды.
При продукции в организме 100 ккал (420 кДж) образуется около 10 мл воды [Moore F., 1963]. Поскольку суточный энергетический выход составляет у взрослого человека 1500— 2000 ккал (6300—9240 кДж), объем образующейся при этом метаболической воды составляет около 150—220 мл, т. е. около 8—10% суточной потребности. Окисление 100 г белков сопровождается образованием 41 мл воды, 100 г жиров —107 мл и 100 г углеводов — 55 мл воды. Очевидно, что метаболическая вода не содержит электролитов. Лихорадка, травма, инфекции и другие тяжелые заболевания приводят к увеличению образования эндогенной воды в 2—3 раза.
Диурез и перспирационные потери. Наиболее тонким и чувствительным показателем баланса жидкости в организме является диурез. Здоровый человек в состоянии выделить в течение суток все продукты обмена в относительно небольшом объеме мочи (400—600 мл). Оптимальный же диурез в 3—4 раза больше и составляет 1400—1600 мл/сут. Помимо этого, при нормальных температурных условиях и нормальной влажности воздуха организм теряет через кожу и путем испарения через дыхательные пути от 800 до 1000 мл воды, образующих так называемые неощутимые потери. Таким образом, общее выведение воды (с мочой и перспирацией) должно составлять 2200— 2600 мл/сут.
В реанимационной практике существуют три варианта определения диуреза: сбор суточной мочи (при неосложненном течении болезни), определение диуреза каждые 8 ч (при инфузионной терапии любого типа) и почасовое определение диуреза (у больных с выраженными расстройствами водно-электролитного баланса, находящихся в шоке и с подозрением на развитие почечной недостаточности при катетеризованном мочевом пузыре). Функция почек в послеоперационном периоде считается удовлетворительной, если в первые 2 сут после операции диурез составляет в среднем 25—35 мл/ч. Это нижняя граница нормы. В последующие дни при благоприятном течении и при условии адекватной инфузионной терапии целесообразно добиваться диуреза, близкого к 80—90 мл/ч, т. е. 1700—2000 мл/сут.
Однако наш опыт показывает, что у больных, которым проводится реанимация, или у больных, находящихся в критическом состоянии, а также в первые дни после обширных операций получить такой диурез практически трудно. Это возможно лишь при значительной водной и солевой нагрузке, которая опасна в критических состояниях, поскольку возможны водная перегрузка легких и нарушение функции почек. Для того чтобы больной в первые 2 сут после обширной операции, когда активно действует фактор антидиуреза, выделил за сутки 2 л мочи, необходимо вводить ему внутривенно жидкости, включая солевые растворы, в количестве 4,5—5 л/сут. По-видимому, в среднем удовлетворительный для тяжелобольного диурез, обеспечивающий полное выведение шлаков, должен составлять 60 мл/ч (1500±500 мл/сут).
Олигурией считается диурез ниже 25—30 мл/ч (меньше 500 мл/сут). В настоящее время различают три типа олигурии (с учетом анатомо-функциональных факторов): преренальную, ренальную и постренальную [Dougan L. R., Flnaly W. E., 1973]. Олигурия первого типа возникает в результате блока почечных сосудов или неадекватного кровообращения. Олигурия второго типа характеризуется паренхиматозной почечной недостаточностью, а третьего — связана с нарушением оттока мочи из почек. С точки зрения реаниматолога, практически наиболее важны два первых. Чтобы оценить значение и качество олигурии, важно знать объем циркулирующей крови (ОЦК), системный объемный кровоток (сердечный выброс), содержание и распределение электролитов в организме и ряд других не менее важных показателей. Плотность мочи, превышающая 1,016—1,018 г/л, свидетельствует о преренальном типе олигурии. Высокая концентрация Na+ в моче (выше 30 ммоль/л) указывает на почечную недостаточность. В этом случае олигурия имеет ренальное происхождение (поражение реабсорбционной функции канальцевого аппарата). О характере олигурии можно также судить по содержанию мочевины в крови и моче. Концентрация мочевины крови, превышающая 25—33 ммоль/л (в норме 2,5— 6,5 ммоль/л), может свидетельствовать о почечной недостаточности. Низкое содержание мочевины в моче (менее 10 г/л) также указывает на почечную недостаточность.
При оценке функции почек у тяжелобольного важно также учитывать отношение осмоляльности мочи к осмоляльности плазмы [Kennedy С., 1968] (табл. 1.3).
Таблица 1.3. Определение типа олигурии по соотношению показателей осмоляльности и содержания мочевины в моче и плазме
Тип олигурии |
Осмоляльность |
Мочевина |
||
|
|
|
||
|
в моче |
в плазме |
в моче |
в плазме |
Преренальная |
2,0 |
1 |
20 |
1 |
Ренальная ранняя |
1,7 |
1 |
14 |
1 |
» поздняя |
1,1 |
1 |
5 |
1 |
Осмоляльность мочи колеблется в широких пределах — от 400 до 1500 мосмоль/кг. После ночного (12-часового) воздержания от мочеиспускания осмоляльность мочи должна быть по крайней мере 850 мосмоль/кг. Нормальная осмоляльность мочи и рН ее, равный 5,8 или более низкий, указывают на нормальную функцию почек. Нррмальное отношение осмоляльности мочи к осмоляльности плазмы 3,4 : 1—4,2 : 1.
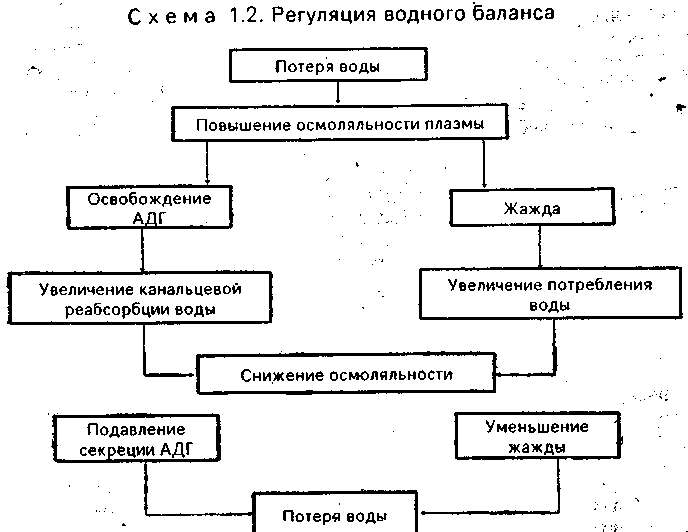
Регуляция водного баланса. Она осуществляется путем активации (угнетения) осморецепторов гипоталамуса, которые реагируют на изменения осмоляльности плазмы и изменения концентрации главного плазменного электролита — Na+. При этом происходят стимуляция или, наоборот, угнетение чувства жажды и соответственно изменения секреции АДГ. Общий механизм регуляции водного баланса представлен на схеме 1.2.
У здорового человека при снижении осмоляльности плазмы до нижней границы нормы (280 мосмоль/кг) полностью подавляется секреция АДГ и выделяющаяся моча имеет очень низкую осмоляльность — до 30 мосмоль/кг. Увеличение осмоляльности плазмы ведет соответственно к повышению уровня АДГ в плазме, и, когда осмоляльность плазмы достигает 295 мос-моль/кг, имеет место максимальный антидиуретический эффект с повышением осмоляльности мочи до 1200 мосмоль/кг [Feig P. U., McCurdy D. K., 1977].
Таким образом, в норме водный баланс регулируется посредством чувства жажды и изменения секреции АДГ в довольно узких пределах изменений осмоляльности плазмы — or 280 до 295 мосмоль/кг.
Однако при патологических состояниях возникают и другие факторы, влияющие на уровень высвобождения АДГ, появление жажды и, следовательно, на баланс воды: потеря ОЦК, боль, травма, рвота, действие лекарственных средств [Goldberg M.,. 1981]. Жажда может стимулироваться при снижении ОЦК и повышении уровня ангиотензина в крови.
В последние годы важное значение в регуляции водного баланса организма придают недавно открытому фактору, так называемому 'атриальному натрийуретическому пептиду ,j Предполагается, что фактор высвобождается из предсердий при их наполнении и стимулирует натрийурез и общий диурез путем повышения скорости клубочковой фильтрации и снижения реабсорбции Na+. Экспериментально показано, что пептид быстро уменьшает объем плазмы и снижает таким образом абсолютный уровень артериального давления. Однако эффекты пептида быстро нивелируются другими регуляторными факторами, например возникшей гипотензией или повышением тонуса симпатической иннервации почек [Trippodo N., 1989]. Начато изучение влияния атриального натрийуретического пептида при гипертонической болезни (первичной гипертензии). Обнаружены его корреляция с возрастом, уровнем артериального давления, наличием или отсутствием гипертрофии левого желудочка и отрицательная корреляция с уровнем ренина в плазме [Wambach G. et al., 1989].
Потери жидкостей и патологические перемещения их в организме. Основными причинами нарушений водно-электролитного баланса являются внешние потери жидкостей и патологические перераспределения их между главными жидкостными средами. Они могут происходить вследствие патологической активации естественных процессов в организме, в частности при полиурии, диарее, чрезмерном потении, а также при обильной рвоте, наконец, в связи с потерями через различные дренажи и фистулы или с поверхности ран и ожогов. Внутренние перемещения жидкостей возможны при развитии отеков в травмированных и инфицированных областях, но главным образом обусловлены изменениями осмоляльности жидкостных сред. Конкретными примерами внутренних перемещений являются накопление жидкости в плевральной и брюшной полостях при плеврите и перитоните, кровопотеря в ткани при обширных переломах, перемещения плазмы в травмированные ткани при синдроме раздавливания и др.
Особым типом внутреннего перемещения жидкости является образование так называемых трансцеллюлярных бассейнов в желудочно-кишечном тракте (при кишечной непроходимости, завороте, инфаркте кишечника, тяжелых послеоперационных парезах).
Образование трансцеллюлярных бассейнов равносильно внешним патологическим потерям жидкостей, ибо происходит секвестрация жидкости с высоким содержанием электролитов. Общий объем суточной секреции на различных уровнях желудочно-кишечного тракта составляет в норме 8—10 л, в том числе слюны 1000—1500 мл, желудочного сока — около 2500 мл, желчи —750—1000 мл, панкреатического сока — свыше 1000 мл, секрета тонкого кишечника — около 3000 мл. В норме все это количество жидкости (за вычетом 100—150 мл, выделяемых с калом) всасывается в тонком кишечнике (табл. 1.4).
Таблица 1.4. Состав главных электролитов в средах желудочно- кишечного тракта и объемы потерь при кишечных свищах и диарее
Секреция |
Объем, мл/сут |
Содержание электролитов, ммоль/л |
||
Na+ |
К+ |
Cl— |
||
В норме: |
||||
слюна |
1000 |
100 |
5 |
75 |
желудочный сок (рН<4,0) |
2500 |
во |
10 |
100 |
» » (рН>4,0) |
2500 |
100 |
10 |
100 |
желчь |
1500 |
140 |
10 |
100 |
панкреатический сок |
1000 |
140 |
10 |
75 |
кишечный сок (смешанный) |
3500 |
100 |
20 |
100 |
При кишечных свищах: |
||||
временной илеостоме |
500— 2000 |
130 |
20 |
110 |
дефинитивной илеостоме |
400 |
50 |
10 |
60 |
временной колостоме |
400 |
80 |
20 |
50 |
При каловом свище |
300 |
50 |
10 |
40 |
При диарее |
1000—4000 |
60 |
30 |
45 |
За исключением желчи и панкреатического сока, содержимое желудочно-кишечного тракта по электролитному составу гипотонично. При тяжелых состояниях, например многократной рвоте любого происхождения, завороте кишечника, кишечной непроходимости на различных уровнях или в результате послеоперационного нарушения моторики кишечника, внутрикишечная секвестрация достигает нескольких литров. Это приводит к тяжелейшим биохимическим нарушениям во всех водных средах — клеточной, интерстициальной и сосудистой, причем теряется значительное количество белков. В каждом литре такой жидкости может содержаться до 30 г белков, главным образом альбумина. В плазме увеличивается содержание глобулиновых фракций при общем снижении количества циркулирующего белка. Значительные внешние потери жидкостей имеют место при обширных ранах и ожогах.
Важным источником внешних потерь жидкости является потение. При этом происходит потеря главным образом водной фракции внеклеточной жидкости без потери белка. Пот является гипотоничной жидкостью. В летнее время его тоничность составляет всего 1/3, а в зимнее приближается к 2/3 тоничности изотонического раствора хлорида натрия. Внешние потери жидкости при обильном потении могут быть значительными, в связи с чем в отдельных случаях требуется срочная коррекция. Обильное питье при потении может снизить относительное содержание в плазме Na+ и С1—. По этой причине внешние потери, возникшие в связи с потением, следует возмещать солевыми растворами, но не глюкозой.
В клинической практике, особенно у хирургических больных, нередко возникают значительные внутренние перемещения; жидкостей, носящие характер патологических перераспределений воды в виде накопления ее в отдельных областях тела, например в области ожога, раны или обширной травмы. В отличие от явных внешних потерь внутренняя секвестрация, как и образование трансцеллюлярных бассейнов, не вызывает существенных изменений массы тела.
Ту область человеческого тела, куда временно перемещается жидкость, принято называть третьим пространством (при этом имеется в виду, что два первых пространства представлены клеточным и внеклеточным водными секторами). Максимум внутренней секвестрации жидкостей наступает через 36—48 ч после травмы или операции. По истечении этого времени процесс начинает медленно регрессировать и жидкость третьего пространства начинает рассасываться.
Содержимое третьего пространства обычно представляет собой смешанную жидкость, в состав которой входят как внутриклеточная и интерстициальная жидкость, так и плазма. Образование третьего пространства обычно сопровождается клинической картиной дефицита жидкости, характеризующейся падением диуреза, снижением ЦВД и сгущением крови в связи с потерей части плазмы.
Наиболее существенные и выраженные перемещения жидкости в организме и ее секвестрация наблюдаются при перитоните. По своему значению и патофизиологической роли секвестрация жидкости при перитоните сходна с нарушениями водного баланса при тяжелых ожогах в острой фазе. В обоих случаях возникают гемоконцентрация, дефицит плазмы, потеря белка и общая дегидратация, в зависимости от характера перитонита секвестрация развивается с различной скоростью, однако в тяжелых случаях процесс может быть почти молниеносным. При адекватном лечении антибиотиками или после успешного оперативного вмешательства происходит достаточно быстрое (в пределах 1—2 нед) обратное развитие процесса, заканчивающееся почти полным всасыванием жидкости и даже белков из брюшной полости.
Значительные секвестрации жидкости в третье пространство могут также происходить при распространенном тромбозе вен, особенно бедренных и подвздошных.
Секвестрированные жидкости возвращаются в интерстициальное пространство и в плазму по мере того, как ликвидируется причина, вызвавшая секвестрацию. С ликвидацией третьего пространства и рассасыванием секвестрированной жидкости в циркулирующую плазму и интерстициальное пространство вместе с водой поступают дополнительные количества электролитов. Это обстоятельство необходимо учитывать при лечении. При почечной недостаточности процесс естественной ликвидации третьего пространства может принимать опасный характер в связи с возможностью патологической задержки электролитов в крови.
Подобный же процесс обратного всасывания и ликвидации третьего пространства происходит при ликвидации кишечной непроходимости и восстановлении моторной функции кишечника.
В лечебной тактике, особенно при определении объемов замещения потерь воды и электролитов у подобных больных, описанные тенденции должны быть учтены. В восстановительном периоде не следует стремиться к полному возмещению повышенной экскреции электролитов, так как она может быть отражением повышенного поступления электролитов в циркулирующую плазму и интерстициальное пространство из третьего пространства. У некоторых больных в этом периоде выявляется снижение массы тела в сочетании с усилением диуреза без признаков дегидратации. Гематокрит, содержание белков, а также Na+ и С1— в крови быстро нормализуются. Обычно в этом периоде отпадает необходимость в продолжении инфузионной терапии.
Клинические проявления нарушений водно-электролитного баланса. Наиболее часто нарушения возникают при острых заболеваниях органов брюшной полости, вмешательствах на желудочно-кишечном тракте, ожогах, тяжелых хронических заболеваниях с наличием свищей, а также при выраженных внешних потерях жидкостей.
В оценке степени дисгидрии большое значение имеет анамнез. Указания на частую рвоту, предшествовавшую периоду врачебного наблюдения, или диарею заставляют предположить, что имеется существенный водно-электролитный дисбаланс, даже если при первоначальном осмотре признаки его еще не выявляются.
При остро развившемся перитоните или кишечной непроходимости водно-электролитный дисбаланс наряду с интоксикацией является первым звеном в патогенетической цепи заболевания. Отсутствие видимых потерь у таких больных еще не означает благополучия: признаки дегидратации проявляются внезапно и прогрессируют молниеносно. Потерянная вода и электролиты концентрируются в полости кишечника и в меньшей степени в брюшной полости. Определение водного баланса и динамики этого показателя с помощью весов-кровати нередко дает ошибочные результаты, поскольку в таких случаях вода не покидает организм. Использование весов-кровати целесообразно в тех случаях, когда есть полная уверенность в отсутствии секвестрации жидкости в естественные полости организма. В запущенных случаях острой кишечной непроходимости, особенно при нарушении брыжеечного кровообращения, полость кишечника может аккумулировать до 5—7 л жидкости с высоким содержанием электролитов.
Жажда — один из главных и наиболее характерных симптомов дефицита воды. Жажда должна быть четко дифференцирована от сухости слизистой оболочки рта, которая может быть устранена полосканием рта и глотки; жажда этим приемом не устраняется. (Наличие жажды показывает, что объем воды во внеклеточном пространстве уменьшен относительно содержания солей в нем. Следовательно, если больной с истинной жаждой имеет доступ к воде, то он в состоянии быстро устранить дефицит ее. Потеря чистой воды и возникновение в связи с этим жажды возможны также при обильном потении (высокая лихорадка), диарее и осмотическом диурезе (высокий уровень глюкозы при диабетической коме, применение маннитола или мочевины).
Сухость в подмышечных и паховых областях является важным симптомом потери воды и свидетельствует о том, что дефицит воды в организме составляет минимум 1500 мл.
Снижение тургора тканей и кожи необходимо рассматривать как показатель уменьшения объема интерстициальной жидкости. У пожилых людей и в норме кожа нередко бывает сухой и малоэластичной. У тучных даже при выраженной дегидратации кожа может сохранять эластичность.
Внешний вид языка в значительной степени отражает состояние дисгидрии. В нормальных условиях язык имеет единственную более или менее выраженную срединную продольную борозду. При дегидратации появляются дополнительные борозды, параллельные срединной.
Тонус глазных яблок — ценный симптом, свидетельствующий не только о дегидратации (снижение тонуса), но и о гипергидратации организма, особенно мозга (напряжение глазного яблока).
Изменения массы тела на протяжении короткого времени (например, через час) являются показателем изменений объема внеклеточной жидкости. Однако к результатам взвешивания надо относиться с большой осторожностью и оценивать их только в сочетании с другими показателями. Образование третьего пространства, например, может не отразиться на изменениях массы тела, между тем при наличии большого третьего пространства организм находится в состоянии относительной дегидратации. Другая трудность в оценке изменений массы тела заключается в том, что при критическом состоянии больного необходимо учитывать характер обмена в момент взвешивания: катаболическая фаза обычно сопряжена с потерей тканей (до 500 г/сут), анаболическая фаза характеризуется увеличением тканевых масс (около 150 г/сут). Для послеоперационных больных характерно уменьшение тканевых масс приблизительно на 300 г/сут. В большинстве случаев увеличение массы тела следует рассматривать как задержку воды. Потеря массы тела, превышающая 500 г/сут, свидетельствует о потере воды. Лечение никогда не должно основываться только на учете изменений массы тела. Необходимо принимать во внимание всю клиническую картину.
Изменения артериального давления и пульса отражают существенные потери воды организмом, однако в большей степени они связаны с уменьшением ОЦК. Тахикардия — довольно ранний признак снижения ОЦК. У больных с дефицитом объема крови тахикардия обычно коррелирует с постуральными реакциями артериального давления. Первые признаки снижения артериального давления могут наблюдаться лишь при существенном дефиците ОЦК, превышающем по крайней мере 1 л при гипотензии в положении сидя и 1,5 л при развитии гипотензии в горизонтальном положении.
Состояние наполнения наружной яремной вены. У здорового человека в горизонтальном положении наружная яремная вена на уровне переднего края грудиноключично-сосцевидной мышцы наполнена кровью и хорошо контурируется под кожей. Наполнение этой вены довольно точно отражает величину ЦВД. Повышенное ЦВД наблюдается при увеличении объема плазмы или крови или при сердечной недостаточности. При уменьшении объема плазмы ЦВД снижается. Спадение шейных вен в горизонтальном положении свидетельствует о том, что у больного уменьшен объем плазмы, и указывает на необходимость введения солевых растворов. Для того чтобы дифференцировать сердечную недостаточность от увеличений объема плазмы, одинаково проявляющихся вздутием шейных вен, пользуются тестом на печеночно-яремный рёфлюкс. Больному в сидячем или в полусидячем положении надавливают на живот в области расположения печени, стремясь вызвать ее сдавление. При сердечной недостаточности этот тест вызывает увеличение вздутия шейных вен, при увеличенном объеме плазмы (в отсутствие сердечной недостаточности) печеночно-яремный рефлюкс отсутствует и вздутие вен уменьшается.
Отеки всегда отражают увеличение объема интерстициальной жидкости и могут указывать на то, что общее количество Na+ в организме повышено. Однако отеки не являются высокочувствительным показателем баланса Na+: в организме общее количество обменного Na+ может повыситься на 20—25% без появления отеков. Это связано с тем, что перераспределение воды между сосудистым и интерстициальным пространством обусловлено высоким белковым градиентом между этими двумя средами. При нормальном белковом балансе появление едва заметной ямки при надавливании пальцем в области передней поверхности большеберцовой кости свидетельствует о том, что в организме имеется избыток по крайней мере 400 ммоль Na+, что составляет более 2,5 л солевого раствора.
Появление влажных хрипов в легких указывает на накопление воды в альвеолах и в отсутствие признаков сердечной недостаточности может свидетельствовать о наличии лишней воды в организме.
Исследование ОЦК дает важную информацию о степени гидратации интерстициального и главным образом внутрисосудистого пространства.
Примерная зависимость между дефицитом воды и клиническими проявлениями дегидратации представлена в табл. 1.5.
Таблица 1.5. Клинические признаки дегидратации в зависимости от дефицита воды
Дефицит воды, л |
Симптом |
Менее 1,5 |
Жажда, гемодинамика нормальная |
1,5—4 |
Выраженная жажда, сухость языка, полости рта, подмышечных впадин и паховых областей, повышение содержания Na+ в плазме и относительной плотности мочи, тенденция к гипотензии или нормотензии. |
Свыше 4 л |
Мучительная жажда, выраженная гипернатриемия, олигурия, снижение массы тела, умеренное повышение гематокрита, гипотензия, тахикардия, апатия, ступор. Если состояние вовремя не корригируется, то наступают гиперосмоляльная кома и смерть. |
Главными признаками дефицита воды в организме являются жажда, олигурия и гипернатриемия.
В оценке водно-электролитного баланса у больного, находящегося в критическом состоянии, неоценимую роль играет тщательный учет количества жидкости, поступающей в организм и теряемой различными путями. Исследования водного баланса должны быть начаты немедленно после поступления больного в отделение реанимации. Практически оптимальной временной границей определения жидкостного баланса считают 8 ч утра, когда происходит смена лечащего персонала. Использование весов-кровати, несмотря на определенные оговорки, предусматривающие осторожность в трактовке изменений массы тела, оказывает существенную помощь в оценке жидкостного баланса организма.
Все физиологические и патологические потери жидкостей организмом необходимо строго учитывать и посылать в лабораторию для анализа содержания в них электролитов и других компонентов. Такими фрагментами жидкостных потерь могут быть моча, жидкий кал, рвотные массы, кишечное содержимое, полученное при лаваже кишечника во время операции, отделяемое через дренажи и др.
В клинической практике даже при самом точном и скрупулезном учете потерь жидкостей при оценке жидкостного баланса организма могут возникать ошибки, что обусловлено прежде всего невозможностью точного учета неощутимых потерь через дыхательные пути и кожу. У лихорадящих больных такие ошибки весьма существенны. Практика показывает, что попытки соотнести количество водных потерь с температурой тела обычно бесплодны. Никогда нельзя даже приблизительно сказать, каким оказался прирост потерь воды при повышении температуры тела на каждый градус, так как гипертермия и лихорадка в разные периоды, как известно, могут сопровождаться обильным потением, но могут протекать и без него. Тем не менее необходимо указать, что при всякой лихорадке организм теряет воды всегда больше, чем в нормальном состоянии, и эти потери могут колебаться (табл. 1.6). Потери воды организмом зависят от температуры окружающей среды и частоты дыхания.
Таблица 1.6. Дополнительные потери воды в зависимости от температуры тела, температуры окружающей среды и частоты дыхания [Condon R. Е., 1975]
Объем дополнительных потерь воды, мл/сут |
Температура тела, °С |
Температура окружающей среды, °С |
Частота дыхания, мин—1 |
0 |
<38,3 |
<29,5 |
<35 |
500 |
38,4—39,4 |
29,5—35 |
>35 |
1000 |
>39,5 |
>35 |
— |
В обычной клинической практике врачу приходится иметь дело как с состояниями, характеризующимися избытком воды, так и с состояниями, обусловленными ее дефицитом.
Понятие «потеря жидкости» в клинической практике может истолковываться весьма широко. Так могут обозначаться различные состояния, начиная от ограниченной внеклеточной и вполне компенсированной дегидратации при нетяжелых заболеваниях до потери огромных объемов жидкостей, равных объему плазмы или даже общему объему крови и измеряемых иногда десятками литров. Такие огромные потери возникают, например, при странгуляционной кишечной непроходимости или инфаркте кишечника, тяжелом перитоните или панкреонекрозе. Обычно эти заболевания, сопровождающиеся выраженной дегидратацией, имеют крайне тяжелое, иногда злокачественное течение и трудно поддаются лечению. Помимо воздействия самого интоксикационного фактора, развиваются глубокие нарушения практически всех видов обменных функций.
