
- •1.Абсолютная и относительная погрешности.
- •2 Классификация погрешностей по форме представления:
- •3 Способы выявления систематической погрешности
- •Выполнение анализа независимыми методами.
- •Проведение холостого опыта или анализа.
- •Метод стандартных образцов
- •4 Случайные погрешности
- •5. Генеральная и выборочная совокупность
- •6. Среднее арифметическое выборочной совокупности. Случайное отклонение.
- •7. Выборочное стандартное отклонение. Дисперсия
- •8. Среднеквадратичное отклонение
- •9. Нормальное распределение
- •10. Распределение Стьюдента
- •11. Требование к пробе анализа. Генеральная, средняя, лабораторная и анализируемая проба
- •12. Отбор проб газов, жидкостей и твердых веществ.
- •13.Отбор проб продуктов питания и продовольственного сырья.
- •14. Принципы подготовки проб к анализу.
- •15. Метод разложения проб
- •16. Растворение проб.
- •17. Сплавление пробы.
- •18. Пиролиз пробы.
- •19. Методы разделения и концентрирования проб.
- •20. Сущность титриметрии
- •21. Стандартизация растворов титрантов.
- •22. Точка эквивалентности
- •23. Точка конца титрования
- •24. Кривые титрования
- •25. Способы титрования
- •26. Индикаторы и правила выбора индикатора
- •27. Гальванический элемент
- •28. Общие принципы электрохимических методов анализа. Классификация электродов и электродных систем.
- •29. Метод прямой кондуктометрии
- •30. Безэлектродная кондуктометрия
- •32. Сущность потенциометрического анализа. Окислительно-восстановительный потенциал и его зависимость от концентрации и температуры.
- •33. Методы прямой потенциометрии
- •34. Электроды сравнения и индикаторный электрод
- •35. Ионоселективные электроды
- •1. Первичные:
- •2. Сложные и многомембранные
- •36. Методы потенциометрического титрования
- •38. Сущность кулонометрического анализа.
- •39. Прямая кулонометрия
- •40. Кулонометрия при постоянной силе тока
- •41. Теоретические основы вольтамперометрии
- •43. Методы полярографии
- •44. Метод дифференциальной полярографии
- •45. Инверсионная вольтамперометрия
- •49. Принципиальная схема хроматографа
- •52. Радиоактивность. Методы регистрации радиоактивности
- •42. Схема установки полярографического анализа
- •42. Схема установки полярографического анализа
- •1.Абсолютная и относительная погрешности.
- •2 Классификация погрешностей по форме представления:
35. Ионоселективные электроды
Ионоселективные электроды представляет собой устройство, основным элементом которого является мембрана, проницаемая только для определенного иона. Ионселективные электроды имеют следующие достоинства: они не оказывают воздействия на исследуемый раствор, портативны, пригодны как для прямых определений, так и в качестве индикаторов в титриметрии.Ион-е, электрохим. электроды, равновесный потенциал к-рых в р-ре электролита, содержащем определенные ионы, обратимо и избирательно зависит от концентрации этих ионов. На этом основании ион-ые электроды используют для определения концентрации (активности) разл. ионов в р-ре, а также для анализа и контроля процессов, протекание к-рых сопровождается изменением ионного состава р-ров. Разработка и применение ион-ых электродов для определения разл. ионов - осн. задача потенциометрии. В большинстве случаев ион-ый электрод представляет собой устройство, осн. элементом к-рого является мембрана, проницаемая только для определенного иона. Между р-рами электролитов, разделенных мембраной, устанавливается стабильная разность потенциалов, к-рая алгебраически складывается из двух межфазных скачков потенциала и диффузионного потенциала, возникающего внутри мембраны.
Типы:
1. Первичные:
- электроды со стеклянной мембраной
- кристаллические мембранные электроды – мембраны состоят из ионных кристаллов или их смесей. Иногда представляют собой монокристаллы.
- электроды с жидкой мембраной – основу мембраны составляют несмешивающиеся с водой жидкости. Внутренний р-р сравнения отделён от анализируемого р-ра тонким слоем жидкости содержащий жидкий ион, не смешивающийся с водой, но селективно реагирующий с определённым ионом: жидкие иономембранные электроды и электроды с жидкой мембраной с нейтральным носителем
2. Сложные и многомембранные
- молекулярно-чувствительные устройства, такие как газочувствительные или ферментные электроды, в которых потенциометрический детектирующий блок основан на стандартных потенциометрический электродах ранее перечисленных типов.
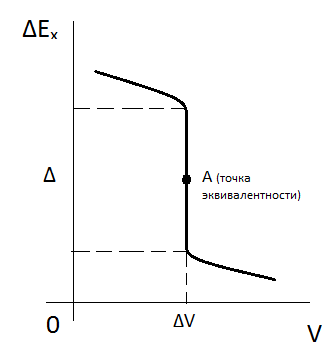
36. Методы потенциометрического титрования
В процессе потенциометрического титрования определяют точку эквивалентности и концентрацию растворов. Этот метод используется при титровании окрашенных мутных растворов.
Сущность метода: в области близкой к точке эквивалентности происходит резкое изменение измерений разности потенциалов (). Малейшее изменение объема добавляемого титранта, вызывает это резкое изменение.
Для определения точки эквивалентности концентрации раствора используют следующие способы потенциометрического титрования:
осаждение
переведение в малодиссоциируемые комплексы
окислительно-восстановительное титрование
титрование в неводных растворах
титрование смесей ионов
37.
З-н
Фарадея:
Согласно з-ну Ф по количеству электричества,
израсходованного на электролитическое
выделение элемента из р-ра, можно
определить количество выделевшегося
эл-та. ![]() ,
,
где q – колич электричества, А*с;
m – масса выделившегося в-ва, г;
n – число электронов, участв в р-ции;
F – число Ф =9,65*104 Кл/моль.
