
- •1.Абсолютная и относительная погрешности.
- •2 Классификация погрешностей по форме представления:
- •3 Способы выявления систематической погрешности
- •Выполнение анализа независимыми методами.
- •Проведение холостого опыта или анализа.
- •Метод стандартных образцов
- •4 Случайные погрешности
- •5. Генеральная и выборочная совокупность
- •6. Среднее арифметическое выборочной совокупности. Случайное отклонение.
- •7. Выборочное стандартное отклонение. Дисперсия
- •8. Среднеквадратичное отклонение
- •9. Нормальное распределение
- •10. Распределение Стьюдента
- •11. Требование к пробе анализа. Генеральная, средняя, лабораторная и анализируемая проба
- •12. Отбор проб газов, жидкостей и твердых веществ.
- •13.Отбор проб продуктов питания и продовольственного сырья.
- •14. Принципы подготовки проб к анализу.
- •15. Метод разложения проб
- •16. Растворение проб.
- •17. Сплавление пробы.
- •18. Пиролиз пробы.
- •19. Методы разделения и концентрирования проб.
- •20. Сущность титриметрии
- •21. Стандартизация растворов титрантов.
- •22. Точка эквивалентности
- •23. Точка конца титрования
- •24. Кривые титрования
- •25. Способы титрования
- •26. Индикаторы и правила выбора индикатора
- •27. Гальванический элемент
- •28. Общие принципы электрохимических методов анализа. Классификация электродов и электродных систем.
- •29. Метод прямой кондуктометрии
- •30. Безэлектродная кондуктометрия
- •32. Сущность потенциометрического анализа. Окислительно-восстановительный потенциал и его зависимость от концентрации и температуры.
- •33. Методы прямой потенциометрии
- •34. Электроды сравнения и индикаторный электрод
- •35. Ионоселективные электроды
- •1. Первичные:
- •2. Сложные и многомембранные
- •36. Методы потенциометрического титрования
- •38. Сущность кулонометрического анализа.
- •39. Прямая кулонометрия
- •40. Кулонометрия при постоянной силе тока
- •41. Теоретические основы вольтамперометрии
- •43. Методы полярографии
- •44. Метод дифференциальной полярографии
- •45. Инверсионная вольтамперометрия
- •49. Принципиальная схема хроматографа
- •52. Радиоактивность. Методы регистрации радиоактивности
- •42. Схема установки полярографического анализа
- •42. Схема установки полярографического анализа
- •1.Абсолютная и относительная погрешности.
- •2 Классификация погрешностей по форме представления:
26. Индикаторы и правила выбора индикатора
Индикаторы – в-ва, кот изменяют свою окраску при изменении рН.
В качестве индикаторов применяют:
Лакмус, кот в кисл среде – красн, в щелочн – синий;
Фенолфталеин, кот в кисл среде – бесцвет, в щелочн – малиновый;
Метилоранжевый, кот в кисл среде - розовый, в щелочной – желт.
У правильно выбранного индикатора интервал перехода окраски должен полностью или частично перекрываться скачком титрования. Если такого перехода нет, то индикатор для данного титрования не подходит.
В частности для кислот – основн титрования использ лакмус, метилоранжевый, метилкрасный, фенолфталеин.
Для фиксирования точки стехеометричности по промежуточ оттенкам окраски индикатора вводят такое понятие как показатель титрования, кот соотвевт значен рН, при кот заканчивается титрование, при кот находится конечная точка титрования.
Необходимо знать, что погрешность титр может быть обусловлена тем, что рН индикатор сам имеет кислот-осн природу, т.е. наличие индикатора в р-ре изменяет его рН, следовательно, колич необходимо ограничивать при добавлении в р-р, т.е. обходиться минимальным его колич. Кроме этого на погрешность влияет ещё то, что добавление индикатора вызывает постепенное разбавление р-ра, а также из-за увеличения воды, кот получ в результате реакции: Н+ + ОН- = Н2О.
27. Гальванический элемент
Гальвани́ческий элеме́нт — химический источник электрического тока. Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока. Главные составные части гальванических элементов: два электрода разл. природы и электролит. Обычно электроды - это металлич. пластинки или сетки, на к-рые нанесены реагенты ("активные в-ва"); на отрицат. электрод - восстановитель (Zn, Li и др.), на положительный -окислитель (оксиды Mn, Hg и др., а также соли). На каждом из электродов, погруженных в электролит, устанавливается определенный потенциал (окислит.-восстановит. потенциал данной электродной р-ции); разность этих потенциалов в отсутствие тока наз. напряжением разомкнутой цепи (НРЦ). При соединении электродов между собой с помощью внеш. электрич. цепи электроны начинают перетекать от отрицат. электрода к положительному - возникает электрич. ток. Суммарная электрохим. р-ция на обоих электродах наз. токообразующей; по мере ее протекания восстановитель отдает, а окислитель присоединяет электроны. Ток прекращается при размыкании внеш. цепи, а также после израсходования запаса хотя бы одного из реагентов. ЭДС гальванического элемента зависит от материала электродов и состава электролита.
28. Общие принципы электрохимических методов анализа. Классификация электродов и электродных систем.
Данные методы анализа связаны с направленным движением заряженных частиц, т. е. с электрическим током, возникающим при действии ЭДС или разности потенциалов. В электрохимических процессах электрический ток протекает в проводниках второго рода – электролитах, т. е. в растворах веществ. Заряженными частицами в электролитах явл-ся положительные и отрицательные ионы, образующиеся при электролитической диссоциации полярных молекул диссоциированного вещ-ва (различных солей, кислот, оснований) полярными молекулами р-ля (воды) или другими физико-химическими механизмами.
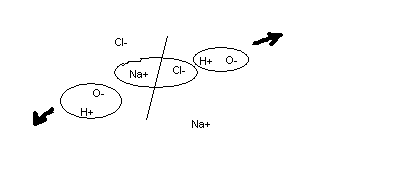
В электрохимических устройствах имеется как min 2 электрода, причем на одном из них постоянно или в данный момент времени возникает или подается положительный потенциал, а на втором электроде – отрицательный. При этом положительные ионы электролита будут двигаться к отриц электроду, а отрицательные – к положит. Возникает ток в электролите.

И только возле самих электродов возможна отдача отрицательными ионами электронов плюсовому электроду, а плюсовые ионы могут забрать электроны у отрицательного электрода.
Электроды и электродные системы классифицируются:
- по агрегатному состоянию: твердые (металлические), жидкие (ртуть), газообразные (водород)
- кинематическому исполнению: неподвижные, подвижные (совершают поступательное и вращат движение)
- по контакту с электролитом: контактирующие, безконтактные
- по способу взаимодействия с электролитами: пассивные, активные (могут растворяться в электролитах)
- твердые электроды: металлические (золото), неметалич (графит)
- электродные системы: с наложением тока из вне (с электродам подается внешняя ЭДС), без наложения тока из вне.
