
- •1.Абсолютная и относительная погрешности.
- •2 Классификация погрешностей по форме представления:
- •3 Способы выявления систематической погрешности
- •Выполнение анализа независимыми методами.
- •Проведение холостого опыта или анализа.
- •Метод стандартных образцов
- •4 Случайные погрешности
- •5. Генеральная и выборочная совокупность
- •6. Среднее арифметическое выборочной совокупности. Случайное отклонение.
- •7. Выборочное стандартное отклонение. Дисперсия
- •8. Среднеквадратичное отклонение
- •9. Нормальное распределение
- •10. Распределение Стьюдента
- •11. Требование к пробе анализа. Генеральная, средняя, лабораторная и анализируемая проба
- •12. Отбор проб газов, жидкостей и твердых веществ.
- •13.Отбор проб продуктов питания и продовольственного сырья.
- •14. Принципы подготовки проб к анализу.
- •15. Метод разложения проб
- •16. Растворение проб.
- •17. Сплавление пробы.
- •18. Пиролиз пробы.
- •19. Методы разделения и концентрирования проб.
- •20. Сущность титриметрии
- •21. Стандартизация растворов титрантов.
- •22. Точка эквивалентности
- •23. Точка конца титрования
- •24. Кривые титрования
- •25. Способы титрования
- •26. Индикаторы и правила выбора индикатора
- •27. Гальванический элемент
- •28. Общие принципы электрохимических методов анализа. Классификация электродов и электродных систем.
- •29. Метод прямой кондуктометрии
- •30. Безэлектродная кондуктометрия
- •32. Сущность потенциометрического анализа. Окислительно-восстановительный потенциал и его зависимость от концентрации и температуры.
- •33. Методы прямой потенциометрии
- •34. Электроды сравнения и индикаторный электрод
- •35. Ионоселективные электроды
- •1. Первичные:
- •2. Сложные и многомембранные
- •36. Методы потенциометрического титрования
- •38. Сущность кулонометрического анализа.
- •39. Прямая кулонометрия
- •40. Кулонометрия при постоянной силе тока
- •41. Теоретические основы вольтамперометрии
- •43. Методы полярографии
- •44. Метод дифференциальной полярографии
- •45. Инверсионная вольтамперометрия
- •49. Принципиальная схема хроматографа
- •52. Радиоактивность. Методы регистрации радиоактивности
- •42. Схема установки полярографического анализа
- •42. Схема установки полярографического анализа
- •1.Абсолютная и относительная погрешности.
- •2 Классификация погрешностей по форме представления:
22. Точка эквивалентности
ЭКВИВАЛЕНТ – некая реальная или условная частица числа Х, которая в данной кослотно-основной реакции эквивалентна 1 иону Н+ (реже иону ОН-) или в данной реакции окисления-восстановления эквивалентна 1 электрону.
Под условной частицей (структурным элементом) понимают как реально существующие частицы (электроны, ионы, атомы, молекулы), так и доли этих частиц, иногда их группы.
Фактор эквивалентности и эквивалент данного вещества являются непостоянными величинами, а зависят от стехиометрии реакции, определяющей число ионов водорода в реакции либо число полученных или отданных электронов в реакции.
Точка эквивалентности (в титриметрическом анализе) — момент титрования, когда число эквивалентов добавляемого титранта эквивалентно или равно числу эквивалентов определяемого вещества в образце. Точкой эквивалентности называется момент, наступающий в ходе титрования, когда реагирующие вещества полностью прореагировали. В этот момент они находятся в эквивалентных количествах, т.е. достаточных для полного, без остатка, протекания реакции.
23. Точка конца титрования
В точке эквивалентности наблюдается резкое изменение электропроводности.
Титрование проводят до точки конца титрования, когда с помощью приборн.методов устанавливают соответствие эквивалентности титранта и титруемого вещества. Точка конца титрования соответствует точному объему добавленного титранта, кот. не меньше эквивалент-го объема титранта, т.е. равно или чуть больше, эта точка устанавливается индикатор.методами, физико-хим.инструм-ми методами.
В индикаторных методах чаще всего исп.цветной индикатор, кот.изменяет свой цвет.
24. Кривые титрования
Кривая титрования – это график зависимости pH, оптической плотности или каких-либо других характеристик титруемого раствора (ось ординат) от объема добавленного титранта (ось абсцисс). Масштаб оси абсцисс всегда линейный, а оси ординат может быть линейным или логарифмическим. Линейный масштаб удобен для тех методов контроля за титрованием (спектрофотометрия, амперометрия), в которых контролируемый параметр меняется с концентрацией линейно, а логарифмический – в случае логарифмического изменения (например, при потенциометрии с ионоселективным электродом). Логарифмический масштаб часто используют при визуальном определении конечной точки титрования, поскольку именно в этом масштабе наиболее наглядно проявляется резкое изменение свойств раствора вблизи точки эквивалентности.
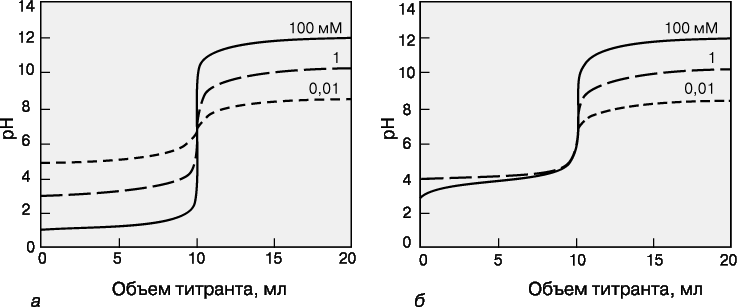 КРИВЫЕ
ТИТРОВАНИЯ сильной кислоты сильным
основанием (а) и слабой кислоты (pKa = 5)
сильным основанием (б) для разных
концентраций определяемого вещества.
КРИВЫЕ
ТИТРОВАНИЯ сильной кислоты сильным
основанием (а) и слабой кислоты (pKa = 5)
сильным основанием (б) для разных
концентраций определяемого вещества.
25. Способы титрования
В титриметрии испол. 3 способа титрования: прямое, обратное и по заместителю.
Прямое титрование – титров. р-ра опред.вещества А непосредственно р-м титранта В. Его применяют в том случае, если р-я между А и В протекает быстро. Содержание комп-та А при прямом титр-нии титрантом В рас-ся на основе р-ва п(А)=п(В). В кач-ве примера определ.в-ва сп-м прямого тит-я след.р-я титр-я:
CH3COOH + NaOH CH3COONa + H2O
n (CH3COOH)=n (NaOH)
Обратное титр-е зак-ся в добавлении к опред.в-ву А избытка точно известного к-ва станд.р-ра В и после завершения р-ии между ними осущ.титров-е ост-гося кол-ва в-вар-м титранта В’. Этот способ применяют в тех случаях, когда р-я между А и В протек.нед.быстро, либо нет подх-гоиндикатора для фиксир-я точки экв-ти этой реакции. Пример:
CaCO3 + 2HCl (из-к) CaCl2 + CO2 + H2O
HCl (ост) + NaOH NaCl + H2O
n(1/2 CaCO3)=n(HCl)- n(NaOH)
Титрование по заместителю з-ся в титр-ии титрантом В не опред.в-ва А, а экв-го ему кол-ва з-ля А’, получив-гося в рез-те предвар.провед-й р-ии между опред.в-м А и каким-либо реагентом. Титров-е по з-лю примен.обычно в тех случаях, когда невозможно провести прямое титрование.
К-во молей эк-та опред-го в-ва титр-ии з-ля всегда равно к-ву молей эк-та титранта п(А)=п(В)=п(А’). пример:
K2Cr2O7 + 6KI + 7H2SO4 Cr2(SO4)3 + 3I2 (з-ль) + 4K2SO4 + 7H2O
I2 + 2Na2S2O3 2NaI + Na2S4O6
n(K2Cr2O7)= n(I2)= n(Na2S2O3)
