
- •Термогравиметрия
- •1. Введение
- •2. Краткая история термического анализа
- •3. Получение и запись кривых нагревания
- •3. 1. Температурные кривые нагревания (т)
- •3. 2. Дифференциальные кривые нагревания (дта)
- •3. 3. Геометрические элементы дта кривой
- •4. Получение термогравиметрических кривых (тг)
- •4. 1. Термогравиметрическая кривая (тг)
- •4. 2. Геометрические элементы тг кривой
- •4.3. Дифференциальная термогравиметрическая (дтг) кривая
- •5. Основы количественного метода дта
- •5. 1. Количественные расчеты тепловых эффектов в методе дта, основанные на модели гомогенного распределения температур в образце (метод Шпейля)
- •5. 2. Количественные расчеты тепловых эффектов в методе дта, основанные на уравнениях теплопроводности и температурного градиента в образце
- •5. 3. Количественные расчеты тепловых эффектов в методе дта, основанные на определении постоянной времени и термического сопротивления
- •Измерение величины тепловых эффектов по кривым дта
- •6. 1. Методы измерения площадей
- •6. 2. Определение калибровочного коэффициента k
- •6. 2. 1. Определение k по энтальпиям плавления веществ
- •6. 2. 2. Электрическая калибровка приборов по эффекту Джоуля
- •6. 2. 3. Определение рабочей чувствительности приборов дта
- •6. 2. 4. Определение величины термических эффектов методом дта
- •7. Обзор методов термического анализа
- •7. 1. Термогравиметрия (тг)
- •7. 1. 1. Применения тг
- •7. 2. Дифференциальный термический анализ (дта) и дифференциальная сканирующая калориметрия (дск)
- •7. 2. 1. Дифференциальный термический анализ (дта)
- •7. 2. 2. Дифференциальная сканирующая калориметрия (дск)
- •7. 2. 3. Градуировка и интерпретация кривых дта и дск
- •7. 2. 4. Применения дта и дск
- •Определение степени чистоты вещества
- •Другие применения
- •7. 3. Комбинированные методы
- •7. 3. 1. Комбинация методов, осуществляемых одновременно
- •7. 3. 2. Пример использования комбинированного анализа
- •7. 3. 3. Дериватография
- •Обработка дериватограммы
- •Определение кристаллизационной воды в кристаллогидрате ВаСl2∙2н2о Вычисление процентного состава кристаллогидрата
- •Определение реакционной способности вещества (энергии активации)
- •Метод Пилояна
- •7. 4. Другие термоаналитические методы
- •7. 4. 1. Термомеханические методы
- •Термодилатометрия
- •Термомеханический анализ (тма) и динамический механический анализ (дма)
- •Высокотемпературная рентгеновская дифракция (рд)
- •Контрольные вопросы
- •Заключение
- •Список рекомендуемой литературы
- •Термогравиметрия
- •614990, Пермь, ул. Букирева, 15
- •614990, Пермь, ул. Букирева, 15
Обработка дериватограммы
Подписать полученные кривые (Т, ТГ, ДТГ, ДТА). В лабораторном журнале записать: дату проведения опыта, формулу исследуемого вещества, массу навески, условия проведения опыта (чувствительность весов, скорость и время нагрева, атмосферу, в которой нагревалось вещество).
Обозначить температуры начала и конца реакции, стадий процесса, температуры пиков на кривой ДТА, дать характеристику наблюдаемым изменениям кривых:
а) физический или химический процесс происходит на данной стадии нагревания вещества;
б) сколько стадий составляют процесс дегидратации данного кристаллогидрата, определить температурный интервал каждой стадии;
в) определить энергетику каждой стадии процесса (эндотермический, экзотермический процесс).
Сделать расчет потери массы вещества (воды), для всего процесса и для каждой стадии отдельно. Потерю воды выразить в граммах, процентах и молях.
Предложить схему процесса дегидратации. Оформить отчет о проведенной работе.
Определение кристаллизационной воды в кристаллогидрате ВаСl2∙2н2о Вычисление процентного состава кристаллогидрата
Пусть масса навески составляет 0,1941 г (194,1 мг). Мr(ВаС12) = 208,3 г/моль. Мr(ВаСl2∙2Н2О) = 244,3 г/моль.
Молекула кристаллогидрата содержит 2 молекулы воды, что составляет 14,7 % массы молекулы. Следовательно, на одну молекулу воды придется 7,35 % массы.
Рассчитаем, какое количество воды будет удаляться на каждой стадии процесса. Считаем, что вся потерянная масса приходится на воду.
Стадия I. Температура начала - 80°С, температура конца - 122°С. Изменение массы на кривой ТГ по дериватограмме составляет
7,3 %. Согласно расчетам, это соответствует потере 1 молекулы воды. Потеря массы на данной стадии составит 194,1∙ 0,073 = 14,17 мг.
Стадия II. Температура начала - 122°С, температура конца - 172°С. Изменение массы на второй стадии составляет 7,4 %, что также соответствует потере 1 молекулы воды. Таким образом, на данной стадии потеря массы составит 194,1∙ 0,074 = 14,36 мг.
Общая потеря массы – 14,7 % или 28,53 мг от навески кристаллогидрата. Такое количество вещества соответствует потере всей кристаллизационной воды в молекуле ВаСl2∙2Н2О (см. расчет процентного состава кристаллогидрата).
ЛАБОРАТОРНАЯ РАБОТА 2
Определение реакционной способности вещества (энергии активации)
Существует целый ряд методов (Пилояна, Шатавы, Коутса-Редферна) определения кинетических параметров по данным неизометрической кинетики.
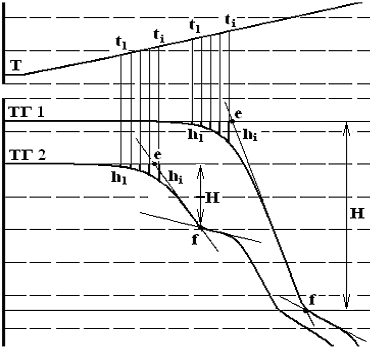
Рис. 7. 19. Прием обработки кривых изменения массы для вычисления степени превращения.
На рисунке 7. 19 представлены различные виды кривых изменения массы.
Энергия активации процесса определяется по тангенсу угла наклона прямой, построенной по данным термографии (термогравиметрической кривой ТГ). Для этого на всей ступени кривой изменения массы ТГ через равные промежутки берут точки 1, 2, 3, 4 и т.д. (ТГ 1 на рис. 7. 19). Для каждой точки вычисляют α-степень превращения, которую находят как отношение высоты (hi) кривой при данной температуре (ti) ко всей высоте ступени (H):
![]() и т.д.
и т.д.
Если вследствие температурного дрейфа участки кривой ab и cd наклонены (ТГ 2 на рис. 7.19), для определения h и Н пользуются следующим приемом: к линейным участкам кривой проводят три касательные и через точки их пересечения е и f чертят прямые, параллельные оси времени. Расстояние между этими прямыми - это величина Н. Значения α и соответствующие ей температуры используют для построения графиков.
