
- •Термогравиметрия
- •1. Введение
- •2. Краткая история термического анализа
- •3. Получение и запись кривых нагревания
- •3. 1. Температурные кривые нагревания (т)
- •3. 2. Дифференциальные кривые нагревания (дта)
- •3. 3. Геометрические элементы дта кривой
- •4. Получение термогравиметрических кривых (тг)
- •4. 1. Термогравиметрическая кривая (тг)
- •4. 2. Геометрические элементы тг кривой
- •4.3. Дифференциальная термогравиметрическая (дтг) кривая
- •5. Основы количественного метода дта
- •5. 1. Количественные расчеты тепловых эффектов в методе дта, основанные на модели гомогенного распределения температур в образце (метод Шпейля)
- •5. 2. Количественные расчеты тепловых эффектов в методе дта, основанные на уравнениях теплопроводности и температурного градиента в образце
- •5. 3. Количественные расчеты тепловых эффектов в методе дта, основанные на определении постоянной времени и термического сопротивления
- •Измерение величины тепловых эффектов по кривым дта
- •6. 1. Методы измерения площадей
- •6. 2. Определение калибровочного коэффициента k
- •6. 2. 1. Определение k по энтальпиям плавления веществ
- •6. 2. 2. Электрическая калибровка приборов по эффекту Джоуля
- •6. 2. 3. Определение рабочей чувствительности приборов дта
- •6. 2. 4. Определение величины термических эффектов методом дта
- •7. Обзор методов термического анализа
- •7. 1. Термогравиметрия (тг)
- •7. 1. 1. Применения тг
- •7. 2. Дифференциальный термический анализ (дта) и дифференциальная сканирующая калориметрия (дск)
- •7. 2. 1. Дифференциальный термический анализ (дта)
- •7. 2. 2. Дифференциальная сканирующая калориметрия (дск)
- •7. 2. 3. Градуировка и интерпретация кривых дта и дск
- •7. 2. 4. Применения дта и дск
- •Определение степени чистоты вещества
- •Другие применения
- •7. 3. Комбинированные методы
- •7. 3. 1. Комбинация методов, осуществляемых одновременно
- •7. 3. 2. Пример использования комбинированного анализа
- •7. 3. 3. Дериватография
- •Обработка дериватограммы
- •Определение кристаллизационной воды в кристаллогидрате ВаСl2∙2н2о Вычисление процентного состава кристаллогидрата
- •Определение реакционной способности вещества (энергии активации)
- •Метод Пилояна
- •7. 4. Другие термоаналитические методы
- •7. 4. 1. Термомеханические методы
- •Термодилатометрия
- •Термомеханический анализ (тма) и динамический механический анализ (дма)
- •Высокотемпературная рентгеновская дифракция (рд)
- •Контрольные вопросы
- •Заключение
- •Список рекомендуемой литературы
- •Термогравиметрия
- •614990, Пермь, ул. Букирева, 15
- •614990, Пермь, ул. Букирева, 15
4. 2. Геометрические элементы тг кривой
Для реакции одностадийного разложения твердых тел ТГ кривая имеет следующие характеристики (см. рис. 4. 1): участок АВ – плато, где еще не наблюдается изменения массы, т.е. термической реакции нет. Точка В соответствует температуре ti, при которой начинается разложение. Конечная температура tf в точке С соответствует максимальному значению изменения массы и окончанию реакции. Точка ts является точкой перегиба кривой ВС и имеет большое значение при изучении кинетики реакции разложения. Для точного определения температуры начала разложения ti необходимо, чтобы весы обладали высокой чувствительностью.
Температурный интервал реакции определяется как разность конечной tf и начальной ti температур (Δt= tf - ti).
Для эндотермических реакций при увеличении скорости нагревания наблюдается рост ti и tf, причем tf растет быстрее, чем ti.
4.3. Дифференциальная термогравиметрическая (дтг) кривая
Математически ДТГ
кривая это зависимость
![]() (скорость изменения массы, как функция
от температуры).
(скорость изменения массы, как функция
от температуры).
Запись ДТГ кривых ведется автоматически (рис. 4. 3 б), путем электронного дифференцирования сигнала ТГ кривой (рис. 4. 3 а). Ранее построение ДТГ кривых проводилось путем расчета. Однако графическое построение ДТГ кривой на основании полученной ТГ кривой трудоемко и не дает точных результатов.
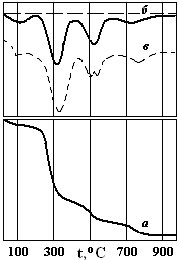
Рис. 4. 3. ТГ кривая потери веса боксита (а), построенная по ТГ кривой ДТГ кривая потери веса (б) и автоматически построенная кривая ДТА нагревания боксита (в).
В Венгрии был разработан и сконструирован прибор – дериватограф, который при исследовании вещества методом термического анализа позволяет одновременно записывать Т, ТГ, ДТГ и ДТА кривые. Запись ДТА кривой совместно с ТГ и ДТГ имеет ряд преимуществ перед записью только одной ТГ кривой:
По внешнему виду кривые ДТА и ДТГ очень похожи между собой (рис. 4. 3 б и в). ДТГ кривые лучше воспроизводимы, чем ДТА кривые. Однако ДТА кривые регистрируют термические эффекты, которые не сопровождаются потерей массы.
При одновременной записи обеих кривых ДТА и ДТГ для одного и того же образца легче судить о характере и механизме превращения в изучаемом веществе.
По кривым ДТГ более точно определяются температуры начала и конца реакции, а по пику ДТГ кривой - температура максимальной скорости реакции. Однако не следует отождествлять температуру пика ДТГ кривой с температурой полного разложения.
ДТГ кривая по максимуму пиков позволяет лучше различать перекрывающиеся стадии реакции.
Так как ДТГ кривая является производной от ТГ кривой, то площадь, заключенная между ДТГ кривой и нулевой линией, точно соответствует изменению массы, определенной по ТГ кривой. Такое количественное интегрирование по площади, полученное из ДТГ кривой, очень полезно при изучении кинетики термических реакций.
ДТГ кривая, так же как и ТГ, не отражает всех термических эффектов, которые имеют место при нагревании исследуемого твердого вещества. Например, полиморфные превращения на ТГ и ДТГ кривых не регистрируются, так как они не сопровождаются изменением массы. Поэтому для всестороннего исследования необходимо наряду с кривыми потери массы получать также кривые ДТА, причем запись всех кривых следует производить в одном опыте при работе с одной и той же навеской.
