
Актуальные вопросы современной гепатологии
.pdf8. Контроль эффективности лечения.
Перед проведением манипуляции обязательным является лабо- раторно-инструментальное обследование больного, включающее в себя клинический анализ крови с определением тромбоцитов, показателей свертывающей системы крови, группы крови, резусфактора, RW, ВИЧ.
УЗИ органов брюшной полости позволяет уточнить размеры печени, определить ее анатомическое строение, топографические отношения с соседними органами, выявить наличие очагового образования печени, а также уточнить расположение желчного пузыря. Это поможет предупредить возможное повреждение крупных сосудов в воротах печени, желчного пузыря и других внутренних органов.
Предварительное обследование позволяет выявить противопоказания для проведения манипуляции, определить способ проведения исследования (чрескожная слепая биопсия или прицельная биопсия под контролем УЗИ).
Необходимо получение информированного согласия больного на проведение исследования.
Абсолютные противопоказания к проведению пункционной биопсии печени:
—Геморрагический диатез, склонность к кровотечениям (снижение протромбинового времени < 60%, MHO > 1,2, АЧТВ > 35 сек, время кровотечения > 7 мин), тромбоцитопения — число тромбоцитов < 70000.
—Гнойные процессы в печени, брюшной и плевральной по-
лостях.
—Инфицированные поражения кожи в месте пункции (пиодермия, фурункулез).
—Билиарная гипертензия, в том числе холангит с признаками билиарной гипертензии.
—Признаки выраженной портальной гипертензии.
—Напряженный асцит.
—Коматозное состояние.
—Психическое заболевание пациента.
Наличие очаговых образований печени (гемангиомы, опухоли, кисты и т.д.) является абсолютным противопоказанием для проведения чрескожной слепой пункционной биопсии печени. В этом случае проводится прицельная биопсия под контролем УЗИ.
221
Относительные противопоказания:
—Сердечная недостаточность (НК II-III).
—Гипертоническая болезнь II-III ст., повышение на момент манипуляции АД (> 140-150 и 80-90 мм рт. ст.).
—Анемия.
—Асцит.
—Воспалительные заболевания внепеченочной локализации в фазе обострения (ОРВИ, бронхит, пневмония, холецистит, панкреатит, язвенная болезнь в стадии обострения, цистит, пиелонефрит и т.д.).
При наличии относительных противопоказаний биопсию печени проводят в случае необходимости после специальной подготовки больного и проведения медикаментозной коррекции.
С помощью анализа биоптатов печени можно определить не только стадию фиброза. Использование специфических красителей (например, Sirius red), а также морфометрия позволяют более точно оценить динамику фиброза у пациента. Эти подходы особенно важны при проведении исследований.
Таким образом, биопсия печени помогает получить: - информацию об этиологии; - информацию о кофакторах;
-возможность иммуногистохимических, биохимических и биомолекулярных исследований;
- возможность определения содержания железа; - возможность классификации по активности выраженности
фиброза («золотой стандарт»).
Эластография
Поиск методов неинвазивной диагностики ФП становится предметом многочисленных исследований последних лет, поскольку именно фиброз служит «связующим звеном» между воспалением и формированием собственно цирроза печени. Одним из методов выявления и оценки степени ФП является инструментальное определение эластичности печени — кратковременная эластография, положенная в основу принципа работы аппарата "ФиброСкан" (Echosens, Франция) (рис. 9), который позволяет за короткий промежуток времени (5-7 минут) определить наличие и степень выраженности фиброза печени.
222
Рисунок 9. Аппарат «ФиброСкан» для выполнения эластографии печени
Основная рабочая часть аппарата представлена ультразвуковым преобразовательным датчиком, в который встроен источник колебаний средней амплитуды и низкой частоты. Генерируемые им колебания передаются на подлежащие исследуемые ткани печени и создают упругие волны, подвергающие модуляции отраженный ультразвук. Скорость распространения упругих волн определяется эластичностью печеночной ткани. Суммарный объем подвергающейся исследованию печеночной ткани составляет в среднем 6 кубических см, что многократно превышает таковой при пункционной биопсии печени (рис. 10).
223
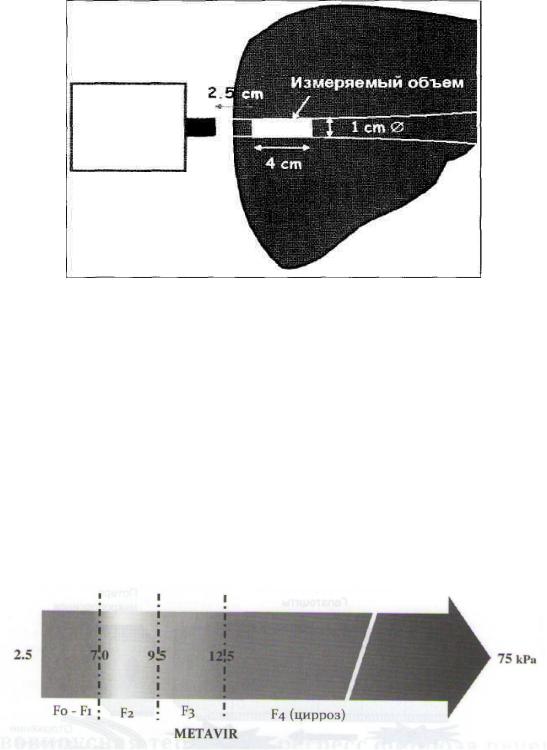
Рисунок 10. Объем ткани печени для оценки ее эластичности
Результаты эластографии печени коррелируют со стадиями ФП, оцененными при гистологическом исследовании. В соответствии с классификацией ФП по K.G.Ishak среднее значение эластичности составляет при 0-1 стадиях ФП 6,3 килоПаскаль (кПа), при 2-4 стадиях — 10,6 кПа, при 5-6 стадиях — 18,7 кПа, клинически манифестный ЦП соответствует эластичности печени в 22,7 кПа. При оценке степени ФП по METAVIR стадия F2 соответствует среднему значению эластичности 7,1 кПа, F3 - 9,5 кПа, F4 -
12,5 кПа (рис.11).
Рисунок 11. Клиническая интерпретация данных эластометрии печени
(Castera L., Forns X., Alberti A., 2008)
Необходимо принимать во внимание, что эластография позволяет с наибольшей вероятностью отличить выраженный фиброз (F3 и F4) от его отсутствия (F0) или минимальной степени выраженности (F1). Так, при значениях эластичности более 14 кПа диагности-
224
ческая точность идентификации фиброза печени составляет 82,6 %, чувствительность и специфичность – 72,6 и 93,5% соответственно. По данным M.Ziol (2005), коэффициент корреляции показателей эластичности печени со степенью фиброза по системе METAVIR составил всего 0,79 для F2, в то время как для F3 – 0,91 и для
F4 – 0,97.
Естественное течение хронического гепатита С ведет к формированию ЦП в среднем у 20% больных при существенных индивидуальных различиях в скорости прогрессирования фиброза (В.Т. Ивашкин, 2005). С позиции современной гепатологии в определении прогноза прогрессирования ХГС, разработки индивидуальной тактики ведения больного, схемы диспансерного наблюдения важное значение принадлежит пункционной биопсии печени, целью которой служит определение индекса гистологической активности и стадии ФП. Особенно актуально ее выполнение у больных, инфицированных 1-м или 4-м генотипами HCV при постоянно нормальном или субнормальном уровне АЛТ, что не исключает прогрессирования заболевания с развитием ЦП (Т.М. Игнатова, 2005). Поэтому в первую очередь именно при ХГС активно изучаются возможности неинвазивной оценки степепи ФП, в том числе с помощью эластографии, и на сегодняшний день этот метод получил наибольшее распространение для диагностики и оценки степени ФП при хроническом гепатите С.
Большинство авторов высоко оценивают точность эластографии в уточнении наличия ФП и степени его выраженности у больных ХГС, в первую очередь, при высоких градациях ФП. По данным C. Baldaia (2005), чувствительность метода составляет 90,3%, а специфичность — 97,3%. В качестве сравнения приводятся данные по сывороточным маркерам ФП: чувствительность и специфичность индекса APRI — 86 и 63%, соотношение АСТ/АЛТ — 15 и 67%, уровень ГГТ — 38 и 73% соответственно.
F.Serejo и соавт. (2006) отмечают корреляцию результатов эластографии с сывороточной концентрацией N-терминального пептида проколлагена III типа, выраженностью инсулинорезистентности по показателям НОМА-индекса, уровнем ГГТ и возрастом. Авторы констатируют, что после успешной противовирусной терапии комбинацией Пег-ИФН-α и рибавирина плотность паренхимы печени составила в среднем 5,13 кПа (4,27 – 6,05), в то время как у неот-
225
ветивших на лечение среднее значение этого показателя равнялось 8,02 кПа (5,78 - 22,06). У здоровых добровольцев плотность печени соответствовала 4,5 кПа (3,3 - 5,69). Таким образом, возможно применение эластографии для косвенной оценки динамики гистологических изменений на фоне лечения вирусных гепатитов.
Эластография мало применима при резко выраженном ожирении, узких межреберных промежутках, при больших объемных образованиях печени, при наличии асцита. Если в отношении хронических вирусных гепатитов роль эластографии печени в диагностике и уточнении стадии ФП можно считать определенной, то для других нозологических форм ее диагностическое значение еще предстоит оценить.
Широкое внедрение эластографии печени в клиническую практику позволит существенно облегчить и ускорить обследование больных хроническими диффузными заболеваниями печени, а также осуществлять динамическое наблюдение как за естественным течением болезни, так и за изменением скорости прогрессирования фиброза под влиянием терапии.
Непрямая ультразвуковая эластография легка в проведении и стала очень популярной. Сейчас предложено использование акустической импульсно-волновой эластографии (ARFI) и магнитнорезонансной эластографии.
Неинвазивные маркеры фиброза печени
Потребность в неинвазивных диагностических маркерах фиброза печени объясняется несколькими причинами:
1. Во всем мире миллионы людей инфицированы вирусом гепатита С. Только у сравнительно небольшой их части (примерно у 25%), вероятно, развивается выраженный фиброз или цирроз, максимальная распространенность которого ожидается в 2015-2020 гг. Существующие методы лабораторного анализа сыворотки крови не позволяют выявить лиц с риском развития прогрессирующего фиброза.
Таким образом, у постоянно увеличивающегося числа больных возрастает потребность в биопсии печени с целью оценки фиброза.
Если будут разработаны неинвазивные методы, действительно позволяющие исключить наличие выраженного фиброза, то этим больным не потребуется противовирусная терапия. Более того, они
226
смогут находиться под постоянным наблюдением, подтверждающим отсутствие прогрессирования фиброза.
2.Увеличивающееся число данных, убедительно свидетельствующих об обратимости фиброза, позволяет считать, что тщательный анализ может позволить рассчитывать на успех лечения даже при тяжелом течении заболевания.
3.В ожидании прогресса антифибротической терапии появится потребность в раннем и постоянном мониторинге за ответом на лечение, позволяющим оценить эффективность и оптимизировать применяемые дозы препаратов. Возможность осуществления такого частого контроля существенно превысит возможности биопсии печени.
Таким образом, имеется ряд причин, заставляющих внедрять неинвазивные (альтернативные) методы диагностики ФП:
- «Ошибка образца» при биопсии печени и погрешности в получении материала.
- Межисследовательские различия в трактовке морфологической характеристики образца.
- Наличие противопоказаний к пункционной биопсии и невозможность во всех случаях предупредить осложнения.
- Необходимость выполнения нескольких биопсий в течение жизни одному пациенту.
Идеальный сывороточный маркер должен отвечать нескольким требованиям. Он должен быть специфичным для печени, независимым от метаболических сдвигов, легко определяться и подвергаться минимальным отклонениям при нарушениях мочевыделения и экскреции желчи.
Сывороточный маркер должен отражать формирование фиброза при всех вариантах хронической патологии печени, коррелировать с изменениями состава матрикса и быть достаточно чувствительным тестом для определения разных стадий фиброза, начиная с минимального и заканчивая ЦП. Эти маркеры должны также отражать реакцию на успешное лечение с применением антифибротической терапии.
Современные методы исследования содержания в сыворотке крови единичных молекул матрикса или фрагментов неспецифичны для патологии печени. Они могут отражать нарушение печеночного клиренса и часто недооценивают «немой» ЦП, так как лучше кор-
227
релируют с воспалением. Фиброз печени годами может протекать бессимптомно, причем показатели многих проб выходят за пределы нормы лишь на поздних стадиях патологического процесса. Они не позволяют дифференцировать ранние стадии фиброза.
Оценка этих тестов непосредственно не связана с патогенезом изменений клеток, свойственных фиброзу печени, а скорее отражают синтетическую способность или развитие воспаления в печени. Более того, некоторые физиологические состояния, например фибротический процесс в легких, также ассоциируется с увеличением уровня маркеров фиброза.
Ни один из маркеров не соответствует критериям, достаточным для использования в обычной клинической практике. Отдельные маркеры часто коррелируют с развивающимся фиброзом у большой группы пациентов, но этого бывает недостаточно для индивидуальной оценки фиброза у конкретного больного, особенно при продолжительном динамическом наблюдении за ним.
Однако последние наблюдения свидетельствуют о том, что использование нескольких маркеров в одной и той же пробе сыворотки позволяет с большей вероятностью дифференцировать минимальные изменения от выраженного фиброза. Эти исследования направлены на определение продуктов распада составных элементов и ферментов внеклеточного матрикса, регулирующих их образование.
Серологические маркеры фиброза печени разделяют на прямые (биомаркеры), отражающие метаболизм экстрацеллюлярного матрикса (ЭЦМ), и непрямые (суррогатные), свидетельствующие о нарушении функции печени при выраженном фиброзе или циррозе печени.
Прямые серологические маркеры ФП классифицируются согласно их молекулярной структуре (табл. 4). Данные вещества непосредственно вовлечены в метаболизм ЭЦМ и включают маркеры фиброгенеза, фибролиза и ряд цитокинов.
К маркерам накопления ЭЦМ относятся карбокситерминальный пептид проколлагена I типа, аминотерминальный пептид проколлагена III типа, тканевые ингибиторы металлопротеиназ, трансформирующий фактор роста-β (ТФР - β), коллаген IV типа.
Маркеры деградации ЭЦМ представлены карбокситерминальным и ами-нотерминальным пептидами проколлагена IV типа и
228

матриксными металлопротеиназами. Гиалуроновая кислота и YKL40 в большей степени отражают фиброгенез, однако являются и участниками фибролиза, отражая ремоделирование ЭЦМ.
В настоящее время показана прямая корреляция между уровнем прямых сывороточных маркеров и стадией ФП, в связи с чем прямые серологические маркеры ФП применяются для определения стадии процесса, оценки эффективности лечения и прогнозирования течения заболевания.
Таблица 4
Классификация прямых серологических маркеров фиброза печени
Коллаген
-карбокситерминальный пептид проколлагена I типа
-аминотерминальный пептид проколлагена III типа
-коллаген IV типа и его фрагменты (карбокситерминальный и аминотерминальный пептиды)
Гликопротеины и полисахариды
-гиалуроновая кислота
-ламинил и его фрагменты
-YKL-40
Коллагеназы и их ингибиторы
-металлопротеиназа
-тканевые ингибиторы металлопротеиназ
Цитокины
-трансформирующий фактор роста – β
-фактор роста тромбоцитов
Прямые маркеры фиброгенеза
Показано, что уровень карбокситерминального пептида про-
коллагена I типа увеличивается в крови у больных на стадии цирроза печени (алкогольного), в то время как на стадии стеатогепатита его уровень остается неизменным.
Сывороточный уровень аминотерминального пептида прокол-
лагена III типа коррелирует со стадией ФП при алкогольной болезни печени, вирусных гепатитах и при первичном билиарном циррозе, однако помимо фиброза он также отражает выраженность некротических изменений в ткани печени, коррелируя с индексом гистологической активности.
229
Сывороточный уровень коллагена IV типа и его фрагментов
(карбокситерминальный и аминотерминальный домены проколла-
гена IV типа) достоверно коррелируют со степенью ФП у больных хроническим вирусным гепатитом, алкогольной болезнью печени и гемохроматозом. При хроническом гепатите С уровень коллагена IV типа более 110 мг/мл свидетельствует о F2 стадии ФП, а уровень более 130 мг/мл - о F3.
Ламинин — основной неколлагеновый гликопротеин, сывороточный уровень которого, а также уровень пепсин-резистентного фрагмента ламинина увеличиваются при хронических диффузных заболеваниях печени любой этиологии, отражая наличие, в первую очередь, перисинусоидального фиброза. Уровень ламинина коррелирует со степенью ФП и активностью воспаления в печени при хроническом гепатите С. Показана прямая связь между уровнем ламинина и индексом Child-Turcotte-Pugh, осложнениями цирроза печени, портальным давлением и градиентом давления в печеночных венах.
Гиалуроновая кислота — гликозамингликан, повышение уровня которого наблюдается при заболеваниях печени различной этиологии при наличии ФП. Уровень гиалуроновой кислоты в сыворотке менее 60 мг/л исключает значительный ФП, в том числе ЦП. Уровень гиалуроновой кислоты 85 мг/л позволяет с чувствительностью 64,5% и специфичностью 91,2% указать на выраженный ФП, а уровень 110 мг/л с чувствительностью 79,2% и специфичностью 89.4% — на ЦП. Однако сывороточный уровень гиалуроновой кислоты коррелирует не только со стадией ФП, но и со степенью воспалительных изменений в печени.
YKL-40 (хондрекс) — представитель семейства хитиназ (18гликозилгидролаз), являющийся фактором роста фибробластов, уровень которого коррелирует со стадией ФП. При ХГС сывороточный уровень YKL-40 более 284,8 нг/мл предсказывает наличие ЦП с чувствительностью 80% и специфичностью 71%.
Маркеры фибролиза
Процесс деградации ЭЦМ опосредуется матриксными металлопротеиназами (МП), для которых в качестве антагонистов вы-
ступают специфические тканевые ингибиторы металлопротеиназ
(ИМП). Согласно субстратной специфичности МП подразделяют на 5 типов: интерстициальные коллагеназы (МП -1, -8. -13), жела-
230
