
Актуальные вопросы современной гепатологии
.pdfимеются изменения биохимических параметров сыворотки крови (повышение уровня АЛТ), а у некоторых возможно развитие тяжелой паренхиматозной желтухи. Со временем формируется цирроз печени, который долго может оставаться компенсированным, но у 25-30% пациентов неуклонно прогрессирует, приводя к смерти (до 25% - в детском возрасте). В то же время частота развития цирроза к 50 годам составляет 18%, среди мужчин она может достигать
20-25%.
Диагностика заболевания связана с сопоставлением результатов клинико-лабораторных исследований (биохимический анализ крови, определение концентрации α1-антитрипсина в сыворотке крови, рентгенологическое исследование легких) и генетического анализа полиморфного гена, выполняемого методом ПЦР.
Синдром желтухи в клинике инфекционных болезней
Гепатит А
Вирус гепатита A (HAV - Hepatitis A virus) - гепатотропный вирус семейства Picornaviridae рода Hepatovirus, передающийся преимущественно фекально-оральным путем и способный вызывать острый гепатит у человека и некоторых обезьян. Это небольшой РНК-содержащий вирус, лишенный оболочки. Из всех РНК-содержащих вирусов HAV - наименее вариабельный. Несмотря на это, выделено по меньшей мере 4 генотипа и 7 подтипов HAV. Наиболее распространены I и III генотипы. Выделенные в России штаммы принадлежат к подтипу IA. Не обнаружено значимых различий биологических и антигенных свойств отдельных генотипов HAV. Существование единственного иммунодоминантного эпитопа вируса обусловливает синтез в организме хозяина высокоэффективных нейтрализующих антител, а также облегчает проведение активной и пассивной иммунизации при HAV-инфекции.
Вирус гепатита А распространен повсеместно, его считают одним из наиболее устойчивых к воздействию факторов внешней среды. Факторы риска инфицирования: контакт с больным, недавнее путешествие, пребывание в очаге вспышки гепатита А, проживание в общежитии. У 42% лиц уточнить источник инфицирования не удается. Отмечены случаи заражения вирусом при гемотрансфузии или введении препаратов крови, контакте с инфицированными
111
вирусом приматами. Группы профессионального риска инфицирования HAV: обслуживающий персонал больниц, работники социальных служб, сотрудники детских учреждений. Вышеуказанным категориям лиц, а также лицам, планирующим поездки в эндемичные по HAV страны, целесообразно проведение активной профилактики (вакцинации).
Гепатит А - типичная кишечная инфекция с фекальнооральным механизмом передачи возбудителя. Вирус выделяется больными во внешнюю среду наиболее интенсивно в конце инкубационного и в преджелтушном периодах. С появлением синдрома желтухи заразительность больных при ГА существенно уменьшается. Основные пути передачи - водный, пищевой и бытовой. Факторы передачи - различные пищевые продукты, не подвергающиеся термической обработке, а также вода и грязные руки. Крупные вспышки болезни связаны с загрязнением фекалиями водоемов, являющихся источником водоснабжения, или с попаданием сточных вод в водопроводную сеть. В детских коллективах вирус может передаваться через грязные руки и различные предметы обихода (игрушки, посуду, белье и т.д.).
Заподозрить ГА можно на основании острого начала болезни, появления высокой температуры тела, диспепсических и астеновегетативных явлений, короткого преджелтушного периода, увеличения печени, улучшения самочувствия и нормализации температуры тела при появлении желтухи, значительного повышения активности АЛТ и ACT, гипербилирубинемии, высокого показателя тимоловой пробы, указания на контакт с больным желтухой или пребывание в эндемичных очагах в сроки, соответствующие инкубационному периоду (35 дней) и др. Специфическим маркером ГА являются антитела к вирусу гепатита А класса М. Прогноз благоприятный, в подавляющем большинстве случаев наступает полное выздоровление, формирования хронического гепатита не происходит. Тяжелое течение ВГА наблюдается редко, обычно в том случае, если заболевание развивается на фоне имеющегося поражения печени (хронический гепатит различной этиологии, цирроз печени и др.).
112
Гепатит Е
Вирус гепатита Е (HEV - Hepatitis E virus) - основной возбу-
дитель эндемического гепатита острого течения с фекальнооральным путем передачи, представляющий наибольшую опасность для беременных. Впервые HEV идентифицирован при анализе замороженных образцов сывороток больных гепатитом, развившимся в результате потребления загрязненной воды в ходе наводнения 1955 г. в Индии. Сочетает таксономические признаки семейства Caliciviridae и некоторых фуровирусов растений. Это лишенный оболочки вирус диаметром 32-34 нм с икосаэдральным типом симметрии. Популяция HEV структурно гетерогенна: сравнительный анализ геномов и аминокислотных последовательностей вируса из Азии (Бирмы, Китая, Пакистана и бывших советских республик) и Северной Америки (Мексики) выявил 77 и 87-90% степень гомологии. В настоящее время выделен единственный перекрестно реагирующий эпитоп, на его основе разработан метод серологической диагностики HEV-инфекции.
Гепатит Е - эндемичное заболевание. HEV становится причиной более 50% случаев острого гепатита в странах экваториального пояса, включая страны Центральной Америки, Африки, Среднего Востока, субконтинентальной Индии и Юго-Восточной Азии. В этих регионах вспышки заболеваемости регистрируют каждые 5-10 лет. В периоды между эпидемиями возникают спорадические случаи заболевания гепатитом Е, способствующие сохранению вируса в человеческой популяции. HEV обнаружен у свиней, однако случаев передачи вируса от свиньи человеку не зафиксировано. Уровень общей смертности, связанной с HEV-инфекцией, составляет 0,5-4%. Наиболее высокие показатели заболеваемости гепатитом Е отмечены в возрастном диапазоне от 15 до 40 лет. В детском возрасте заболевание чаще протекает субклинически и проходит незамеченным. Иммунитет при HEV-инфекции нестерильный: у перенесших безжелтушную форму сохраняется возможность реинфицирования.
Инкубационный период составляет от 20 до 65 дней, чаще около 35. В клинической картине преобладают признаки, характерные для гепатита А. Однако в начальном периоде лихорадочная реакция слабо выражена. Больных чаще беспокоят общая слабость, отсутствие аппетита, тошнота, ноющие боли в правом подреберье и
113
эпигастральной области. Продолжительность начального периода составляет 5-6 дней. С появлением желтухи выраженность синдрома общей интоксикации не уменьшается, что отличает гепатит Е от гепатита А. Желтушный период болезни длится 2-3 недели.
Особого внимания заслуживает гепатит Е у женщин во второй половине беременности: у 20-25% из них заболевание может приобретать злокачественное течение по фульминантному типу с быстрым развитием массивного некроза печени и острой печеночной энцефалопатии. При этом нередко возникает ДВС-синдром и отмечается усиленный гемолиз, сопровождающийся гемоглобинурией, приводящей к острой почечной недостаточности. Тяжелое течение гепатита Е часто заканчивается самопроизвольным прерыванием беременности, которое сопровождается резким ухудшением состояния больных женщин. Необходимо отметить, что даже при доношенной беременности более половины детей, родившихся живыми, умирают в течение первого месяца жизни. Специфическим маркером гепатита Е служит обнаружение в сыворотке крови антител класса IgM. Хронические формы заболевания и вирусоносительство не зарегистрированы.
Острый гепатит В
Вирион вируса гепатита В («частица Дейна») – сферическая частица диаметром 42 нм, состоит из ядра – нуклеокапсида, имеющего форму икосаэдра диаметром 28 нм, внутри которого находится двуцепочечная ДНК, концевой белок и фермент ДНКполимераза. В состав нуклеокапсидного белка – HВcAg входит HBеAg. Внешняя оболочка (толщиной 7 нм) образована поверхностным антигеном вируса гепатита В – HВsAg.
Дэвид Морис Суррей Дейн (1923-1998) родился 25 марта 1923 года в Англии. Получил медицинское образование в Clare College (Кембридж), затем проходил клиническую ординатуру в St. Thomas Hospital (Лондон). После специализации в области микробиологии в 1955 году Дейн стал сотрудником отделения и лаборатории Queens University (Белфаст), где и прошла в основном вся его блестящая медицинская карьера.
Вскоре после открытия Б.Бламбергом «австралийского антигена», Дейн с коллегами стал изучать маркеры вирусного гепатита В. В 1970 году Дэвид Дейн вместе с Колином Камероном и Моей
114
Биггс при помощи электронной микроскопии выявили в сыворотке крови полноценный вирион вируса гепатита В, который вскоре получил название «частицы Дейна». Вся последующая медицинская деятельность Дейна была посвящена в первую очередь обеспечению безопасности при переливании донорской крови и профилактике посттрансфузионного заражения различными вирусами.
Вирус гепатита В (HBV - Hepatitis В virus) - гепатотропный вирус, принадлежащий семейству Hepadnaviridae и связанный с развитием у человека гепатита, чаще острого (в том числе фульминантного), реже хронического течения, с относительно высокой частотой формирования ГЦК. Небольшой сферической формы вирион гепатита В (частица Дейна) состоит из частично удвоенной циркулярной молекулы ДНК, окруженной нуклеокапсидом и липопротеидной оболочкой. Геном HBV содержит четыре частично перекрывающиеся открытые рамки считывания (pre-S/S, P, рге-С/С и X), несущие информацию о белках вируса (поверхностных, ДНКполимеразе, core- и Х-протеинах соответственно).
Основная часть белков липопротеидной оболочки вируса представлена HBsAg, или S-протеином. HBsAg представляет собой комплекс белков, образующих наружную оболочку вируса. Это основной скрининговый маркер HBV, его сохранение в сыворотке крови более 6 месяцев указывает на хроническую HBV-инфекцию. Синтез поверхностной оболочки вируса определяется S-геномом вируса, состоящим из трех участков (доменов) - pre-Sl, pre-S2 и S, они кодируют синтез большой, средней и главной субъединиц HBsAg соответственно. Одна из специфических особенностей HBV - интенсивный синтез HBsAg, который в виде сферических частиц и трубочек секретируется в кровь, а также откладывается в виде филаментов в цитоплазме гепатоцитов, придавая им своеобразную окраску (матово-стекловидные гепатоциты). HBsAg имеет различные детерминанты: общую для всех типов а-детерминанту, а также d, у, w, r. Установлено около десяти субтипов поверхностного антигена, основные из них - adw, adr и ayw. Их определение имеет значение для изучения эпидемиологии вируса.
Минорную фракцию поверхностных белков HBV составляют L- и М-протеины, их образование происходит путем присоединения к S-протеину дополнительных аминокислотных последовательностей, информация о которых содержится в pre-Sl и pre-S2 областях генома вируса. Мутации в pre-S/S области генома HBV могут быть
115
связаны с изменением инфекционных и иммуногенных свойств вируса: pre-S/S мутанты вируса не всегда обнаруживают при стандартном скрининге на HBV, они могут вызывать заболевание, несмотря на вакцинацию (вакцинускользающий штамм HBV), приводить к развитию тяжелого быстро прогрессирующего гепатита (фиброзирующего холестатического гепатита В) из-за нарушения экскреции HBsAg из гепатоцита.
Нуклеокапсид HBV, защищающий вирусную ДНК от расщепления эндогенными нуклеазами, образован 180 копиями coreантигена вируса [HBcAg - сердцевинный (ядерный) антиген HBV]. HBcAg в сыворотке крови не обнаруживают. Смещение сайта инициации трансляции в рге-соге область сопровождается синтезом HBеAg. Р-участок генома кодирует полимеразу вируса, сочетающую в себе свойства как эндогенной ДНК-полимеразы, так и обратной транскриптазы, родственной обратным транскриптазам вируса иммунодефицита человека (ВИЧ). Функциональная роль Х- протеина HBV до конца не ясна, однако представляется важной для репликации вируса. Предполагают, что Х-протеин выполняет функцию активатора транскрипции, регулирующего, подобно ВИЧ, активность соответствующего промотера.
Максимальная экспрессия генов HBV происходит в печени, хотя последовательности ДНК и белков вируса идентифицированы в клетках почек, селезенки, поджелудочной железы, костного мозга, крови. В отличие от классических ретровирусов, таких как ВИЧ, HBV для его размножения не нужно встраиваться в геном хозяина. Напротив, включение вирусной ДНК в геном хозяина, хотя и становится важным канцерогенным фактором, в то же время разрушает ее пространственную структуру, приостанавливает репликацию вируса.
Помимо частиц Дейна, сыворотка крови и печень больных HBV-инфекцией содержат неинфекционные вирусные частицы, участвующие в синтезе нейтрализующих перекрестно реагирующих антител. В связи с тем, что все серотипы вируса имеют общую детерминанту, микст-инфекцию несколькими вариантами HBV встречают нечасто. В настоящее время выделяют 8 основных генотипов вируса (А-Н), каждый из них имеет несколько подтипов с характерным ореолом распространения. По предварительным данным, некоторые генотипы HBV могут различаться чувст-
116
вительностью к противовирусной терапии (ПВТ), подверженностью мутациям, риском хронизации заболевания и темпами прогрессирования поражения печени.
HBV широко распространен в мире: в настоящее время насчитывают около 500 млн носителей вируса. За последние 20 лет заболеваемость гепатитом В значительно снизилась в результате проведения широкомасштабных мероприятий по предотвращению распространения ВИЧ, вакцинации против HBV, внедрения более совершенных методов скрининга HBV в крови доноров.
Таблица 9
Мутантные варианты вируса гепатита В
Мутация |
Молекулярный эффект |
Клиническая |
|
значимость |
|||
|
|
||
S - ген |
Исчезновение группоспеци- |
«Ускользание от вакцины» |
|
|
фической детерминанты «а» |
«Ускользание от диагно- |
|
|
|
стики» |
|
Pre – Core |
Исчезновение антигена HBe |
Отрицательные результаты |
|
стоп-кодон |
|
теста на антиген HBe |
|
Ядерный ген |
Нарушенное Т-клеточное |
Более тяжелое клиническое |
|
|
распознавание |
течение |
|
Ядерный |
Усиленная репликация |
Более тяжелое клиническое |
|
промотор |
вируса |
течение |
|
|
|
Фульминантный гепатит |
|
Ген |
Устойчивость к аналогам |
Устойчивость к ламивудину |
|
полимеразы |
нуклеозидов или нуклеоти- |
и адефовиру |
|
|
дов |
|
|
Х-ген |
Подавление антипролифера- |
Развитие печеночно- |
|
|
тивных и апоптотических |
клеточной карциномы |
|
|
механизмов |
|
Острый гепатит В (ОГВ) - антропоноз с контактным и вертикальным механизмом передачи возбудителя. Источником вируса являются больные с различными формами HBV-инфекции, в основном с хроническими (преимущественно вирусоносители). Пути передачи возбудителя - естественный (вертикально - при передаче вируса от матери к ребенку, контактно - при использовании предметов быта и при половых контактах) и искусственный (артифициальный), который реализуется при гемотрансфузиях инфицированной крови или ее препаратов и любых парентеральных манипуляциях (медицинского и не медицинского характера), сопро-
117
вождающихся нарушением целостности кожного покрова и слизистых, если манипуляции проводились инструментами, контаминированными кровью, содержащей вирус ГВ. Заподозрить ОГВ можно на основании постепенного начала болезни с появления астеновегетативных и диспепсических явлений, артралгии, экзантемы (чаще всего - крапивницы), преджелтушного периода, продолжающегося от 2 до 4 недель, увеличения печени, существенного повышения активности АЛТ и ACT, гипербилирубинемии, указаний на наличие факторов риска инфицирования вирусом ГВ в сроки, соответствующие инкубационному периоду и др. Специфическими маркерами ОГВ являются HBsAg и анти-HBcIgM. Прогноз при ОГВ в целом благоприятный, более 90% больных выздоравливают, вместе с тем возможны летальные исходы (около 1 %). Хронический гепатит В формируется у 5% больных, у части из которых возможно формирование цирроза печени и первичного рака печени.
Острый гепатит D
В 1977 году группа итальянских исследователей, изучая ткань печени больных хроническим гепатитом В методом иммунофлюоресценции, обнаружили в ядрах гепатоцитов новый белок, который был назван дельта-антигеном. Впоследствии было установлено, что
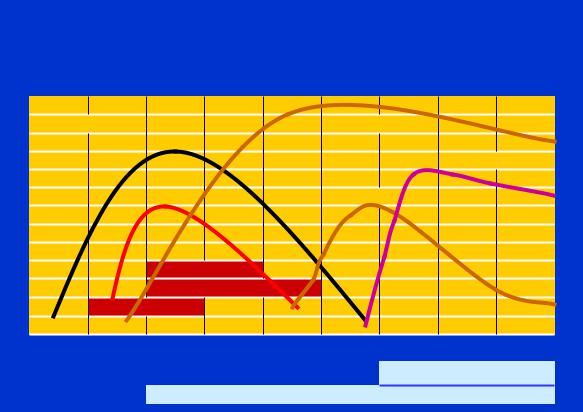
Динамика серологических маркеров гепатита В
Концентрация маркеров |
Анти-HBc |
HBsAg |
|
|
Анти-HBs |
HBeAg |
Анти-HBe |
Cимптомы |
АЛТ |
ДНК-полимераза |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
месяцы |
|||
|
|
|
|
|
|
|
|
|
|
|
после заражения |
|
|
Важнейшие |
HBsAg |
|
|
|
|
|
Анти-HBs |
|
|
||
маркеры |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
7 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Анти-HBc-IgM |
|
|
|
|
|
Анти-HBc-IgG |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
118
этот белок является структурным компонентом нового вируса, получившего название вирус гепатита D. Он представляет собой сферическую частицу диаметром около 36 нм, внутри которой находится нуклеокапсид диаметром 19 нм, содержащий РНК вируса.
Вирус гепатита D (HDV - Hepatitis Delta virus) - "дефектный"
по своей структуре вирус, преимущественно с парентеральным путем передачи, приводящий у инфицированных HBV лиц к формированию поражения печени острого, хронического или, как стало очевидно из наблюдений за больными после трансплантации печени, латентного течения. Сочетает в себе таксономические признаки вироидов и сателлитных вирусов растений.
Вирион HDV - небольшая частица сферической формы, морфологически сходная с частицей Дейна - содержит однонитевую циклическую РНК положительной полярности. HDV не экспрессирует собственные белки оболочки, в качестве которых использует npe-S- и S-протеины HBV, необходимые не только для сборки вириона (основная форма HBsAg), но и для прикрепления HDV к клетке-мишени и его распространения от клетки к клетке (L-форма
HBsAg).
Известны три различных генотипа:
-Генотип I (во Франции, Италии, США и Японии, на острове Тайвань, а также в Ливане). Имеются данные о роли данного генотипа в развитии фульминантного гепатита в России.
Генотип IА (преимущественно в Азии). Генотип IВ (преимущественно в США).
-Генотип II (распространен в Японии). В 2001 году имела место эндемия в Якутии.
-Генотип III (в Южной Америке). В 2001 году описана вспышка среди индейского населения Венесуэлы.
В мире насчитывается 15 миллионов человек, инфицированных HDV, что составляет приблизительно 5% носителей HBsAg. Эндемичные по гепатиту D регионы включают Италию, отдельные области Восточной Европы, бассейн Амазонки, Колумбию, Венесуэлу, Западную Азию, Тихоокеанские острова. Несмотря на то, что для развития HDV-инфекции необходимо присутствие HBsAg, ореолы распространения HDV не повторяют в точности распространения HBV-инфекции, предполагая наличие дополнительных факто-
119

ров, влияющих на инфекционные и патогенные свойства вируса. Частота инфицирования HDV в общей популяции относительно невелика (1,4-8,0%), при этом значительно выше среди инъекционных наркоманов (20-53%), больных гемофилией и пациентов отделений гемодиализа (48-80%).
Основной путь передачи HDV - парентеральный. Исследование доноров крови на наличие у них HBsAg и анти-НВcor значительно снижает риск инфицирования HDV в результате гемотрансфузии. В развитых странах основная группа риска - инъекционные наркоманы, сохраняется возможность получения вируса в ходе медицинских манипуляций, нарушающих целостность слизистых оболочек и кожных покровов. Не исключен бытовой путь передачи вируса. Инфекционная активность HDV приблизительно на пять порядков ниже, чем у HBV, поэтому половой путь передачи HDV не столь очевиден. Случаи перинатального инфицирования, вертикальной передачи вируса редки. Зависимость патогенного потенциала HDV от экспрессии HBsAg позволяет считать вакцину против гепатита В также средством профилактики HDV/HBV коинфекции. Специфической профилактики HDV-суперинфекции не существует. Диагностика основана на обнаружении в сыворотке крови маркеров HDV (РНК и a-HDV).
Возможно два варианта дельта-вирусной инфекции - одновременное инфицирование вирусом гепатита В и вирусом гепатита D (коинфекция) и инфицирование вирусом гепатита D носителя вируса гепатита В (суперинфекция).
Таблица 10
Клиническое течение коинфекции и суперинфекции вирусом гепатита D
Течение |
Коинфекция |
Суперинфекция |
|
Выздоровление |
90-95% |
5-10% |
|
Фульминантное |
2-20% |
10-20% |
|
течение |
|||
|
|
||
Хроническое течение |
2-7% |
70-95% |
Предположить наличие коинфекции (острого гепатита В с дельта-агентом) можно на основании острого начала болезни с повышением температуры тела, диспепсическими и астеновегетативными явлениями, короткого (5-7 дней) преджелтушного периода,
120
