
Актуальные вопросы современной гепатологии
.pdfроли вируса в развитии заболевания. Первые работы, посвященные изучению гепатита А, продемонстрировали наличие ВГА в фекалиях и крови больных в инкубационный и в течение 2-3 недель желтушного периода.
Максимальная концентрация антигена ВГА регистрируется на поздней стадии инкубационного периода и в продроме. В дальнейшем процент положительных результатов его обнаружения постепенно уменьшается ко второй и третьей неделям желтушного периода и составляет 20 и 5% соответственно.
Определение продолжительности выделения вируса в процессе инфекции имеет важное практическое значение. От того, как долго больной остается опасным для окружающих, зависят сроки его госпитализации в стационаре, время проведения заключительной дезинфекции в очаге и другие противоэпидемические мероприятия.
В сыворотке крови Аг ВГА удается обнаружить значительно реже. Продолжительность виремии меньше (от нескольких часов до нескольких дней), чем период выделения ВГА с фекалиями. Подтверждением факта циркуляции в крови больного HAV и реальности заражения через инфицированную кровь служат зарегистрированные случаи посттрансфузионного гепатита А.
Разработка и внедрение методов выявления РНК открыли новые возможности в лабораторной диагностике гепатита А. Особое значение имеют результаты обнаружения РНК ВГА в сыворотке крови больных. РНК удается обнаружить в период «окна», то есть до появления Ig M анти-ВГА. Учет данного факта важен при диагностике в инкубационный период и при обследовании лиц из очагов инфекции.
РНК ВГА удается определить и в периоды ранней и поздней реконвалесценции. В типичных случаях время циркуляции вируса может достигать 40 дней. Особенно часто длительное обнаружение РНК ВГА в сыворотке крови регистрируется в случаях затяжного гепатита и у лиц с измененным иммунным статусом.
Наличие разнообразных маркеров инфицирования ВГА и методов их тестирования значительно расширило современные диагностические возможности. В таблице 1 представлен перечень этих маркеров с возможной интерпретацией результатов исследования.
21
Таблица 1
Специфические маркеры инфицирования вирусом гепатита А и интерпретация их обнаружения
Маркер инфицирования |
Интерпретация |
вирусом гепатита А |
результата |
Ig M анти-ВГА |
Острый гепатит А |
Ig G анти-ВГА |
Перенесенный гепатит А, защита от |
(суммарные антитела |
гепатита А после вакцинации (›20 |
против ВГА) |
МЕ/л) |
Ig A анти-ВГА |
Перенесенный гепатит А |
АгВГА |
Репликация вируса |
РНК ВГА |
Репликация вируса |
Диагностика гепатита Е
В 90-е годы эпидемическая форма «ни А ни В гепатита», вызывающая вспышки в странах с жарким климатом, была обозначена как гепатит Е. Вирус идентифицирован в 1983 году при проведении эксперимента с заражением добровольца материалами, полученными от больных, у которых был заподозрен гепатит Е (Балаян М.С., 1995). В последующие годы подробно изучены свойства HEV: это частица сферической формы диаметром 27-34 нм с одноцепочечной РНК, не покрытая оболочкой.
Как и при гепатите А, специфическая лабораторная диагностика гепатита Е строится на тестировании комплекса серологических маркеров инфицирования ВГЕ (анти-ВГЕ классов Ig M и Ig G), непосредственно вируса и его компонентов. Для гепатита Е характерно последовательное появление и исчезновение маркеров в ходе заболевания и в процессе выздоровления. Обобщенная схема представлена ниже (рис. 5).
Острый гепатит Е может быть заподозрен в эпидемических случаях у лиц с острым «ни А ни В гепатитом». Иммуноферментный анализ позволяет выявить анти-ВГЕ Ig M и/или Ig G.
Антитела класса Ig M присутствуют в сыворотке от 2 до 24 недель после острого начала болезни. Антитела класса IgG также появляются через 2 недели, и обычно их титр начинает снижаться после 2-х лет, хотя иногда высокие титры могут наблюдаться в течение многих лет. Выздоровление от острого заболевания приводит к пожизненному иммунитету.
22
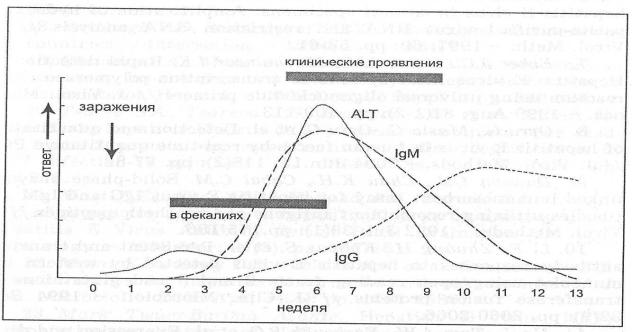
Рисунок 5. Динамика обнаружения маркеров инфицирования ВГЕ при остром гепатите Е
Основным методом исследования, позитивный результат которого свидетельствует о наличии вируса, является метод полимеразной цепной реакции. По мнению A.Anderson и I.Shresta (2002), обнаружение РНК ВГЕ может рассматриваться как «золотой стандарт» лабораторной диагностики гепатита Е. Для подтверждения своих слов авторы ссылаются на данные обнаружения ВГЕ в случаях отсутствия антительного ответа, определяемого на момент обнаружения РНК ВГЕ.
Антитела класса IgA играют важную роль в патогенезе гепатита Е, обеспечивая защиту организма на слизистых оболочках желу- дочно-кишечного тракта, препятствуя дальнейшему проникновению ВГЕ в организм человека.
Обнаружение разнообразных маркеров инфицирования ВГЕ значительно расширило современные диагностические возможности. В таблице 2 представлен их перечень с возможной интерпретацией результатов исследования.
23
Таблица 2
Специфические маркеры инфицирования вирусом гепатита Е и интерпретация их обнаружения
Маркер инфицирования вирусом гепатита Е
Ig M анти-ВГЕ
Ig G анти-ВГЕ (суммарные антитела против ВГЕ)
Ig A анти-ВГЕ АгВГЕ РНК ВГЕ
Интерпретация результата
Острый гепатит Е Перенесенный гепатит Е, защита от гепатита Е Перенесенный гепатит Е Репликация вируса Репликация вируса
Диагностика HCV-инфекции
Вирус гепатита С (HCV) идентифицирован в 1989 году американскими исследователями под руководством M.Houghton, когда была выделена нуклеиновая кислота при экспериментальном заражении шимпанзе и в дальнейшем получена ДНК-копия, которую использовали для создания библиотеки клонов. Скрининг образцов из этой библиотеки позволил выявить клон, экспрессирующий антиген, который реагировал с антителами из сывороток людей, больных посттрансфузионным гепатитом «ни А, ни В». Далее был получен рекомбинантный белок, который содержал последовательность из 363 аминокислотных остатков. Эту последовательность обозначили как С-100-3 и использовали в качестве антигена при создании иммуноферментной тест-системы. В результате стало возможным диагностировать гепатит С и начать его всестороннее изучение.
Вирус гепатита С относится к гепатотропным вирусам, но при этом доказана возможность его внепеченочной репликации, в частности в мононуклеарах крови. Весьма важным свойством этого вируса является способность ускользать из-под иммунного надзора - «immune escape virus». В основе этой способности лежит перманентное и быстрое изменение антигенной структуры, в результате чего вирус воспроизводит себя не в каком-либо постоянном антигенном варианте, а в целой серии близких, но иммунологически различных штаммов (кажущихся разновидностей – «quasispecies»). В отличие от HBV механизм интеграции в геном хозяина вирусу гепатита С не присущ.
24
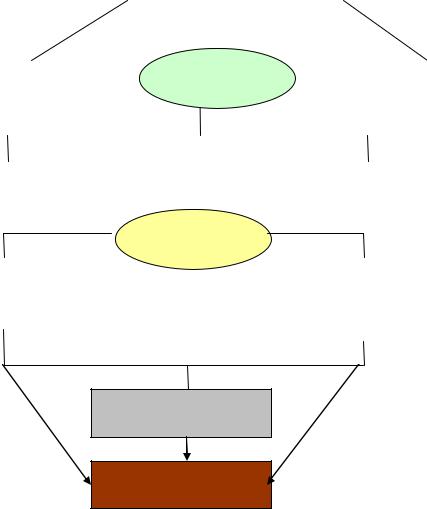
Острый гепатит С (ОГС), как правило, протекает бессимптомно или с минимальными клиническими проявлениями. 70-80% больных предъявляют жалобы только на быструю утомляемость и различной степени выраженности слабость, лишь только у 20-30% больных можно выявить клинически значимые проявления заболевания. Если же имеются признаки желтушного синдрома, то клиническое течение ОГС, лабораторные биохимические тесты, морфологические изменения в ткани печени ничем не отличаются от других вирусных гепатитов. Уникальной особенностью HCV является крайне высокая степень развития хронического гепатита С (рис. 6). Известно, что в 50-90% случаев отмечается неспособность организма к спонтанной элиминации инфекции в зависимости от пути передачи, наличия симптомов гепатита, а также возраста, в котором произошло инфицирование.
|
|
Заражение HCV |
|
|
|
|
|
|
|
|
|
|
|
|
|
Первичная |
|
|
|
|
Бессимптомное течение |
Клинически явная инфекция |
|||||
инфекция |
||||||
75% |
25% |
|||||
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Элиминация вируса |
|
Персистирование инфекции |
|
|
5-20% |
|
|
80-95% |
|
|
|
|
|
|
|
|
Хроническая |
|
|
|
|
инфекция |
|
|
Хронический гепатит |
|
|
|
|
|
|
Хронический гепатит |
|
|
с нормальным уровнем |
|
|
|
|
|
|
с повышенным уровнем |
|
|
аминотрансфераз, 50% |
|
|
|
|
|
|
аминотрансфераз, 50% |
|
|
|
|
|
|
|
|
|
|
|
Цирроз печени 20-30% за 20-30 лет
Гепатоцеллюлярная карцинома 3% в год
Рисунок 6. Течение инфекции, обусловленной вирусом гепатита С
(цит. по L.Garnier, G.Inchauspe, C.Trepo, 2002)
25
Учитывая перечисленные особенности клинического течения HCV-инфекции, само понятие «острый гепатит С» носит скорее символический характер, так как в большинстве случаев инфекция выявляется на хронической стадии заболевания. Условным рубежом, разграничивающим ОГС и ХГС, является срок в 6 месяцев от дебюта клинических симптомов.
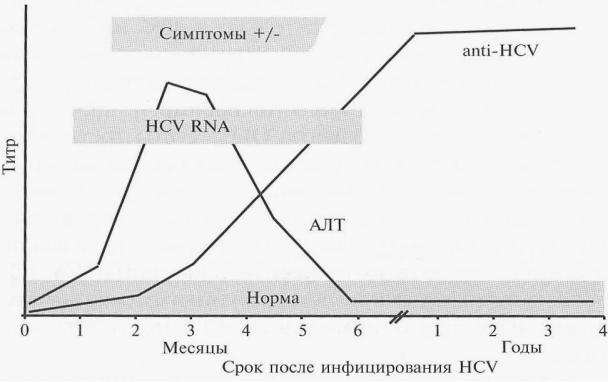
Рисунок 7. Динамика обнаружения маркеров инфицирования HCV при остром гепатите с элиминацией вируса
Только эпидемиологические данные с указанием возможного времени инфицирования анти-HCV после серонегативного периода на фоне персистенции HCV РНК могут достоверно подтвердить диагноз острого гепатита С (рис. 7).
Серологическая диагностика гепатита С имеет ряд особенностей. Основным методом является определение антител к HCV (рис. 8). Наибольшее распространение благодаря своей надежности и чувствительности получил иммуноферментный анализ (enzyme immunosorbent assay, ELISA). Существуют три поколения диагностических иммуноферментных систем, которые различаются своей специфичностью.
26
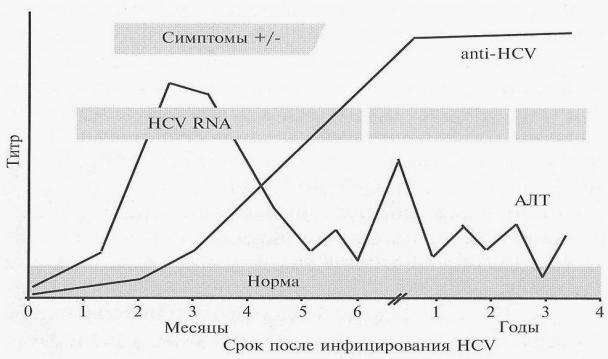
Рисунок 8. Динамика обнаружения маркеров инфицирования HCV при остром гепатите с хронизацией процесса
Трудности при диагностике (ИФА) гепатита С связаны со следующими причинами:
1)отсутствие активной клиники;
2)вирус очень быстро меняется по субтипам;
3)до 20% HCV присутствует в клетках крови;
4)позднее появление антител против вируса;
5)отсутствие вакцинации.
Для того чтобы понять, с чем связаны трудности ИФАдиагностики и отсутствие вакцины к вирусу гепатита С, необходимо представить структуру вируса.
Геном вируса – одиночная цепь РНК – разделен на зоны, в которых заключена информация о структурных и неструктурных белках (рис. 9). Структурная зона представлена следующими участками:
-Core – кодирует ядерные белки;
-E1и E2 (envelop 1 и envelop 2, или NS1 – у некоторых авторов)
–отвечает за синтез оболочечных белков.
Неструктурная зона также разделена на участки NS2, NS3, NS4А, NS4В, NS5А, NS5В, которые содержат информацию о ферментах, определяющих жизнедеятельность вируса.
27
При детальном молекулярно-генетическом исследовании нуклеиновых последовательностей участка NS5 к настоящему моменту обнаружено 6 вариантов генотипа и большое количество субтипов вируса (номенклатура P.Simmonds et al., 1993).
|
|
Трансмем- |
|
РНК-зависимая |
|
|
|
|
РНК- |
||
Белки |
Нуклео- |
бранные |
Кофермент |
||
полимераза |
|||||
капсулы |
капсид |
|
|
||
|
|
|
ядра |
Серинпро- |
|
|
Супрессор |
|
|
теаза РНК- |
|
|
интерферона |
|
|
геликаза |
|
|
|
Соr |
Е1 |
Е2 |
NS2 |
NS3 |
NS4 |
NS4 |
NS5А |
NS5В |
|
|
|
|
А |
В |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Структур- |
Неструктурные белки |
ные белки |
|
Рисунок 9. Структура генома вируса гепатита С. Указаны белки вируса, которые кодируются соответствующими
участками генома
Структурный белок core формирует вирусный нуклеокапсид. Он является одним из наиболее иммуногенных белков вируса и индуцирует мощный Т- и В-клеточный ответ. Показано, что в первый месяц острой фазы гепатита С, когда содержание антител незначительно, только количество core белка увеличивается столь же быстро, как и вирусная РНК. Количественный анализ содержания core белка не выявил различий у будущих реконвалесцентов и хронических больных. После 6 месяцев гепатита С скорость увеличения РНК и белка снижается. Почти все пациенты, выздоровевшие от острого гепатита С, имеют пожизненно анти-core антитела из-за высокой иммуногенности этого белка.
Белок NS2 является вирусной металлозависимой протеиназой и вместе с клеточной пептидазой участвует в аутокаталитическом нарезании самого себя из вирусного полипротеина. Белок NS3 – это вирусная протеиназа, играющая важную роль в процессинге вирус-
28
ных белков. Белок NS4А действует как кофактор для NS3протеолитической активности и регулирует фосфорилирование белка NS5А, который обладает функцией репликазы. Белок NS5В является вирусной РНК-зависимой РНК-полимеразой. В инфицированной вирусом клетки белки NS4А, NS4В, NS5А, NS5В и NS3 ассоциируются в общую структуру, которая играет важную роль в вирусной репликации. Из-за отсутствия 3´-5´ - экзонуклеарной активности эта РНК-полимераза при репликации делает много ошибок, что приводит к высокой скорости мутации. Оба белка области NS5 иммуногенны.
Вострой фазе антитела к неструктурным белкам определяются позднее, чем антитела к структурным белкам. Часто у выздоравливающих пациентов в конце острой фазы происходит снижение титра анти - NS3 антител перед исчезновением вируса. Вероятно, длительно высокие титры антител к NS3 в острой фазе гепатита С можно рассматривать как маркер хронизации. Антитела к NS4 белку в острой фазе детектируются как в высоких, так и в низких титрах вне связи с исходом заболевания. Антитела к NS5 в высоких титрах в конце острой фазы рассматриваются как неблагоприятный признак.
Для надежного выявления вируса гепатита С тест-системы должны иметь несколько (4-6) моноклональных антител к разным структурным эпитопам вируса гепатита С. И даже это не гарантирует, что исследователь не столкнется с очередной модификацией вируса, в которой не будет нужных эпитопов. По мере расширения представлений о структуре вируса методы выявления инфекции становятся все более чувствительными. Высокая изменчивость вируса гепатита С – причина отсутствия до настоящего времени вакцины от этой инфекции.
Тест-система 1-го поколения (ELISA-1) с 1989 года выявляла антитела к антигенам 5-1-1 и С-100-3. Указанные антитела к неструктурным антигенам региона NS3/NS4 определяются только через 3-12 месяцев после инфицирования HCV, специфичность метода составляет 70-80%.
Вдальнейшем были получены новые клоны РНК HCV, продуцирующие другие вирусные антигены для обнаружения соответствующих антител (табл. 3), что привело к появлению 2-го (1991 г.)
и3-го (1993 г.) поколения ELISA. Тесты второй генерации выявляют антитела к core- (С22) и NS3/NS4-антигенам (С33), при этом
29
специфичность составляет более 90%. Положительным данный тест становится через 2-6 месяцев после инфицирования, поскольку гуморальный иммунный ответ на капсидные антигены (структурные белки) начинается быстрее, чем на неструктурные белки. Важно, что только у 40% больных тесты второго поколения положительны через 2 месяца. Таким образом, серологические тест-системы первого и второго поколений не пригодны для подтверждения диагноза острого ГС.
ELISA-3 широко используется для скрининга доноров, являясь значительно более чувствительной и специфичной по сравнению с тест-системами предыдущих поколений. Большое значение имеет возможность выявления с помощью ELISA-3 антител к NS-5 региону, так как до 5% вирусоносителей имеют в крови только данный тип антител, что приводит к ложноотрицательным результатам при использовании первых поколений ELISA.
Использование ELISA-3 дает почти 100% гарантию выявления носителей анти-HCV. Однако в двух случаях антитела могут быть не обнаружены. Во-первых, появление анти-HCV происходит в срок до 6 месяцев после инфицирования (в среднем через 12 недель), то есть в определенный период течения инфекции имеется так называемое «серологическое окно». Во-вторых, антитела могут не выявляться у больных, получавших иммуносупрессорную терапию (например, после трансплантации органов). Кроме того, несмотря на высокую специфичность ELISA-3 (99,7%), возможны также ложноположительные результаты. Важно помнить, что ложноположительные анти-HCV нередко встречаются при аутоиммунных заболеваниях, в том числе при аутоиммунном гепатите, особенно 2 типа. Учитывая это, предложены подтверждающие тесты, такие как рекомбинантный иммуноблотинг (recombinant immunoblot assay, RIBA).
При использовании RIBA антигены HCV наносятся раздельно на полоски нитроцеллюлозы и инкубируются с сывороткой больного. При наличии соответствующих антител происходит их визуализация. Тест-система 3-го поколения (RIBA-3), широко распространенная в Европе, содержит синтетические пептиды core-региона, NS4, рекомбинантные NS3 и NS5 (табл. 3). Результаты RIBA считаются положительными при выявлении антител более чем к одному региону HCV.
30
