
Борзенко,Зайцев
.pdf
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
НИЗКОТЕМПЕРАТУРНЫХ И ПИЩЕВЫХ ТЕХНОЛОГИЙ
Е.И. Борзенко, А.В. Зайцев
УСТАНОВКИ И СИСТЕМЫ НИЗКОТЕМПЕРАТУРНОЙ ТЕХНИКИ
Автоматизированный расчет и моделирование процессов криогенных установок и систем
Учебное пособие
Рекомендовано Учебно-методическим объединением по университетскому политехническому образованию в качестве учебного пособия для студентов
высших учебных заведений, обучающихся по направлению подготовки 140400 «Техническая физика»
1
Санкт-Петербург 2006
2
УДК 536.483, 621.59 ББК 31.392 Б 82
Борзенко Е.И., Зайцев А.В.
Б 82 Установки и системы низкотемпературной техники.
Автоматизированный расчет и моделирование процессов криогенных установок и систем: Учеб. пособие. – СПб.:
СПбГУНиПТ, 2006. – 232 с.
ISBN 5-89565-146-1
Содержит материал, включенный в программу курсов по направлению «Техническая физика» и специальности «Техника и физика низких температур». Рассматриваются алгоритмы расчета термических, калорических и транспортных свойств чистых криогенных рабочих веществ, реальных веществ и их смесей, алгоритмы расчета фазового равновесия многокомпонентных смесей. Приводятся математические модели контактных устройств и колонных аппаратов узлов ректификации криогенных смесей. Анализируются статистические характеристики ректификационных колонн.
Может быть использовано для разработки программного обеспечения курсовых и дипломных проектов студентов, квалификационных работ бакалавров и диссертаций магистрантов, а также полезно для инженеров и аспирантов, занимающихся моделированием криогенных процессов на ЭВМ.
УДК 536.483, 621.59 ББК 31.392
Рецензенты Кафедра Э-4 Московского государственного технического
университета им. Н.Э. Баумана (зав. кафедрой доктор техн. наук, проф. А.М. Архаров).
Доктор техн. наук, проф. М.М. Пеньков (Военно-космическая академия им. А.Ф. Можайского).
Рекомендовано к изданию редакционно-издательским советом университета
ISBN 5-89565-146-1
©Санкт-Петербургский государственный университет низкотемпературных и пищевых технологий, 2006
3

Борзенко Евгений Иванович Зайцев Андрей Викторович
УСТАНОВКИ И СИСТЕМЫ НИЗКОТЕМПЕРАТУРНОЙ ТЕХНИКИ
Автоматизированный расчет и моделирование процессов криогенных установок и систем
Учебное пособие
Редактор Е.О. Трусова Корректор Н.И. Михайлова
Компьютерная верстка А.В. Зайцев Директор ИПЦ Т.Г. Смирнова
Подписано в печать 2006. Формат 60×84 1/16 Печать офсетная. Усл. печ. л. 13,49. Печ. л. 14,5. Уч.-изд. л. 14,0
Тираж 500 экз. Заказ № С 38
СПбГУНиПТ. 191002, Санкт-Петербург, ул. Ломоносова, 9 ИПЦ СПбГУНиПТ. 191002, Санкт-Петербург, ул. Ломоносова, 9
4

1. РАСЧЕТ ПАРАМЕТРОВ СОСТОЯНИЯ РЕАЛЬНЫХ КРИОГЕННЫХ РАБОЧИХ ВЕЩЕСТВ
1.1.Уравнение состояния реальных веществ
Вкриогенных системах и установках в качестве рабочих веществ наиболее широкое применение получили гелий, водород, воздух и такие его основные компоненты, как азот, кислород, аргон, неон, криптон, ксенон, и их смеси. Особенностью криогенных систем является то, что температура и давление рабочих веществ изменяются
вшироких пределах и для описания их свойств, особенно в областях низких температур и высоких давлений, необходимо учитывать характер межмолекулярных взаимодействий, т. е. применять уравнения состояния реального газа.
Простое эмпирическое уравнение состояния реального газа, полученное с учетом сжимаемости 1 кг рабочего вещества, имеет вид
pv = zRT , |
(1.1) |
где p – давление; v – удельный объем; z – коэффициент сжимаемости; R – газовая постоянная; T – температура.
Широко применяются вириальные формы уравнения (1.1) и уточненные эмпирические зависимости с различными индивидуальными коэффициентами, в определенной мере учитывающими многообразие и сложность молекулярных взаимодействий и другие особенности свойств реальных рабочих веществ.
При обобщении экспериментальных данных часто используют вириальное уравнение Боголюбова–Майера [1], которое базируется на наиболее строгом теоретическом подходе и имеет вид
z = pv = 1 + B1*ρ + B2*ρ2 + B3*ρ3 + B4*ρ4 + ...
RT
или в сокращенной форме
∞ |
|
z = 1 + ∑Bi* ρi , |
(1.2) |
i =1
5

где Bi* – вириальные коэффициенты, зависящие от температуры; ρ = 1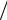 v – плотность.
v – плотность.
Число вириальных коэффициентов в уравнении (1.2) выбирают, исходя из требований к точности обобщения экспериментальных данных; тогда уравнение принимает вид
|
|
|
r |
|
|
|
|
|
|
|
||
|
|
z = 1+ ∑Biρi |
. |
|
|
(1.3) |
||||||
|
|
i =1 |
|
|
|
|
|
|
|
|||
Каждый из вириальных коэффициентов, в свою очередь, |
||||||||||||
записывают как |
|
|
|
|
|
|
|
|
|
|
||
|
|
si |
|
b |
|
|
|
|
|
|
|
|
|
|
Bi = ∑ |
|
ij |
, |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
|
|
j =0 τ j |
|
|
|
|
|
|
|
|||
где si – |
границы изменения j; |
bij |
|
– |
коэффициенты |
разложения; |
||||||
τ = T Tкр |
– |
приведенная температура, |
здесь |
Tкр |
– |
критическая |
||||||
температура. |
|
|
|
|
|
|
|
|
|
|
|
|
Часто |
уравнение Боголюбова–Майера |
(1.3) |
представляют |
|||||||||
в виде [2] |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
r |
|
si |
|
b |
|
|
|
|
||
|
|
z = 1 + ∑ ∑ |
|
ij |
|
ρi . |
|
|
|
|||
|
|
|
τ j |
|
|
|
||||||
|
|
i =1 j =0 |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||
|
|
(1.4) |
|
|
|
|
|
|
|
|
|
|
По мере накопления экспериментальных данных по термодинамическим свойствам рабочих веществ теплоэнергетических установок и систем в научно-технической литературе появилось множество уравнений состояния, описывающих с определенной полнотой и точностью параметры их состояния в p–v–T-пространстве. Наряду с уравнением Боголюбова– Майера получили применение уравнения Битте–Бриджмана, Бенедикта–Рубина [1], а в последние годы – уравнения Рабиновича, Сычева, Вассермана и др. [3–6], взаимосогласованные уравнения
6
Клецкого, уравнения состояния гелия-4 Тарана, Мак-Карти и т. д.
1.2. Расчет параметров состояния криогенных рабочих веществ
Широкое применение электронно-вычислительной техники при проведении расчетно-теоретического анализа криогенных установок вызывает необходимость разработки математического обеспечения вычислительного эксперимента, при этом важное место занимает система расчета термодинамических и теплофизических свойств реальных криогенных рабочих веществ.
Единое уравнение состояния криогенных рабочих веществ.
При разработке системы расчета термодинамических и теплофизических свойств криогенных рабочих веществ в основу было положено уравнение состояния Сычева–Вассермана, которое имеет единую форму для основных криоагентов и обеспечивает относительно высокую точность расчета p–v–T-данных [7].
При аппроксимации экспериментальных данных по основным криогенным веществам было получено уравнение состояния (1.4) в следующем виде:
r si |
i |
|
z = 1+ ∑ ∑bij |
ωρ |
, |
j |
||
i =1 j =0 |
τ |
|
(1.5) |
|
|
где ωρ = ρ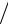 ρкр – приведенная плотность, здесь ρкр – критическая
ρкр – приведенная плотность, здесь ρкр – критическая
плотность.
Для повышения точности описания p–v–T-данных водорода и гелия-4 используют два набора коэффициентов для определенных температурных зон. В связи с тем, что характер изменения термических свойств гелия-4 в области температуры от λ-линии до 25 К значительно отличается от характера изменения их в диапазоне температур от 25 до 1500 К, одно уравнение действует в зоне температур от λ-линии до 25 К, а второе – при значениях T = 15…1500 К. Диапазон 15…1500 К частично охватывает каждое из двух уравнений, поэтому переход от одной группы коэффициентов разложения bij к другой осуществляется
7

при температуре 20 К. Однако необходимо отметить, что уравнение состояния в вириальной форме (1.5) не отображает достоверно поведение термодинамических функций в области критической точки.
Данные о давлении насыщенных паров широко применяются при моделировании процессов в элементах криогенных систем. В связи с этим при разработке алгоритма расчета термодинамического поля рабочих веществ могут быть использованы интерполяционные уравнения [8], в дальнейшем приведенные к виду
n |
|
lg pнас = ∑ fiΘT(i −2) , |
(1.6) |
i =1 |
|
где fi – коэффициенты уравнения; ΘT = T 100 – |
относительная |
температура. |
|
Калорические уравнения для криогенных рабочих веществ.
Калорические уравнения, связывающие энтальпию, энтропию и теплоемкость с давлением и температурой, могут быть получены на основе обобщения экспериментальных данных либо путем интегрирования p–v–T-зависимости. В работах [3–6, 9] используется второй путь и предлагаются формулы для определения следующих значений:
энтальпии
|
|
|
r si |
i + j |
ωρi |
|
|
|
||||
|
h = h0 + RT ∑ ∑ |
|
|
bij |
|
|
; |
|
(1.7) |
|||
|
|
|
τ j |
|
||||||||
|
|
|
i =1 j =0 |
|
i |
|
|
|
||||
энтропии |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ωρ |
r si |
|
j − 1 |
|
ωρi |
|
|
|||
s = s0 |
− R lg |
|
+ R∑ ∑ |
|
|
bij |
|
|
; |
(1.8) |
||
ω0 |
|
|
τ j |
|||||||||
|
|
i =1 j =0 |
i |
|
|
|
||||||
изобарной теплоемкости
8

|
|
|
|
|
|
r si |
|
(ωρi |
2 |
|
r si |
|
|
ωρi |
|
R 1 − ∑ ∑( j − 1)bij |
τ j ) |
||||
j( j − 1) |
|
|
|
i =1 j =0 |
|
|
|
|||
c p = cv0 − R∑ ∑ |
|
bij |
|
+ |
|
|
|
|
|
, (1.9) |
i |
τ j |
|
r si |
|
|
|
||||
|
|
|
|
(ωρi |
τ j ) |
|||||
i =1 j =0 |
|
|
|
|
1 + ∑ ∑(i + 1)bij |
|||||
i =1 j =0
где h0 , s0 , cv0 – энтальпия, энтропия и изохорная теплоемкость в
идеально-газовом состоянии*.
Энтальпию h0 и энтропию s0 определяют из соотношений
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
h0 = ∫c0pdT + h00 + h00 ; |
|
(1.10) |
|||
|
|
|
|
|
T0 |
|
|
|
|
|
|
|
|
|
T |
0 |
|
|
|
|
|
|
|
s0 |
= ∫ |
c p |
dT + s00 + s00 , |
|
(1.11) |
|
|
|
|
|
|
||||
|
|
|
|
|
T |
T |
|
|
|
|
|
|
|
|
0 |
|
|
|
|
где h |
00 |
и s |
00 |
– энтальпия и энтропия при температуре T |
; h0 |
– теплота |
|||
|
|
|
|
0 |
0 |
|
|||
сублимации при T1=10 К; s00 – константа.
Значения констант уравнений (1.7)–(1.11) приводятся в таблице. Изобарную теплоемкость в идеально-газовом состоянии
рассчитывают с помощью полинома
c0 |
|
k |
Θ j |
l |
|
|
= R |
∑α |
+ ∑β |
Θ− j |
, |
||
p |
|
j |
T |
j |
T |
|
|
j =0 |
|
j =1 |
|
|
|
(1.12)
где αj и βj – коэффициенты полинома.
При аппроксимации значений изобарной теплоемкости в идеально-газовом состоянии для азота в полиноме (1.12) вместо ΘT используется значение приведенной температуры τ = T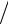 Tкр .
Tкр .
Поскольку изобарная теплоемкость одноатомных газов не зависит от температуры, ее значение в идеально-газовом состоянии
* Здесь и далее рассматриваются удельные калорические параметры.
9

находят по формуле
c0p = 5 R . 2
(1.13)
10
