
Борзенко,Зайцев
.pdf1 – δy = (G9 – G90)/G90; 2 – δlн = (lн – lн0)/lн0;
3 – δG = ( G – GL)/Gн0; 4 – δQн = (Qн – Qн0)/Qн0
После прекращения действия теплового импульса в структурных элементах низкотемпературной ступени охлаждения происходит постепенное восстановление параметров гелиевых потоков, причем скорость их изменения связана с инерционностью структурных элементов.
Из проведенного анализа следует, что импульсные тепловыделения объекта криостатирования при определенных условиях могут вызвать существенные количественные и качественные изменения параметров гелиевых потоков в нижней ступени охлаждения. Это существенным образом сказывается на параметрах работы криогенных машин и аппаратов ступеней предварительного охлаждения системы криогенного обеспечения сверхпроводящих машин и устройств.
52
4. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ФАЗОВОГО РАВНОВЕСИЯ КОМПОНЕНТОВ СМЕСИ
4.1. Термодинамические основы фазового равновесия растворов
Ваппаратах узлов низкотемпературной ректификации применяются двухфазные системы, состоящие из жидкой и паровой фаз и включающие два или более компонентов. На контактных устройствах осуществляется соприкосновение жидкой и паровой фаз,
ив результате тепло- и массообмена происходит непрерывный обмен веществом между фазами, стремящимися к равновесию.
Для определения условий фазового равновесия рассматривают закрытую систему, в которой осуществляется обмен веществом между фазами. В то же время каждая из фаз представляет собой открытую систему, так как является раствором с переменным составом [27].
Вслучае, когда жидкая фаза является идеальным раствором
и описывается законом Рауля, парциальное давление компонента в идеальном растворе pi = psi(T) xi, где psi(T) – давление насыщенного пара чистого компонента при температуре раствора Т; xi – молярная доля компонента в жидкой фазе.
При нахождении равновесных концентраций пара или жидкости часто используют константу фазового равновесия
Ki = |
yi |
, |
(4.1) |
|
|||
|
xi |
|
|
где yi – молярная доля компонента в паровой фазе, а также коэффициент разделения
α |
ik |
= |
Ki |
= |
yi xk |
. |
(4.2) |
Kk |
xi yk |
|
|||||
|
|
|
|
|
|||
|
|
|
|
|
|
||
В частном случае |
|
для |
идеальных |
газов и растворов |
|||
Ki = psi (T )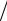 p .
p .
Для идеальных растворов с идеальной газовой смесью в паровой фазе при Т = const коэффициент разделения может быть найден из отношения парциальных давлений компонентов:
53

αik |
= |
|
psi |
(T ) |
|
. |
|
(4.3) |
|||
|
psk |
(T ) |
|
||||||||
|
|
|
|
|
|
|
|||||
Значение концентрации i-го компонента в паровой фазе |
|||||||||||
определяют из уравнения |
|
|
|
|
|
|
|
|
|
|
|
yi = |
|
|
|
αik xi |
|
|
|
. |
(4.4) |
||
|
α |
ik |
x + x |
k |
|||||||
|
|
|
|
||||||||
|
|
|
i |
|
|
|
|||||
Температуру насыщения при фазовом переходе в идеальных
|
k |
растворах по заданному давлению и составу |
∑xi = 1 находят из |
|
i =1 |
трансцендентного уравнения |
|
k |
|
p − ∑ psi (T )xi = 0 . |
(4.5) |
i =1 |
|
Если пар является неидеальной смесью, то для сохранения простой связи между изотермическими изменениями химического потенциала и мерой способности вещества переходить из одной системы в другую вводят величину f – летучесть, или фугитивность. В общем случае летучесть реального вещества является сложной функцией состояния от температуры и давления. Значение летучести приближается к величине давления при сближении свойств реального
вещества со свойствами идеального газа, т. е. |
lim |
f (p,T )= p . |
|||||
|
|
|
|
|
p →0 |
|
|
Отношения |
ψ = f |
p |
и |
ψi |
= fi |
(yi p ) |
называют |
коэффициентами |
летучести |
и |
парциальной летучести, |
a fi – |
|||
парциальной летучестью. |
|
|
|
|
|
|
|
При проведении исследований и решении практических задач удобно оперировать эталонными, или стандартными, состояниями, которые входят в определение «летучесть». Вводя понятие стандартного состояния (обозначено надстрочным индексом 0), получают для компонента смеси ai = fi 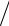 fi0 . Это так называемая относительная летучесть, или активность, а величина, получившая название «коэффициент активности»,
fi0 . Это так называемая относительная летучесть, или активность, а величина, получившая название «коэффициент активности»,
54

γi |
= |
|
fi |
|
(4.6) |
x |
f |
0 |
|||
|
|
i |
|
i |
|
аналогична коэффициенту летучести, или фугитивности, ψi .
Для газов за стандартное всегда принимают такое состояние, в котором летучесть равна единице [28], вследствие чего активность
численно равна летучести, т. е. a |
i |
= f |
|
G |
f |
0 |
= f |
G . |
|
|
i |
|
i |
|
i |
||
Для жидкостей стандартные |
|
состояния конденсированной |
||||||
и паровой фаз должны согласовываться. В качестве определяющего фактора обычно используют давление насыщенного пара, при котором летучесть паровой фазы и летучесть жидкой фазы равны, т.
е. f si = ψsi psi (T ).
Стандартное состояние определяют как состояние чистого вещества при температуре и давлении системы, тогда
|
|
|
|
p |
v |
L |
f |
0L = f |
|
exp |
∫ |
|
|
si |
|
|
||||
|
|
|||||
|
i |
|
RT |
|||
|
|
|
||||
|
|
|
psi (T ) |
|
|
|
dp = ψsi psi (T )(PF )i , |
(4.7) |
|
|
|
|
где vL – молярный объем жидкости; R – газовая постоянная;
(PF ) |
|
p |
|
(RT )dp |
|
∫ |
|
||
= exp |
|
v L |
||
i |
|
|
|
|
|
psi (T ) |
|
||
умеренном давлении, как
– коэффициент Пойнтинга, который при
правило, немного отклоняется от единицы.
Тогда летучесть для жидкой фазы fiL = xi γ fi0L , а константа фазового равновесия для реальных систем пар–жидкость
K |
i |
= |
γi fsi (PF )i |
. |
(4.8) |
|
|||||
|
|
ψi p |
|
||
|
|
|
|
||
Коэффициент активности для i-го компонента многокомпонентной смеси при определенных допущениях может быть определен по уравнению Скэтчарда–Гильденбранда [4]:
|
(δi |
− |
|
)2 |
|
|
|
ln γi = |
δ |
, |
(4.9) |
||||
RTρL |
|||||||
|
|
|
|||||
|
|
|
i |
|
|
||
55
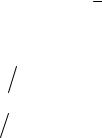
где δi – параметр растворимости компонента; δ – средневзвешенная растворимость смеси,
|
|
∑xiδi ρi2 |
|
|
δ |
= |
i |
. |
|
∑xi ρi2 |
||||
|
|
|
||
|
|
i |
|
Еще более точные значения константы фазового равновесия могут быть получены по экспериментальным данным фазового равновесия бинарных и многокомпонентных систем.
4.2. Расчет фазового равновесия системы жидкость–пар бинарных и многокомпонентных смесей
В криогенной технике разделение смесей чаще всего осуществляют методом низкотемпературной ректификации в сочетании с другими процессами. Среди разделяемых смесей особый интерес представляют воздух, водород, природный газ.
Сухой и очищенный от углеводородных примесей атмосферный воздух представляет собой газовую смесь сложного состава.
Воздух – единственное исходное сырье для получения в промышленных масштабах кислорода, аргона, азота, неона, криптона, ксенона и др. (табл. 4.1).
Фракция низкокипящих компонентов, состоящая из гелия, водорода, неона, находится в ректификационной колонне в газообразном состоянии, накапливается с паром азота под крышкой конденсатора-испарителя нижней колонны, выводится из аппарата, и из нее методом низкотемпературной дефлегмации выделяется неон.
Криптон и ксенон имеют более высокую температуру кипения, чем остальные компоненты воздуха, поэтому они накапливаются в жидком кислороде и выделяются из него методом низкотемпературной ректификации в сочетании с другими методами. После обогащения криптоновый концентрат представляет собой бинарную смесь криптон–ксенон, которая разделяется методом
56
низкотемпературной ректификации.
|
|
|
|
|
|
|
|
Таблица 4.1 |
|
|
Основные свойства веществ [4, 29] |
|
|
||||
|
|
|
|
|
|
|
|
|
|
Химическа |
|
Газовая |
Температур |
Критические |
Фактор |
||
Вещество |
я формула |
|
постоянна |
а кипения, |
параметры |
ацентричност |
||
|
|
я, |
К |
Ткр, K |
pкр, |
ρкр, |
и ω |
|
|
|
|
||||||
|
|
|
Дж/(кг·К) |
|
МПа |
3 |
|
|
|
|
|
|
|
кг/м |
|
||
Азот |
N2 |
|
296,8 |
77,36 |
126,2 |
|
|
0,04 |
|
|
|
|
|
|
3,39 |
313,1 |
|
|
|
|
|
|
|
8 |
|
|
Аргон |
Ar |
|
208,146 |
87,29 |
|
|
|
0,002 |
|
|
|
|
|
150,65 |
4,86 |
531,0 |
|
|
|
|
|
|
|
4 |
|
|
Кислоро |
O2 |
|
259,835 |
90,19 |
|
|
|
0,0213 |
д |
|
|
|
|
154,58 |
5,10 |
436,2 |
|
|
|
|
|
|
1 |
7 |
|
|
Пара- |
p-H2 |
|
4124,2 |
20,39 |
|
|
|
0,2491 |
водород |
|
|
|
|
32,984 |
1,28 |
31,43 |
|
|
|
|
|
|
|
7 |
|
|
Пара- |
p-D2 |
|
2063,0 |
23,57 |
|
|
|
0,238 |
дейтери |
|
|
|
|
38,34 |
1,61 |
20,39 |
|
й |
|
|
|
|
|
|
|
|
Криптон |
Kr |
|
99,215 |
111,7 |
|
|
|
0,002 |
|
|
|
|
|
209,40 |
5,49 |
912,0 |
|
Ксенон |
Xe |
|
63,322 |
165,05 |
|
|
|
0,002 |
|
|
|
|
|
289,74 |
5,82 |
1110, |
|
|
|
|
|
|
|
|
0 |
|
Неон |
Ne |
|
411,94 |
27,17 |
|
|
|
0,0388 |
|
|
|
|
|
44,45 |
2,72 |
484,0 |
|
|
|
|
|
|
|
1 |
|
|
Оксид |
CO |
|
297,0 |
81,63 |
|
|
|
0,049 |
углерода |
|
|
|
|
132,92 |
3,49 |
301,8 |
|
|
|
|
|
|
|
6 |
6 |
|
Диоксид |
CO2 |
|
188,9 |
194,7 |
304,2 |
|
|
0,225 |
углерода |
|
|
|
|
|
7,37 |
468,1 |
|
|
|
|
|
|
|
6 |
9 |
|
Метан |
CH4 |
|
518,3 |
111,7 |
190,6 |
4,6 |
|
0,0104 |
|
|
|
|
|
|
|
162,0 |
|
|
|
|
|
|
|
|
2 |
|
Этан |
C2H6 |
|
276,5 |
161,3 |
305,4 |
|
|
0,098 |
|
|
|
|
|
|
4,88 |
203,1 |
|
|
|
|
|
|
|
3 |
8 |
|
57
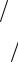
Бинарные и тройные смеси, состоящие из основных компонентов воздуха, в той или иной степени отклоняются от свойств идеальных газовых смесей и растворов, поэтому данные об их равновесных параметрах определяют в результате экспериментальных исследований. При обобщении опытных данных часто используют промежуточные функции γi, Ki [см. уравнения (4.6) и (4.7)], с помощью которых получают выражения, применяемые при расчетах на ЭВМ.
Для удобства обозначения состава бинарных и тройных смесей, состоящих из компонентов воздуха, принимаем, что индекс 1 относится к N2, 2 – к Аг, 3 – к O2, 4 – к Kr и 5 – к Хе.
4.2.1. Интерполяционные уравнения расчета равновесия тройной смеси азот–аргон–кислород
В работах [8, 13, 30] содержится обширная информация по равновесию системы азот–аргон–кислород, которая обобщена в виде интерполяционного уравнения для расчета фазового равновесия.
Однако более удобное обобщение данных по фазовому равновесию предложено В.С. Кортиковым и В.С. Суриной, которое приводится в работе [31]. При этом концентрацию в паре и жидкости тройной системы азот–аргон–кислород определяют по следующим выражениям:
yi = |
αi3xi |
; xi = |
yi |
αi3 |
, |
(4.10) |
3 |
3 |
|
||||
|
∑αi3xi |
|
∑yi αi3 |
|
|
|
|
i =1 |
|
i =1 |
|
|
|
где αi3 – относительная летучесть i-го компонента в кислороде. |
|
|||||
Для азота |
|
|
|
|
|
|
α13 = exp{2,3026[A13x3 + A31x1 + (A12 + A32 )x2 + 6B13 x1x3 + |
|
|||||
+ x1x2 (3B12 + B13 + B23 )+ x2 x3 (3B23 + B12 + B13 )]}; |
(4.11) |
|||||
для аргона
58
α23 = exp{2,3026[A23x3 + A32 x2 + (A31 − A21 )x1 + 6B23x2 x3 + |
|
+ x1x2 (− 3B12 + B13 + B23 )+ x1x3 (3B13 − B12 + B23 )]}, |
(4.12) |
где
A13 = 1,1494 – 0,2696 lgp; |
A31 = 0,8458 |
– 0,0673 lgp – 0,0369 lgp2; |
||
A12 = 0,9406 – 0,2194 lgp; |
A32 = 0,1186 |
– 0,0347 lgp; |
||
B13 |
= 0,0518 |
– 0,015 lgp; |
B12 = 0,0360 – 0,0102 lgp; |
|
B23 |
= 0,0046 |
– 0,0011 lgp; |
A23 = 0,3938 – 0,0957 lgp; |
|
A = 0,4777 + 0,0479 lgp – 0,0432 lgp2; |
p – давление смеси, кПа. |
|||
21 |
|
|
|
|
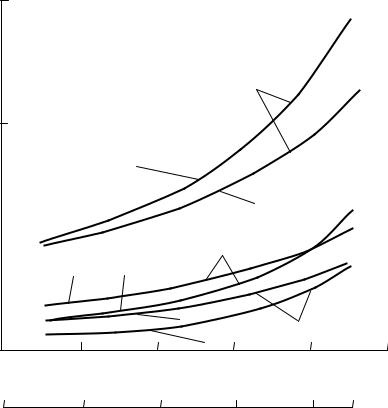
Свойства разделяемой смеси, наряду с другими параметрами, определяются закономерностью изменения фазового равновесия и коэффициентов разделения соответствующих бинарных систем. Константы фазового равновесия компонентов рассматриваемой тройной смеси азот–аргон–кислород изменяются по нелинейному закону (рис. 4.1).
59
Ki
|
|
|
K1 |
|
|
20 |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
3′ |
|
|
|
|
K2 |
|
|
|
2′ |
2 |
|
|
|
|
|
1′ |
|
K3 |
|
0,2 |
|
|
1 |
|
|
0 |
0,2 |
0,4 |
0,6 |
0,8 |
1,0 |
|
|
|
|
x3, моль/моль |
|
0,9 |
0,7 |
0,5 |
0,3 |
0,1 |
0 |
|
|
|
|
x1, моль/моль |
|
Рис. 4.1. Изменение констант фазового равновесия компонентов смеси азот–аргон–кислород при x2 = 0,1 моль/моль:
1, 2, 3 – при p = 150 кПа; 1', 2', 3' – при р = 600 кПа
Наибольшие значения Ki (кривая 1) принадлежат легкокипящему азоту. Вместе с тем константы фазового равновесия компонентов системы азот–аргон–кислород имеют сложную зависимость от давления. Так, если при увеличении давления значения констант K3 и K2 увеличиваются, то K1 уменьшается. В рассмотренном диапазоне изменения концентраций и давлений коэффициенты разделения соответствующих бинарных смесей меняются незначительно. Например, при p = 150 кПа, x2 = 0,10 моль/моль и варьировании x1 от 0,05 до 0,90 моль/моль α12
изменяется от 2,391 до 2,163; α13 – от 3,438 до 3,245; α23 – от 1,438 до
1,500, а при р = 600 кПа при тех же значениях концентрации компонентов α12 изменяется от 1,926 до 1,922; α13 – от 2,348 до 2,563;
60

α23 – от 1,217 до 1,333.
4.2.2. Расчет фазового равновесия смесей кислород–криптон и криптон–ксенон
Криптон и ксенон являются наименее летучими компонентами воздуха, и температура кипения при стандартном давлении у криптона почти на 30 К, а у ксенона на 70 К выше температуры кипения кислорода. В связи с этим они накапливаются в жидком кислороде и представляют собой смесь кислород–(криптон + ксенон), относящуюся к разбавленным растворам, поскольку их суммарная объемная доля составляет 5·10–6.
Для расчета процесса ректификации на первом этапе выделения Kr и Xe важно знать зависимость для области малых содержаний примесей от исходной до 0,0001…0,001 объемной доли
Kr.
При расчете параметров фазового равновесия рассматриваемую смесь условно представляют бинарной (кислород– криптон), тогда концентрация криптона в паре
y4 = K4 x4. |
(4.13) |
Сопоставление и обобщение опытных данных [32, 33] по фазовому равновесию смеси (3–4)* в области малых концентраций позволяет представить зависимость константы K4 от давления в виде
K4 = |
1 |
|
, |
(4.14) |
||
|
|
|
||||
4,202 − 4,730lg p |
||||||
|
|
|
||||
а от температуры – в виде |
|
|
|
|
|
|
K4 = |
1 |
|
, |
(4.15) |
||
|
|
|
||||
|
25,308 − 0,1824T |
|||||
|
|
|
|
|||
где р – давление, МПа; Т – температура, К.
Для расчета параметров фазового равновесия смеси кислород– криптон используем подпрограмму, текст которой на
* Здесь и далее даны обозначения соответствующих индексов компонентов смесей.
61
