
РАМАЗАНОВА К.Р
..pdf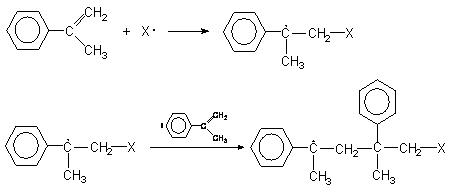
111
зольного кольца и двойной связи. Для α-метилстирола можно записать три резонансные структуры. Видно, что бензольное кольцо здесь имеет повышенную электронную плотность по сравнению с незамещённым бензолом. Соответственно винильный фрагмент молекулы α-метилстирола обеднён электронной плотностью по сравнению с обычной двойной связью. Эффект делокализации делает p-электроны двойной связи менее доступными для электрофилов. Напротив, p-орбиталь бензола становится более доступной для электрофилов.
α-метилстирол – ценнейший продукт в крупнотоннажной химии полимеров. Применяют его в качестве мономера при производстве синтетических каучуков, латексов, различных водостойких мастик.
α-метилстирол полимеризуется согласно анионному механизму, например, под действием амида натрия, бутиллития и другие.
При радикальной полимеризации α-метилстирол образует димеры и низкомолекулярные олигомеры, при низких температурах под действием катализаторов ионного характера (Na-нафталин, C4H9Li, эфираты BF3, калий и др. щелочные сплавы), радиационного либо УФ-облучения – гомополимеры довольно высокой молекулярной массы и различной стереорегулярности. Достаточно просто сополимеризуется со стиролом, бутадиеном, акрилонитрилом и другими ненасыщенными мономерами.
(4.7)
Употребляют α-метилстирол как сомономер в производстве сополимера со стиролом (САМ), определенных видов АБС-пластиков, обладающих более высокой теплоустойчивостью, чем полистирол, и бутадиен-стирольные каучуки.
Полимер α-метилстирола употребляют для совмещения с ПВХ и дргими полимерами с целью повышения их теплостойкости. Полиметилстирол, получаемый таковыми способами, используется для производства предметов широкого потребления, игрушек, упаковочных материалов и других целей.
α-Метилстирол получают синтетическим способом [1а], а также из побочного продукта при производстве фенола и ацетона – диметилфенилкарбинола [1а, 32, 33, 36] и именно этой проблеме посвящается раздел диссертации.
Альтернативой гомогенному катализатору серной кислоте с льюисовской кислотностью разложения ГПК на фенол и ацетон с точки зрения активности и селективности, экологической безопасности, лёгкости разделения продуктов реакции и простоты регенерации являются твёрдые катализаторы с бренстедовской кислотностью [1а, 134, 135, 140, 142-144]. Среди твёрдых катализаторов наиболее эффективными являются гетерополикислоты и цезий-замещённые гетерополикислоты с полианионом Кеггина, которые обладают чисто бренстедовской кислотностью и высокой
112
термостабильностью и относятся к новому поколению так называемых «зелёных» катализаторов [142-144]. Высокая эффективность гетерополикислот как катализаторов обусловлена их сильной бренстедовской кислотностью, превышающей кислотность минеральных кислот и традиционных твёрдых катализаторов. Это даёт возможность проводить каталитический процесс при более низкой концентрации катализатора и/или более низкой температуре, что способствует повышению селективности процесса. Кроме того, благодаря инертности полианиона Кеггина гетерополикислоты не вступают в побочные реакции с органическими реагентами, что характерно для обычных минеральных кислот, в частности, серной кислоты. Например, додеканвольфрамофосфорная кислота Н3РW12О40 обладает наивысшей бренстедовской кислотностью, выше, чем 100 %-ная серная кислота. Среди солей цезийзамещенной гетерополикислоты (Сs)mН3-mРW12О40 (0 ≤ m ≤3) чрезвычайно высокой каталитической активностью и селективностью с кристаллической структурой полианиона Кеггина обладает Сs2.5Н0. 5РW12О40 (Сs2.5 с числом атомов цезия N=2,5) [142144]. Каталитическая активность Сs2.5 более чем в 10 раз превышает активность цеолитов и в 3 раза выше активности исходной гетерополикислоты. Высокая активность Сs2.5 обусловлена высокой поверхностной бренстедовской кислотностью благодаря большой площади поверхности 150-200 м2/г. Поверхность Сs2.5 является гидрофобной, не растворяется в жидкостях любого типа. Гетерополикислоты и их соединения с металлами используются в качестве гомогенных и гетерогенных (массивных и нанесённых) катализаторов. Гетерогенные катализаторы обладают высокой каталитической активностью в низкотемпературных реакциях. Для практических целей используют твёрдые гетерогенные катализаторы на инертных носителях с неповреждённой структурой полианиона Кеггина, полученные путём пропитки (20-50) масс.% гетерополикислотой или нанесением Сs2.5 по специальной методике [35-38]. В качестве пористых инертных носителей применяют глину К-10, мезопористый диоксид кремния МСМ-41 и др. и получают, например, катализаторы с формулой 20
масс.% Н3РW12О40 ⁄МСМ-41 или 20 масс.% Сs2. 5Н0. 5РW12О40 ⁄МСМ-41. В работах [142-144] подробно изучены первичная (анион Кеггина), вторичная и третичная
структуры названных катализаторов комплексом физических и химических методов, а также кинетика разложения ГПК при Т = 30-50°С в среде кумола.
Данный раздел посвящён синтезу гетерогенных катализаторов Н3РW12О40 (Н3)
и её цезий-замещёной соли Сs2.5Н0.5РW12О40 (Сs2.5) на основе МСМ-41 [142-144] и исследованию процесса разложения модельных образцов ГПК и ДМФК, их смесей и
технического ГПК, а также созданию экспериментальной установки каталитической дистилляции синтеза поликонденсационных мономеров (фенола и ацетона) и α- метилстирола разложением технического ГПК с использованием синтезированных гетерогенных катализаторов [211а-213а, 222а, 225а-228а].
4.3.1. Синтез гетерогенных катализаторов
Синтезы гетерогенных катализаторов Н3РW12О40 и её цезий-замещённой соли
Сs2.5Н0.5РW12О40 на основе МСМ-41 проведены по методикам и рекомендациям, изложенные в работах [142-144].
Подготовка носителя. В качестве носителя выбран мезопористый диоксид кремния марки МСМ-41 с размерами гранул 3-5 мм с диаметром пор 82 А° и площадью поверхности 320 м2/г, полученных после растирания гранул размером 10-15 мм с
113
последующим просеиванием. Предварительно носитель МСМ-41 была обработана азотной кислотой (1 моль) (10 мл раствора на 1 г диоксида кремния) при перемешивании в течение 15 мин при Т = 80°С с промывкой водой и ускоренной осушкой под вакуумом при 110°С и последующей кальцинацией при Т = 300°С в течение 3 ч.
При синтезе гетерогенных катализаторов использовали гетерополикислоту Н3РW12О40•nН2О с физико-химическими показателями согласно нормам и требованиям ТУ 6-09-01-744-88 (марка х.ч.) и карбонат цезия согласно ТУ 6-09-638-80. В кристаллогидрате Н3РW12О40• nН2О определяли число молекул кристаллизационной воды гравиметрическим методом при нагревании навески кислоты в течение 1 час. при Т = 220°С, число молекул n кристаллизационной воды в гетерополикислоте вычисляли по формуле:
n= 2880,17•mВ/[mК- mВ ]•18,01, |
(4.42) |
где 2280,17 и 18,01 – молекулярные массы гетерополикислоты и воды; mК – навеска гетерополикислоты; mВ – масса воды в граммах по гравиметрии.
Установлено, что в зависимости от партии гетерополикислоты число молекул воды находилось в пределах n = 5-13. Количество кристаллизационной воды учитывали при пропитке диоксида кремния МСМ-41 гетерополикислотой Н3РW12О40•nН2О и синтезе цезий-замещённой соли.
Готовили раствор из расчёта 0,1 г гетерополикислоты в 1 мл бутаноле-1. После пропитки диоксида кремния при перемешивании в течение 30 мин и снятия излишней жидкости влажный осадок сушили при Т = 110°С в течение суток и затем кальцинировали при Т = 300°С в течение 3 ч. В полученном катализаторе определяли содержание гетерополикислоты. Полученный катализатор пропитывали следующей порцией свежеприготовленного раствора гетерополикислоты в бутаноле-1, добивались содержания 10, 20 и 50% гетерополикислоты в мезопористом диоксиде кремния и получали соответствующие гетерогенные катализаторы.
Образование цезий-замещённой соли Сs2.5Н0.5РW12О40 в мезопорах диоксида кремния МСМ-41 в результате реакции между гетерополикислотой и карбонатом цезия контролировали количественно по схеме
2,5Сs2СО3 + 2Н3РW12О40•nН2О → 2Сs2.5Н0.5РW12О40 + 2,5СО2↑ + (2,5+2n)Н2О, |
(4.18) |
где n=5-13 количество кристаллизационной воды учитывали при пропитке диоксида кремния гетерополикислотой из раствора в бутаноле.
Расчёты количества mС в граммах Сs2СО3 и mК в граммах Н3РW12О40•nН2О для получения количества m в граммах Сs2.5Н0.5РW12О40 в мезопорах МСМ-41 с массой
mН в граммах или с содержанием m=10 и 20 масс.% Сs2.5Н0.5РW12О40 на МСМ-41 проводили по выше приведённой реакции по формулам:
M (%) = 100• m/( m+ mН); |
(4.43) |
mC = 1,25•m• M1/M3; mK= m• M2/M3,
где M3, M2 и M1 – молекулярные массы Сs2.5Н0.5РW12О40, Н3РW12О40•nН2О и Сs2СО3. Получение гетерогенного катализатора с m = 10 или 20 масс.% содержанием
цезий-замещённой соли Сs2.5Н0.5РW12О40 на мезопорах носителя МСМ-41 проводили в два этапа. Сначала МСМ-41 пропитывали последовательно водным раствором кар-
114
боната цезия из расчёта 0,1 карбоната цезия в 1 мл воды до содержания mC карбоната цезия в МСМ-41 при перемешивании в течение 30 мин. После пропитки МСМ-41 при перемешивании в течение 30 мин и снятия излишней жидкости влажный осадок сушили при Т = 110°С в течение суток и каждый раз методом гравиметрии контролировали количество пропитанного карбоната цезия. На втором этапе проводили пропитку МСМ-41 и добивались пропитки необходимого расчётного количества mК Н3РW12О40•nН2О из раствора в бутаноле-1, как описано выше при получении гетерогенных катализаторов на МСМ-41 с различным содержанием гетерополикислоты. Каждый раз после пропитки и сушки методом гравиметрии контролировали пропитанное количество гетерополикислоты. Затем синтезированные гетерогенные катализаторы кальцинировали при Т = 300°С в течение 3 ч для протекания до конца реакции синтеза Сs2.5Н0.5РW12О40 путём взаимодействия гетерополикислоты и карбоната цезия в мезопорах МСМ-41. Полученные гетерогенные катализаторы промывали ацетоном марки ч.д.а. и сушили при температуре 100°С в течение 1 ч. В синтезированных гетерогенных катализаторах (табл. 4.4) контролировали содержание гетерополикислоты химическим и цезия (Сs, масс.%) атомно-адсорбционным методом, где число атомов цезия N (0 ≤ N≤3) в цезий – замещённой соли СsNН3-NРW12О40 в гетерогенном катализаторе вычисляли по экспериментально установленной аппроксимационной формуле:
N = 0,267• (Сs – 1). |
(4.44) |
В табл. 4.4 приведены экспериментально установленные структурные характеристики синтезированных гетерогенных катализаторов, которые согласуются с литературными данными [142-144].
Таблица 4.4 Структурные характеристики синтезированных гетерогенных катализаторов
Синтезированный гетерогенный |
Средний диаметр |
Площадь |
||
катализатор |
пор, нм |
поверхности, м2/г |
||
10% Н3РW12О40/ МСМ-41 |
7,2 |
230 |
||
20% Н3РW12О40 |
/МСМ-41 |
5,8 |
207 |
|
50% Н3РW12О40 |
/МСМ-41 |
5,8 |
195 |
|
10% Cs2.5Н0.5РW12О40 |
/МСМ-41 |
5,2 |
210 |
|
20% Cs2.5Н0.5РW12О40 |
/МСМ-41 |
6,1 |
250 |
|
|
|
|
|
|
4.3.2. Синтез фенола, ацетона и α-метилстирола на гетерогенных катализаторах разложением модельных образцов гидропероксида кумола и диметилфенилкарбинола,
их смесей и технического гидропероксида кумола
Данный раздел посвящён исследованию активности и селективности синтезированных гетерогенных катализаторов (табл. 4.4) и кинетики процесса разложения отдельно модельных или стандартных образцов ГПК на фенол и ацетон и ДМФК на АМС, смеси модельных ГПК и ДМФК, а также технического ГПК, содержащего до 7 масс.% ДМФК [211а-213а,222а,225а-228а]. В качестве модельного образца ДМФК выбран стандарт фирмы Lancaster с содержанием основного вещества более 98
115
масс.% (табл. 2.3, раздел 2.2), а ГПК с содержанием основного вещества 99 масс.% полученный по методике [27].
Исследования нами проведены на лабораторной установке, которая состояла из колбы с обратным холодильником и термометром. Разложения модельных образцов ГПК и ДМФК, их смеси и технического ГПК проводили в ацетоне при температуре кипения Ткип. = 56°С или изотермических условиях. Установлено, что при температуре кипения ацетона все синтезированные катализаторы (табл. 4.4) инертны к ацетону, к примесям до 1 масс.% АЦФ и 3 масс.% кумола в ацетоне, и по данным газохроматографического анализа, не образуется каких-либо новых химических соединений. При скорости перемешивания 400 об/мин гетерогенного катализатора в количестве 10 мл на 100 мл ацетона при температуре его кипения вводили 4 г исследуемого модельного образца ГПК или ДМФК или 4 г их смеси модельных образцов (ГПК 93 масс.% +7 масс.% ДМФК) или 4 г промышленного образца технического ГПК. При этом через определённое время τ (мин) отбирали пробу для анализа реакционной массы разложения на компонентный состав. При этом по данным газохроматографического анализа рассчитывали конверсию X* (%) исходных и образованных продуктов реакции при фиксированном времени τ (мин), отнесённую к 4 г исследуемого образца.
На рис. 4.7-4.9 приведены результаты исследования в среде ацетона при изотермических условиях зависимости конверсии от времени X*(τ) (кинетика) модельных образцов ГПК и ДМФК, смеси этих образцов и технического ГПК при их разложении и образования при этом фенола и α-метилстирола на синтезированных гетерогенных катализаторах (табл. 4.4).
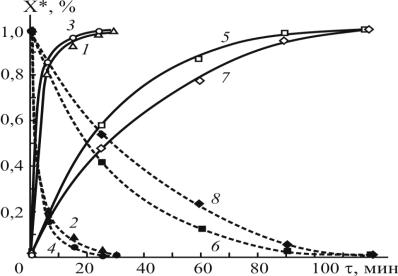
Рис. 4.7. Кинетика конверсии модельных образцов ГПК (2, 4) в фенол (1, 3) и ДМФК (6, 8) в α - метилстирол (5, 7) в ацетоне при изотермических условиях на гетерогенных катали-
заторах, где 1, 2, 7, 8 – 10, 20 масс.% Н3РW12О40/МСМ-41 и 10 масс.% Cs2.5Н0.5РW12О40/МСМ-41; 3-6 – 50% Н3РW12О40/МСМ-41 и 20 масс.%
Cs2.5Н0.5РW12О40/МСМ-41
116
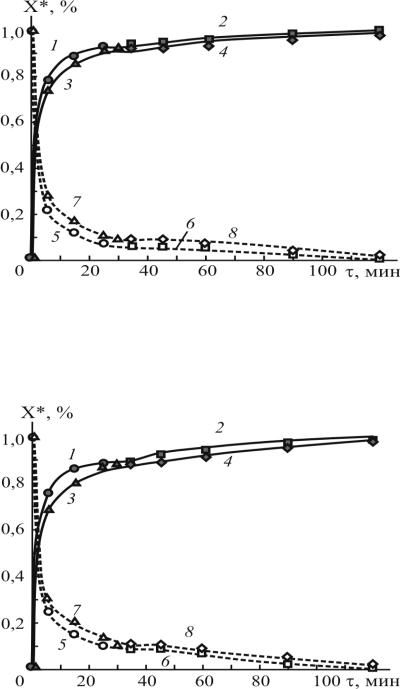
Рис. 4.8. Кинетика конверсии смеси (93 масс.% ГПК+7 масс.% ДМФК) модельных образцов ГПК (5, 7) в фенол (1, 3) и ДМФК (6, 8) в α-метилстирол (2, 4) в ацетоне при изотермических условиях на гетерогенных катализаторах, где 3, 4, 7, 8 – 10, 20 масс.%
Н3РW12О40/МСМ-41 и 10 масс.% Cs2.5Н0.5РW12О40/МСМ-41; 1, 2, 5, 6 – 50 масс.% Н3РW12О40/МСМ-41 и 20 масс. % Cs2.5Н0.5РW12О40/МСМ-41
Рис. 4.9. Кинетика конверсии технического гидропероксид кумола (89 масс.% гидропероксид кумола, 7 масс.% диметилфенилкарбинола, остальное примеси ацетофенона и кумола) (5-8) в фенол (1, 3) и ацетон, α-метилстирол (2, 4) в среде ацетона при температуре его кипения на синтезированных гетерогенных катализаторах, где 3, 4, 7, 8 – 10-20 %
Н3РW12О40/ МСМ-41 и 10% Cs2.5Н0.5РW12О40 /МСМ-41; 1, 2, 5, 6 – 50% Н3РW12О40 /МСМ41 и 20% Cs2.5Н0.5РW12О40 /МСМ-41
Модельный образец ГПК (рис. 4.7, кр. 2 и 4) со 100 %-ой конверсией и 100 %- ой селективностью разлагается на фенол (кр. 1 и 3) и ацетон, а модельный образец ДМФК (кр. 6 и 8) со 100 %-ной конверсией и 100 %-ной селективностью разлагается на α-метилстирол (5 и 7) на синтезированных гетерогенных катализаторах (табл. 4.4). При этом самую высокую и одинаковую активность при разложении ГПК и ДМФК проявляют гетерогенные катализаторы 50% Н3РW12О40/МСМ-41 и 20%
117
Cs2.5Н0.5РW12О40/МСМ-41 (рис. 4.7, кр. 3-6; табл. 4.4), так эти катализаторы через 60 мин разлагают ДМФК на 90 % (кр. 6), через 5 мин разлагают ГПК на 85 % и время
100%-ного разложения для ГПК составляет 25 мин (кр. 4), в отличие 30 мин для ка-
тализаторов 10-20 % Н3РW12О40/ МСМ-41 и 10% Cs2.5Н0.5РW12О40/МСМ-41 (кр. 2). Вместе с тем все синтезированные гетерогенные катализаторы (табл. 4.4) разлагают
на 100 % ДМФК через 120 мин (рис. 4.7, кр. 6 и 8).
Смесь модельных образцов ГПК и ДМФК. Промышленный образец техниче-
ского ГПК. На рис. 4.8 приведены кинетические кривые X*(τ) разложения смеси модельных образцов, содержащие 93 масс.% ГПК+7 масс.% ДМФК, а на рис. 4.9 технического ГПК с содержанием 89 масс.% ГПК, 7 масс.% ДМФК, 3 масс.% кумола и 1 масс.% АЦФ на синтезированных гетерогенных катализаторах (табл. 4.4). Исследование именно такой модельной смеси ГПК+ДМФК продиктовано тем, что в промышленных образцах технического ГПК содержание ДМФК не превышает 7 масс.% [1,20]. Сравнения кинетических кривых разложения смеси модельных образцов ГПК+ДМФК (рис. 4.8, кр. 5-8) и технического ГПК (рис. 4.9, кр. 5-8), а также образования фенола (рис. 4.8 и 4.9, кр. 1 и 3) и α-метилстирола (рис. 4.8 и 4.9, кр. 2 и 4) показывают, что их поведения имеют почти одинаковый характер.
Газохроматографическим методом анализа РМР установлено, что на всех гетерогенных катализаторах (табл. 4.4) модельная смесь ГПК+ДМФК (рис. 4.8) и технический ГПК разлагается в две стадии. На первой стадии в течение 25-30 мин происходит разложение ГПК (рис. 4.8 и 4.9, кр. 5 и 7) со 100 %-ной селективностью и 100 %-ной конверсией на фенол (кр. 1 и 3), а на второй стадии ДМФК со 100 %-ной селективностью и 100 %-ой конверсией на α-метилстирол (кр. 2 и 4). Причём, содержащиеся в промышленном образце технического ГПК (рис. 4.9) примеси 3 масс.% кумола и 1 масс.% АЦФ не влияют на процесс его двухстадийного разложения и конверсию, и селективность синтезированных гетерогенных катализаторов (рис. 4.9).
При этом, как и в случае разложения модельных образцов ГПК и ДМФК (рис. 4.7, кр. 3-6), наибольшую активность проявляют гетерогенные катализаторы 50
масс.% Н3РW12О40/МСМ-41 и 20 масс.% Cs2.5Н0.5РW12О40/МСМ-41 (рис. 4.8 и 4.9, кр.
1, 2, 5, 6).
Различная реакционная способность пероксидной группы в ГПК и гидроксильной группы в ДМФК обуславливает различные значения максимального значения времени 25-30 мин. 100 %-ной конверсий ГПК в фенол и 120 мин 100 %-ной конверсий ДМФК в α-метилстирол со 100 %-ной селективностью на гетерогенных катализаторах и различный характер кинетических кривых X*(τ) (рис. 4.7-4.9, кр. 1- 8). Вместе с тем, общим является химизм процесса количественного разложения модельных образцов ГПК и ДМФК, их в модельной смеси или техническом ГПК со 100%-ной селективностью только на фенол, ацетон и α-метилстирол на гетерогенных катализаторах (табл. 4.4).
C6H5C(CH3)2OOH → C6H5OH + CH3COCH3, |
(4.9) |
C6H5C(CH3)2OH → C6H5C(CH3)CH2 + H2O |
(4.10) |
Полученные результаты исследования (рис. 4.7-4.9) использованы нами для создания экспериментальной установки каталитической дистилляции синтеза фенола, ацетона и α-метилстирола разложением технического ГПК на синтезированных
118
гетерогенных катализаторах. Обозначим через τ* время контакта или время пребывания технического ГПК, содержащего ДМФК, в слое катализатора. При непрерывном режиме разложения время пребывания ГПК для 100 %-ной конверсии в слое гетерогенного катализатора должно быть не менее τ*>30 мин (рис. 4.7, кр. 2 и 4; рис. 4.8 и 4.9, кр. 5 и 7), а время контакта ДМФК для 100%-ной конверсии в слое гетерогенного катализатора или время пребывания технического ГПК должно быть не менее τ* > 120 мин (рис. 4.7-4.9, кр. 6 и 8). Причём, для организации двухступенчатого процесса разложения технического ГПК, оптимальным является наличие двух реакторов или реакционно-ректификационных колонн со слоем гетерогенного катализатора (таблица 4.4) или один реактор для разложения ГПК и отдельно для дегидратации ДМФК. Различие времени пребывания ГПК и ДМФК для их 100 %-ной конверсии в составе технического ГПК при объёме слоя гетерогенного катализатора 100 мл в каждом реакторе скорость подачи технического ГПК должна быть не менее 100 мл/час. При этом общее время пребывания технического ГПК в двух реакторах составляет τ* > 200 мл/100 мл/ч >120 мин. Диаметр реакторов 2•R0 и высоту h слоя гетерогенного катализатора выбрали, исходя из математической модели каталитического реактора (разд. 4.1, рис. 4.1) или фактически реконструирована установка КДК (рис. 4.3). Отличием является то, что задействованы две первые колонны 1 и 2 (рис. 4.3) для работы при атмосферном давлении с высотой слоя синтезированных гетерогенных катализаторов 175 мм с h/2•R0 = 6,47 согласно условию 1≤ h/2R0 ≤10 оптимальной конструкции каталитического реактора (рис. 4.6, раздел 4.1).
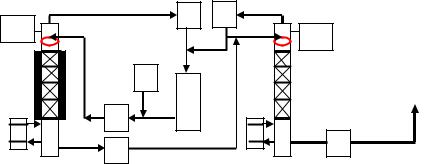
Блок-схема установка двухстадийного разложения технического ГПК, приведённая на рис. 4.10, состоит из реакционно-ректификационных колонн 1 и 2, загруженных гетерогенными катализаторами, расположенными над кубовой частью колонн, имеющих входы, расположенные над слоем катализатора, и верхний и нижний выходы. Реакционно-ректификационная колонна 1 предназначена для получения фенола и ацетона разложением ГПК технического ГПК со 100%-ной конверсией и 100%-ной селективностью исключительно на фенол и ацетон в слое гетерогенного катализатора при температуре кипения ацетона 56°С каталитической дистилляцией фенола и ацетона в непрерывном изотермическом режиме, а реакционноректификационная колонна 2 предназначена для получения путём дегидратации ДМФК со 100%-ной конверсией в слое гетерогенного катализатора при температуре кипения ацетона 56°С каталитической дистилляцией α-метилстирола в непрерывном изотермическом режиме.
Верхний выход колонны 1 соединён через дефлегматор 3 с входом сборника 5, выход которого через насос 7 соединён с входом колонны 1. Устройство подачи технического ГПК в ацетоне на вход колонны 1 подробно описано в патенте [228а], отметим, что в трубопроводе между сборником 5 и насосом 7 смонтирован патрубок 6 подачи технического ГПК в ацетоне из калиброванной мерной бюретки. Нижний выход кубовой части колонны 1 через насос 8 соединён с входом колонны 2, верхний выход которого через дефлегматор 4 соединён с входом колонны 2 и входом сборника 5. Нижний выход кубовой части колонны 2 соединён с насосом 9. В верхней части колонн 1 и 2 над слоем катализатора смонтированы термопары 10 и 11. Катализаторная секция колонны 1 снабжена рубашкой охлаждения. Колонны 1 и 2 снабжены устройствами замера уровня кубовой жидкости (а, рис. 4.10).
119
10 |
|
|
3 |
4 |
|
|
|
|
|
|
11 |
Реакционная масса разложения: |
|
|
|
|
|
|
||
|
|
|
|
|
|
фенол, ацетон, α-метилстирол, |
|
|
6 |
|
|
|
кумол, ацетофенон |
|
|
|
|
|
|
на ректификацию |
а |
|
7 |
5 |
а |
2 |
|
1 |
|
|
9 |
|||
|
8 |
|
|
|
||
|
|
|
|
|
||
|
|
|
|
|
|
Рис. 4.10. Блок-схема экспериментальной установки (конструкции реакторов на рис. 4.6) непрерывного процесса каталитической дистилляции фенола, ацетона и α-метилстирола разложением технического гидропероксида кумола, содержащего диметилфенилкарбинол на синтезированных гетерогенных катализаторах типа Н3РW12О40/МСМ-41 и
Cs2.5Н0.5РW12О40/МСМ-41 (Патент РФ № 2442769, 01.10.2010): 1 и 2 – реакционноректификационные колонны с гетерогенным катализатором; 3 и 4 – дефлегматоры; 5 –
сборник ацетона; 6 – устройство подачи технического ГПК и а – замера уровня кубовой жидкости; 7- 9 – насосы; 10 и 11 – термопары.
Устройство замера уровня кубовой жидкости представляет собой толстостенную стеклянную трубку с контрольными метками минимально и максимально допустимого уровня кубовой жидкости, смонтированной с внешней стороны кубовой части колонны и выполненной сообщающейся с полостью кубовой части колонны. В колоннах 1 и 2 уровень кубовой жидкости не должен достигать слоя катализатора и находиться в пределах минимально и максимально допустимого уровня. Колонны 1 или 2 имеют одинаковый размер и представляют собой вертикальную металлическую трубу высотой 480 мм и внутренним диаметром 27 мм, с торцевых сторон которой смонтированы фланцы с отверстиями для крепёжных болтов (рис. 4.6). Полезный объём колонны 275 см3 . Внутри трубы на высоте 200 мм смонтировано опорное металлическое кольцо перпендикулярно продольной оси трубы с металлической сеткой, удерживающей слой катализатора, у которой размер ячеек 1мм. На металлической сетке опорного металлического кольца размещён слой гетерогенного катализатора (таблица 4.4) в количестве 100 мл. Высота слоя катализатора составила 175 мм. Над слоем катализатора также установлена металлическая сетка с размерами ячеек 1 мм, которая предотвращает унос катализатора и обеспечивает равномерное распределение потока жидкости. Вход ректификационной колонны расположен на высоте 40 мм, термопара смонтирована на высоте 70 мм от верхней металлической сетки слоя катализатора. Нижняя и верхняя крышки колонны выполнены в виде «глухих» фланцев с соответствующими выходами в виде штуцеров с резьбой. Фланцы крышек и трубы имеют выступы и зазоры типа «папа-мама», обеспечивающие герметичность соединяемых элементов. Крышки и труба дополнительно уплотнены прокладкой и через фланцевые соединения стянуты болтами с гайкой. Секция с катализаторным слоем колонны 1 снабжена водяной рубашкой охлаждения.
Кубовая часть колонны 1 или 2 снабжена электронагревателем в виде спирали из вольфрама, который регулирует температуру кубовой части колонны изменением
120
напряжения тока. Поэтому через регулятор напряжения задаётся требуемое тепло, которое необходимо для обеспечения температуры насыщенных паров ацетона 56°С в верхней части колонн 1 и 2 по термопарам 10 и 11. Для сохранения теплового баланса в колонне 1 из-за теплового эффекта экзотермической реакции разложения ГПК регулируют подачу тепла на электронагреватель в сторону уменьшения напряжения тока и, при необходимости, регулируют подачу воды в рубашку реакционной секции колонны 1. Сигналы с термопар 10 и 11 по двум каналам преобразуются и в виде температуры регистрируются потенциометром в реальном режиме времени. Дефлегматоры 3 и 4 имеют одинаковый размер и предназначены для охлаждения насыщенных паров ацетона и представляют собой изделие «труба в трубе» с размером внутренней трубы: длина 500 мм, диаметр 50 мм. Материалы колонн, дефлегматоров и их элементов, трубопроводов представляют собой сталь марки 12Х18Н10Т. Сборник 5 ацетона представляет собой стеклянную ёмкость объёмом 10 л с пластмассовой крышкой с отверстиями для ввода ацетона с колонн 1 и 2 и выхода паров, а также с нижним краном слива лишнего ацетона или для подачи во всасывающий трубопровод насоса 7. Для подачи ацетонового раствора технического ГПК служит калиброванная мерная бюретка. Насосы 7-9 представляют собой дозировочные насосы марки НД2М 1,6/100КВ с взрывозащищённым исполнением. Максимальная скорость подачи 1,6 л/ч, давление 16 кгс/см2, материал проточной части 12Х18Н10Т. Для исключения потерь тепла колонны и все трубопроводы изолированы асбестом и асбестовым шнуром на силикате натрия.
Технологический процесс на установке каталитической дистилляции (рис. 4.10) осуществляют по безотходной технологии в непрерывном изотермическом режиме при температуре кипения ацетона. Основные параметры работы экспериментальной установки:
-температура насыщенных паров ацетона 56°С, которую контролируют с помощью термопар 10 и 11, или температура кипения ацетона;
-уровни кубовых жидкостей колонн 1 и 2 в пределах минимально и максимально допустимых уровней, которые отслеживают по контрольным меткам;
-постоянная скорость подачи 300 мл/ч ацетона или ацетонового раствора технического ГПК.
Пуск и вывод на режим установки осуществляют с использованием ацетона при подаче с ёмкости 5 насосом 7 на вход колонны 1 и далее в колонну 2. После выхода на режим установки по ацетону с калиброванной бюретки технический ГПК через патрубок 6 самотёком («гравитационно») поступает во всасывающий трубопровод насоса 7. Общая скорость подачи смеси ацетона и технического ГПК насосом 7,
постоянна 300 мл/ч при вариации соотношения объёма ацетона VА к объёму VТГ технического ГПК или VА:VТГ = (1-11)׃1 (табл. 4.5). Уменьшение объёмной доли технического ГПК в ацетоне нецелесообразно с практической точки зрения, поэтому в ка-
честве нижнего предела из интервала значений выбрано соотношение VА:VТГ=11׃1. Верхний предел VА:VТГ=2׃1, характеризующийся увеличенным содержанием технического ГПК, обусловлен экзотермическим эффектом реакции разложения ГПК на гетерогенном катализаторе при превышении указанного соотношения.
Таблица 4.5
Разложение технического ГПК состава 89 масс.% ГПК, 7 масс.% ДМФК,
