
133851261-119352752-Tehnica-farmaceutica
.pdf2.Emulgatorii se clasifică după structura chimică în:
-hidraţi de carbon (guma arabică, tragacanta, agar-agar);
-alcooli (colesterol, alcool cetilic, stearilic);
-esteri (compuşi sulfuraţi şi sulfonaţi, esteri ai propilenglicolului);
-compuşi cuaternari de amoniu (clorura de benzalconiu, bromura de cetilmetilamoniu) etc.
4.Corelarea structurii chimice cu cea fizică sistematizează emulgatorii în trei grupe:
-tensioactivii, care scad tensiunea la interfaţa lichid-lichid;
-coloizii hidrofili, care formează filme multimoleculare şi măresc vâscozitatea mediului, scăzând posibilitatea de contopire a picăturilor dispersate;
-substanţele solide fin pulverizate, ce se adsorb la interfaţa şi produce un strat rezistent în jurul picăturilor. Pulberi fine hidrofile ca argila, bentonita permit stabilizarea emulsiilor de tipul U/A şi pulberile hidrofobe (cărbune, grafit) pentru tipul A/U.
5.O deosebită importantă în formularea unei emulsii o prezintă calea de administrare, care grupează emulgatorii după acest criteriu în emulgatori:
-de uz intern (guma arabica, tragacanta, derivaţi de celuloză etc.);
-de uz extern (săpunuri alcaline, compuşi sulfonaţi, carbopoli, săpunuri inverse, spanuri, tweenuri).
În cazul emulsiilor administrate intern, trebuie să se cunoască cantitatea de emulgator care se poate utiliza în compoziţia unei emulsii pentru a nu provoca efecte secundare.
Emulgatorul, ca o a treia componentă a unei emulsii, cu rol în stabilizarea fazei disperse în mediul de dispersie, poate acţiona prin mai multe mecanisme. Emulgatorii care se orientează la interfaţa celor două lichide şi produc o reducere a tensiunii interfaciale cu formarea unei pelicule în jurul particulei fazei interne se numesc emulgatori adevăraţi sau propriu-zişi. În această grupa sunt incluse substanţele tensioactive (anionice, cationactive, neionogene şi amfotere).
Emulgatorii care contribuie la mărirea vâscozităţii fazei externe se numesc pseudoemulgatori sau emulgatori secundari.
Numeroase produse naturale acţionează ca agenţi de vâscozitate pentru soluţii apoase (guma arabică, tragacanta, agar-agar, pectina, alginaţii, derivaţii de celuloză, saponine, gelatina) sau uleioase (lecitina, ceara, lanolina).
Mecanismul de acţiune al emulgatorilor tensioactivi. Emulgatorii adevăraţi sunt substanţe caracterizate prin structura amfifilă polar-nepolar, cu afinitate atât pentru faza uleioasă, cât şi apoasă. Ele se orientează la interfaţa celor două lichide
221
nemiscibile, formează un film monomolecular, se dizolvă preferenţial în cele două faze distincte şi astfel determină o acţiune stabilizatoare, anulând tendinţa de coalescenţă, de lipire a picăturilor fazei dispersate. Substanţele tensioactive pot fi şi purtătoare de sarcini electrice care contribuie la stabilitatea emulsiei prin respingerile de natura electrostatică.
Grupările hidrofile din structura unui emulgator sunt solubile în apă şi cuprind următoarele grupe funcţionale: hidroxil, carboxil, sulfat şi sulfonat cu un cation monovalent, nitric, amino, duble legături de carbon, oxigen eteric etc. Grupările lipofile solubile în ulei, nepolare, sunt lanţuri de hidrocarburi, cicluri de atomi de carbon şi grupe carboxil cu cationi bivalenţi.
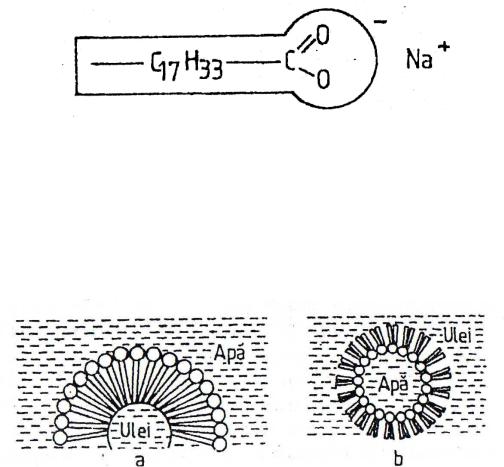
Substanţele tensioactive se caracterizează printr-o structură chimică amfifilă - o catenă hidrocarbonată, alungită, hidrofobă, care are la un capăt o grupare polară, redusă ca dimensiuni, dar care imprimă întregii molecule caracter hidrofil. Pentru formarea şi stabilizarea unei emulsii U/A se urmăreşte intervenţia stearatului de sodiu, sare a unui acid gras cu 18 atomi de carbon. Catena hidrocarbonată este imaginată printr-un dreptunghi, în timp ce partea hidrofilă, gruparea polarizata, este reprezentată ca un cerc.
Fig.nr.31. Reprezentarea părţii hidrofobe şi hidrofobe a unui tensioactiv anionic - stearat de sodiu
În momentul în care este adăugat un astfel de tensioactiv, într-un sistem format din două lichide nemiscibile, moleculele de săpun - prin anionii lor - au tendinţa de a se acumula la suprafaţa despărţitoare, orientându-se cu gruparea carboxil către mediul apos şi radicalul hidrocarbonat spre ulei (figura 32), formând o peliculă în jurul particulei.
Fig.nr.32. Schema formarii unui film monomolecular de: (a) stearat de sodiu în jurul unei picături de ulei într-o emulsie U/A; (b) stearat de calciu în jurul picăturii de apa în emulsia tip A/U.
222
Între cele două lichide nemiscibile apare o zonă de tranziţie, ce realizează separarea fazelor concomitent cu scăderea tensiunii interfaciale şi creşterea suprafeţei de dispersare. Lichidul emulsionat se va transforma în picături mici ce se dispersează omogen şi formează emulsia.
Pe lângă faptul că moleculele de tensioactiv realizează reducerea tensiunii superficiale (dintre cele două lichide complet deosebite), prin acumularea lor la suprafaţa fazei dispersate ele au rol similar unei bariere mecanice ce se opune unirii picăturilor aceluiaşi lichid într-o picătură unică. La acest efect se adăuga şi respingerea electrostatică impusă de prezenţă unor sarcini electrice existente pe suprafaţa particulelor emulsionate.
Stearatul de calciu utilizat ca emulgator într-o emulsie A/U se orientează cu grupările de hidrocarbură către ulei şi cu grupările carboxil spre apă.
Teoria penei - explică formarea emulsiilor la care emulgatorul, prin volumul diferit al celor două grupări hidrofile şi lipofile, sugerează forma de pană (prismă triunghiulară utilizată la despicarea lemnului). În cazul stearatului de sodiu, gruparea hidrofilă îşi va mări considerabil volumul prin efectul de hidratare şi gruparea lipofilă rămâne neschimbată. Moleculele de stearat de sodiu se vor, orienta într-un strat monomolecular la interfaţa ulei - apă şi tensiunea interfacială este înlăturată. Se formează noi suprafeţe de separaţie între grupările hidrofile şi faza apoasă şi lanţurile de atomi de carbon şi faza uleioasă, care prezintă tensiune interfacială redusă sau nulă.
Substanţa care are caracter accentuat hidrofil sau lipofil se dizolvă în faza respectivă şi nu poate rămâne orientată la interfaţa celor două lichide nemiscibile, fiind neutilizabilă ca emulgator.
Gruparea hidrofilă a stearatului de sodiu se dizolvă mai uşor în faza apoasă decât gruparea oleofilă în ulei şi tensiunea interfacială dinspre faza apoasă este mai scăzută decât spre faza uleioasă. Datorită tensiunii interfaciale mai puternice spre faza uleioasă se produce o curbare a suprafeţei de separare către partea uleioasă, care capătă formă sferică.
Săpunurile bivalente se comportă ca emulgator de tip A/U la care predomină grupările lipofile ce se dizolvă mai uşor în ulei decât grupările hidrofile în apă.
În cazul stearatului de calciu, tensiunea interfacială spre faza apoasă rămâne mai ridicată decât spre ulei şi are loc o curbare a suprafeţelor de separaţie spre faza apoasă, formându-se picături de apă dispersate în ulei.
Teoria formării filmului plastic explică stabilitatea emulsiilor cu săpunuri alcaline, substanţe sub formă de pulberi fine sau cu emulgatori complecşi constituiţi dintr-un emulgator U/A şi altul A/U.
Asociind doi emulgatori opuşi ca acţiune, se poate obţine o reducere mai accentuată a tensiunii interfaciale decât se obţine cu fiecare emulgator separat. Asocierea de emulgatori (cetilsulfat de sodiu şi colesterol, stearat de sodiu cu colesterol, polisorbat cu spanuri, laurilsulfat de sodiu cu monostearat de gliceril) se orientează cu grupările hidrofile spre faza apoasă, cu cele lipofile spre faza uleioasă.
223
În plus, emulgatorii ionogeni conferă sarcină electrică, formând un înveliş de sarcini negative şi pozitive. Stratul de ioni de acelaşi fel contribuie la respingerea electrostatică între particule, mărind stabilitatea emulsiei.
Orientarea moleculelor emulgatorului la suprafaţa de separare între cele două faze; urmată de fixarea mai mică sau mai mare de moleculele de apă sau ulei ca prezenţă, în unele cazuri, a unui înveliş de sarcini electrice, este interpretată ca un film care se opune coalescenţei şi ruperii emulsiei. Filmul de adsorbţie trebuie să fie suficient de solid pentru a se opune tendinţei de contopire a particulelor, dar şi cu o elasticitate corespunzătoare, pentru a rezista la eventualele deformări la agitare sau curgere a emulsiei.
W.D. Bancroft enunţă regula conform căreia faza externă a unei emulsii va fi aceea în care emulgatorul este mai solubil, sau altfel spus, emulgatorul emulsionează faza în care nu se dizolvă.
Tipul emulsiei este dependent de structura moleculei emulgatorului. În domeniul emulsiilor s-a demonstrat ca un emulgator poate realiza ambele tipuri de emulsii, condiţionat de formularea preparatului şi modul de preparare.
Caracterul amfoter al moleculei de lecitină, ca şi proporţia dintre cele două faze, permite să se obţină emulsii U/A şi A/U.
¾ Emulgatori adevăraţi - substanţe tensioactive
•Emulgatori anionici
Săpunurile monovalente sunt constituite dintr-un lanţ de 12 - 18 atomi de carbon, lipofil, şi o grupare carboxil, sarea alcalină puternic hidrofilă care îşi manifestă cu preponderenţă caracterul faţă de lipofilia catenei de atomi de carbon. În plus, în soluţia apoasă săpunurile alcaline disociază, anionului revenindu-i astfel acţiunea emulgatoare, motiv pentru care sunt emulgatori tip U/A. Săpunurile de sodiu, potasiu şi amoniu sunt cele mai utilizate în scop farmaceutic. Orientarea moleculelor de săpun în micele explică acţiunea stabilizantă a acestora. Săpunul de amoniu se obţine în timpul preparării emulsiei prin reacţia dintre acizii graşi liberi din uleiul vegetal şi amoniac.
Acţiunea de emulgator a stearatului de amoniu format “in situ” este eficientă pentru stabilizarea emulsiei de tip U/A - respectiv a linimentului amoniacal.
Proprietăţile emulsive pot fi mărite prin introducerea de grupări hidrofile în molecula săpunului, ca gruparea hidroxil, dubla legătura, gruparea sulfurică la acidul oleic, acidul ricinoleic şi esterul sulfuric al acestuia.
Săpunurile alcaline sunt instabile în mediul acid, incompatibile cu sărurile de calciu şi magneziu când se formează săpunurile respective, insolubile în apă. Săpunurile bivalente (stearat de calciu, magneziu) şi trivalente sunt insolubile în apă, solubile în ulei. Săpunurile de calciu sunt emulgatorii care se formează în timpul preparării linimentului oleo-calcar, din reacţia acizilor liberi cu hidroxidul de calciu.
224
Săpunurile de amine sau săpunurile organice sunt săruri ale acizilor graşi cu aminele aciclice (trietanolamina) sau amine ciclice (morfolina), cu proprietăţi emulsive de tip U/A. Laurat de monoetanolamină, laurat de dietanolamină, oleat de trietanolamină sunt folosite la obţinerea emulsiilor U/A, de uz extern.
Emulsiile rezultate cu emulgatorii reprezentaţi de săpunurile organice sunt mai stabile, au un grad de dispersie superior şi fiind mai puţin alcaline sau chiar neutre, nu irită pielea.
Esteri ai alcoolilor superiori cu acidul sulfuric sunt produşi ce provin prin esterificarea alcoolului lauric, cetilic sau stearilic cu acidul sulfuric: laurilsulfat de sodiu, cetilsulfatul de sodiu şi stearilsulfatul de sodiu. Substanţele se comportă ca săpunurile, au însă reacţie neutră, formează săruri de calciu hidrosolubile şi sunt insensibile faţă de electroliţi. F.R. X oficializează laurilsulfatul de sodiu folosit ca emulgator U/A, în concentraţie de 0,7 - 2% în emulsii fluide, linimente, unguenteemulsii.
F.R. X oficializează asocierea alcoolului cetilic şi alcoolului stearilic ce intră în compoziţia alcoolului cetilstearilic, emulgator în proporţie de 90%, cu 10% cetilstearilsulfatul de sodiu.
Derivaţi sulfonaţi ai acizilor graşi sunt substanţe cu formula generala R- SO2-O-Na+. Cel mai important reprezentant este dioctilsulfosuccinatul de sodiu - Aerosol OT sau Manoxol OT. Este un emulgator cu proprietăţi tensioactive marcate; nu reacţionează cu ionul de calciu.
Carbopolii (carbomeri) sunt polimeri de carboxivinil cu grupe carboxil distribuite pe catenă. Carbopolul se utilizează în emulsii după neutralizarea cu o amină sau hidroxid de sodiu, pentru a asigura grupări solubile în ulei şi apă. În cazul emulsiilor cu concentraţii reduse de fază uleioasă, neutralizarea carbopolului se face numai cu hidroxid de sodiu. Vâscozitatea maximă a emulsiilor se obţine la pH 6 şi scade apoi odată cu creşterea pH-ului.
•Emulgatorii cationici
Emulgatorii cationici sunt combinaţii de amoniu cuaternar (numite şi săpunuri inverse, săpunuri cationice) la care cationului îi revin proprietăţile emulsionante: bromura de cetiltrimetilamoniu (cetrimid), clorura de benzalconiu (zefirol) sunt compuşi solubili în apă ce determină formarea de emulsii U/A. Totodată, având proprietatea de a modifica permeabilitatea la nivelul membranelor biologice, au şi proprietăţi antiseptice şi de aceea pot fi utilizate în scop conservant. Sunt incompatibile cu agenţi tensioactivi anionici şi unele substanţe ca iodul, fenolul, hidroxizii alcalini, săpunuri etc.
•Emulgatori amfoteri
Gelatina - este o proteină purificată obţinută prin hidroliza acidă parţială sau hidroliza alcalină parţială a ţesuturilor animale cu conţinut în colagen. Gelatinele au
225
un caracter amfoter. În soluţie alcalină, gelatina este emulgator anionic, în soluţie acidă este emulgator cationic. Gelatinele sunt solubile în apă încălzită la aproximativ 60°C; se imbibă absorbind o cantitate de 5 -10 ori mai mare decât masa proprie. În concentraţii sub 1%, gelatinele dau soluţii coloidale. Peste această concentraţie realizează geluri moi sau elastice.
Vâscozitatea şi stabilitatea lor este cea mai redusă la punctul izoelectric şi pH 7 - 8,3 pentru gelatina de tip A şi pH 4,7 - 5 pentru gelatina tip B.
Lecitinele - provin de la glicerină în care două grupări hidroxil sunt esterificate cu acizi graşi superiori, a treia grupă hidroxil cu acid fosforic, de care se leagă un rest de colină sau colamină. Grupările acid fosforic - colina, respectiv colamina, sunt hidrofile, resturile de acizi graşi lipofile, rezultând o echilibrare a celor două tipuri de grupări, încât lecitinele pot forma emulsii de ambele tipuri, în funcţie de predominanţa fazei apoase sau uleioase şi tehnica de lucru.
Lecitinele se pot utiliza şi la prepararea emulsiilor parenterale.
•Emulgatori neionogeni
Alcoolii superiori (alcool cetilic, stearilic, lauric) sunt substanţe cu caracter lipofil ce determină formarea de emulsii A/U. În cazul acestor alcooli, gruparea hidroxil (componenta hidrofilă) nu imprimă moleculei proprietăţile hidrofile, motiv pentru care sunt consideraţi stabilizatori de emulsii de tip A/U.
F.R. X oficializează amestecul de alcool stearilic şi alcool cetilic l: l sub denumirea de Alcoholum cetylstearylicum (cetosterol, ceara Lanette 0).
Colesterolul - reprezintă un alcool ciclic cu un hidroxil şi o dublă legătură, grupări hidrofile ce nu-şi manifestă caracterul faţă de puternicul caracter hidrofob dat de cele patru cicluri de atomi de carbon, ceea ce face ca substanţa să constituie un emulgator de tip A/U.
Esterii parţiali ai acizilor graşi superiori cu polialcoolii permit obţinerea de emulsii de tip A/U (esteri cu etilenglicolul sau propilenglicolul). Dintre esterii parţiali ai glicerolului se utilizează monostearatul de gliceril în scopul creşterii proprietăţilor emulsive ale altor emulgatorilor anionactivi, cationactivi sau neionici. Se obţin monostearaţi de gliceril autoemulgatori sub denumirea de Tegin şi Margamuls etc.
Esterii acizilor graşi cu sorbitanul (Span, Arlacel, Crill, Crilex) se obţin din sorbitol care, prin eliminarea unei molecule de apă, trece în anhidrida internă - sorbitan; aceasta este esterificată cu diferiţi acizi graşi. Produsele sunt notate cu cifre ce exprimă în mod arbitrar natura acidului gras cu care s-a realizat esterificarea:
Span 20 - sorbitan monolaurat; Span 40 - sorbitan monopalmitat;
Span 60 - sorbitan monostearat; Span 80 - sorbitan monooleat; Span 85 - sorbitan trioleat.
226
La aceşti emulgatori, grupările oleofile sunt preponderente faţă de grupările hidrofile; de aceea formează emulsii de tip A/U.
Monopalmitatul, monostearatul şi tristearatul de sorbitan sunt produşi solizi, ceilalţi esteri sunt fluizi.
Derivaţii de polioxielilen ai esterilor acizilor graşi cu sorbitanul (eteri ai spanurilor cu PEG-uri) sunt cunoscuţi sub denumirea de Tweenuri sau polisorbaţi. În funcţie de natura radicalului acidului gras, de numărul şi lungimea catenelor de polietilenglicol, produşii au aceeaşi numerotare cu Spanurile:
Tween 20 - PEG - sorbitan monolaurat; Tween 40 - PEG - sorbitan monopalmitat; Tween 60 - PEG - sorbitan monostearat; Tween 80 - PEG - sorbitan monooleat; Tween 85 - PEG - sorbitan trioleat.
Introducerea în molecula spanurilor a catenelor de PEG, cu caracter hidrofil, va conferi proprietăţi de emulgator pentru emulsiile de tip U/A. Acestea sunt stabile la variaţii de pH şi electroliţi.
În F.R. X se oficializează Tweenul 80 cu denumirea de Sorbimacrogoli oleas 300 sau polisorbat 80. Tweenurile intră în compoziţia emulsiilor de uz extem şi intern; pot fi solubilizanţi, umectanţi. Prezintă dezavantajul unui gust neplăcut şi facilitează absorbţia substanţelor toxice în organismul uman, ceea ce limitează utilizarea în cazul emulsiilor de uz intern la concentraţii de 2-3%; se admite folosirea unei concentraţii care să nu depăşească o proporţie mai mare de 25 mg/kg corp.
Tensioactivii neionogeni sunt mai puţin toxici decât cei ionogeni şi mai puţin sensibili la electroliţi şi la variaţii de pH.
Peliculele interfaciale la interfaţa U/A formate de tensioactivii neionogeni nu sunt încărcate electric şi stabilitatea sistemului este conferită de lanţurile hidratate de oxid de etilen, care produc o respingere sterică.
Esterii acizilor graşi cu polietilenglicolii se cunosc sub denumirea de Myrj 41, 55, 52 etc., care se deosebesc după numărul de grupări de oxid de etilen.
Eteri ai alcoolilor graşi superiori cu polietilenglicolii (Brij) prezintă caracter predominant hidrofil şi se utilizează ca atare sau participă la formarea de emulgatori complecşi. Cei mai importanţi sunt:
Brij 30 - eter monolauric al PEG;
Brij 52 - eter cetilic al PEG; Brij 72 - eter stearilic al PEG; Brij 98 - eter oleic. al PEG.
Saponozidele - sunt emulgatori naturali care se clasifică în funcţie de aglicon în saponozide sterolice şi saponozide triterpenice. Se caracterizează printr-o accentuată acţiune de suprafaţă, reducând puternic tensiunea interfacială; în concentraţii mici de 0,1-0,5% se utilizează ca stabilizatori în asociere cu alţi emulgatori.
227
•Balanţa hidrofil - lipofilă (HLB)
Proprietăţile substanţelor tensioactive sunt strâns legate de structura moleculelor şi depind, în special, de echilibrul care se stabileşte între grupările lipofile şi hidrofile ale moleculei respective. Aceasta permite, într-o oarecare măsură, sesizarea domeniului de utilizare a fiecărui tensioactiv.
Balanţa hidrofil - lipofilă (Hydrophile - Lipophile Balance - HLB) este un sistem de clasificare a tensidelor definit de M.C. Griffin.
Valoarea HLB este în funcţie directă de importanţa părţii hidrofile a moleculei:
¾este maximă când predomină valoarea hidrofilă;
¾este scăzută la molecule lipofile.
O moleculă de substanţă tensioactivă care este hidrofilă 100% are valoarea HLB ipotetica 20. Scara cifrică a valorilor HLB a fost stabilită între 1-40, cu punctul de echilibru, unde hidrofilia este egală cu lipofilia, ca fiind 10.
Valorile HLB până la 20 se referă la produşi neionogeni.
O valoare HLB peste 20 înseamnă că hidrofilia unui produs în comparaţie cu etalonul (cu valoarea HLB egala cu 10) este mai mare. Fenomenul este caracteristic la unii tensioactivi anionici ca în cazul laurilsulfalului de sodiu cu HLB egal cu 40.
Tabel 12. Valorile balanţei hidrofil-lipofilă (HLB) a unor substanţe tensioactive
Trioleat de sorbitan (Span 85; Arlacel 85) |
1,8 |
Monostearat de gliceril (Tegin 515) |
3,8 |
Monostearat de sorbitan (Span 60; Arlacel 65) |
4,7 |
Guma arabică |
8,0 |
Monolaurat de sorbitan (Span 20; Arlacel 20) |
8,0 |
Metilceluloză 15 (Methacel 15) |
10,5 |
Monostearat de PEG 400 (Myrj 45) |
11,11 |
Oleat de trietanolamină |
12,0 |
Tragacanta |
13,2 |
Polisorbat 60 (Tween 60) |
14,9 |
Polisorbat 80 (Tween 80) |
15,0 |
Polisorbat 20 (Tween 20) |
16,7 |
Oleat de sodiu |
18,0 |
Oleat de potasiu |
28,0 |
Laurilsulfat de sodiu (Duponol) |
40,0 |
Substanţele cu valoare HLB inferioară cifrei 1 sau superioară lui 50 sunt fie solubile în ulei, fie în apă, conform tabelului următor.
228

GM
LIPOFILI |
|
HIDROFILI |
|
|
TENSIOACTIVI |
|
|
Solubili |
DISPERSABILI |
|
Solubili |
în ulei |
în |
|
în apă |
ulei |
apă |
|
|
|
SOLVENŢI |
|
|
# 1 |
# 10 |
# 50 |
HLB |
Fig.nr.33. Comportarea substanţelor tensioactive
Valoarea HLB reflectă o serie de caractere ale tensioactivului: solubilitatea în apă sau ulei, constanta dielectrică, tensiunea interfacială.
La valori HLB cuprinse între:
¾1-3 tensioactivul nu se dispersează în apă;
¾între 3- 6 este o dispersie slabă;
¾între 6 - 8 la agitare puternică se obţine o dispersie lăptoasă care devine mai stabilă la valori 8 - 10;
¾între 10 - 13 aspectul este translucid până la lichid limpede,
¾peste 13 rezultă o soluţie clară.
În funcţie de valoarea HLB a tensidului, se apreciază domeniul de utilizare:
9antispumanţi HLB 1,5 – 3,
9emulgatori A/U HLB 3 – 6,
9umectanţi HLB 7 – 9,
9emulgatori U/A HLB 8 – 18,
9detergenţiHLB 13 – 15,
9solubilizanţi HLB 15 – 18.
Unele tenside sunt utilizate ca antiseptice în preparate pentru piele, mucoase
şi ca dezinfectante pentru materialele chirurgicale. Tensioactivii cationici prezintă proprietăţi cheratolitice. În general, substanţele tensioactive influenţează viteza şi durata efectului terapeutic, modificând viteza de penetrare a substanţei active. În anumite cazuri, ele pot mari eficacitatea unui medicament, dar este posibilă o reducere a efectului terapeutic.
229

Metode de determinare a valorii HLB. Valoarea HLB a unei substanţe tensioactive poate fi stabilită experimental sau prin calcul.
Metodele experimentale de determinare a valorii HLB implică prepararea şi observarea unui număr mare de emulsii test şi au la bază relaţiile existente între HLB şi constanta dielectrică, între HLB şi căldura de hidratare a derivaţilor polietilenglicolici etc.
Gorman a stabilit existenţa unei funcţii logaritmice între HLB şi constanta dielectrică ε de tipul:
HLB = f(logε )
Pe baza valorilor experimentale obţinute se alcătuieşte un grafic, iar prin extrapolare se determină valoarea HLB.
Metodele experimentale de determinare a HLB necesită un timp apreciabil, motiv pentru care se preferă determinarea valorii HLB prin calcul, ţinând cont de numărul grupelor polare sau lipofile conţinute în molecula tensioactivului respectiv.
Pentru un număr mare de esteri ai acizilor graşi cu alcooli superiori, se aplică formula stabilită de Griffin:
|
|
S |
|
HLB = 20 1 |
− |
|
|
|
|||
|
|
A |
|
în care: S = indicele de saponificare al esterului acidului gras;
A = indicele de aciditate al acidului gras;
În cazul esterilor acizilor graşi la care nu se poate obţine un indice exact de saponificare, se utilizează formula:
HLB = E + P
5
în care: E = greutatea procentuală în oxid de etilen;
P = greutatea procentuală a conţinutului în alcool polihidroxilic (glicerol, sorbitol)
Pentru substanţele tensioactive care posedă partea hidrofilă constituită numai din grupări de oxid de etilen, respectiv alcooli polihidroxilici, ecuaţia devine:
HLB = E5 sau HLB = P5
Aceste relaţii nu se pot aplica tensidelor care conţin oxid de propilen, oxid de butilen, azot, sulf sau tensidelor ionogene care disociază în soluţii apoase şi devin
230
