
133851261-119352752-Tehnica-farmaceutica
.pdf
In unele cazuri medicamentele parenterale nu pot fi supuse unor metode radicale de distrugere a microorganismelor, de aceea se recurge la aplicarea unei metode care să asigure sterilitatea şi evitarea contaminării cu pirogene cât şi dezvoltarea microorgansimelor, cunoscută sub denumirea de metoda aseptică.
Asepsia, cuvânt provenit de la două cuvinte din limba greacă: a = fără, sepsis = infecţie, reprezintă ansamblul de măsuri utilizate pentru a impiedica infestarea cu micoorganisme sau viruşi a unui organsim viu, mediu inert sau a unui preparat medicamentos. Se realizează printr-o serie de metode fizice şi chimice şi prin luarea unor măsuri de precauţie prin care se evită pătrunderea microorganismelor.
Atât în laboratorul de soluţii sterile cât şi în industria farmaceutică prepararea medicamentelor parenterale se va efectua în spaţii special amenajate, numite zone sterile(boxe sau blocuri sterile). Aceste incăperi sterile se pot clasifica:
¾Clasice, având flux convenţional al aerului;
¾Încăperi cu flux laminar al aerului. Cele clasice pot fi: 1). vitrine sterile;
2). încăperi sau blocuri sterile.
1. vitrinele sterile au forme diferite; sunt de dimensiuni mici şi sunt închise etanş, iar operatorul se află în exterior. Operaţiile se realizează fie cu ajutorul unor mănuşi etanşe fixate în perete, în care se introduc mâinile, fie cu ajutorul unui mecanism, cu comenzile din exterior. Vitrinele de sticlă au pereţi din sticlă, observându-se ce se petrece în interior; au una sau mai multe uşi batante, surse de aer filtrat şi lămpi cu U.V.. Vitrinele cu pereţi supli, gonflabile şi transparente sunt denumite bule sterile.
Fig.nr.13. Vitrină sterilă sau izolator
2. sălile sau blocurile sterile (Sali albe sterile = S.A.S.) au construcţie mai complexă, operatorul trebuind să intre în interiorul acestora, deci el devind o sursă de contaminare permanentă. Este necesar să se asigure condiţii de climatizare favorabile desfăşurării procesului de producţie.
111
În încăperea sterilă trebuie să se asigure pătrunderea aerului prefiltrat, apoi climatizat, filtrat printr-un filtru sterilizant şi iradiat cu raze U.V.. La ieşirea din incintă există un ventilator cu care se face recircularea aerului. Intrarea în incinta de sterilizare se face prin uşi batante (cele glisante nu pot fi curăţate în toate punctele).
În încăperea sterilă, la mijlocul ei, poate fi instalată şi o boxă sterilă, în care să pătrundă aer prefiltrat, climatizat şi filtrat, diferit de cel din incinta încăperii; boxa este prevăzută cu o lampă de U.V..
Înainte de a intra în încăperea sterilă, există cel puţin două încăperi, denumite S.A.S. (sas-uri):
1.o încăpere în care se realizează o prelucrare a materialului;
2.o alta de pregătire a personalului.
Intrarea în S.A.S. se face dintr-un culoar. Înainte de începerea lucrului, trebuie asigurată sterilizarea materialului, a spaţiului şi a ustensilelor cu vapori de formol (operaţie care se realizează în pauza de lucru).
Materialul cu volum mic: recipientele de condiţionare, pulberile solide, sunt sterilizate în afara blocului steril şi vin în ambalaje mari care nu sunt sterile în exterior. Deci este necesar ca aceste materiale să fie introduse în SAS-ul de materiale, care poate fi un sterilizator cu dublă deschidere, una către exterior prin care introducem materialul şi alta către camera sterilă.
Uneori este suficientă prezenţa lămpilor de U.V. pentru materialele solide, flacoane.
Lichidele, solvenţii şi unele soluţii, sunt introduse în incinta sterilă în două moduri:
a)sterilizate în afară şi furnizate în recipiente ermetic închise, lăsate mai întâi
în S.A.S.-ul de materiale;
b)aduse direct în incinta sterilă prin conducte de canalizare (apa distilată).
Conductele au la locul de deschidere un filtru sterilizant, care este util pentru sterilizarea unor gaze (azot şi dioxid de carbon) necesare în prepararea unor soluţii sensibile la acţiunea oxigenului.
Personalul este ales cu grijă, este bine instruit şi sănătos. Acesta se dezbracă în S.A.S.-ul pentru personal şi primeşte un halat de protecţie steril, bonetă, mănuşi sterilizate, încălţăminte sterilă şi o mască sterilă, iar pentru protecţie de U.V. ochelari fumurii.
În unele săli sterile, operatorul poartă costum de scafandru, deci respiră prin tub, deci nu mai este nevoie de climatizarea aerului şi nici pericol de contaminare de la operator.
Mai eficiente sunt încăperile cu flux laminar, traversate de un aer care se deplasează uniform, în linii paralele.
Sunt denumite camere sau săli albe sterile, pentru că sunt lipsite complet de particule în suspensie, eliminate prin mişcări laminare ale aerului. Cele mai eficiente când fluxul de aer este vertical. Există şi flux de aer orizontal, precum şi cu mişcare
112
mixtă – vertical din plafon către podea. Plafonul din filtre HEPA; iar podeaua dintr-o grilă dublată de o podea poroasă, care poate fi un prefiltru, în cazul reciclării aerului.
La fluxul vertical, aerul deplasându-se de sus în jos, antrenează particule, care datorită gravitaţiei se depun. Acesta este foarte costisitor. Mai frecvent este fluxul orizontal, în care aerul circulă de la un perete poros HEPA, la peretele opus.
Particulele şi microorganismele circulă şi se depun pe suprafeţe paralele cu fluxul de aer. Acest spaţiu trebuie curăţat din timp în timp.
Se întâlnesc şi încăperi mixte, în care mişcarea laminară este de la perete la sol sau de la plafon la perete. Mişcările sunt paralele.
Folosită în încăperile sterile demontabile, ce pot fi instalate ca acoperiş deasupra maşinilor de umplut şi închis fiole, care trebuie să funcţioneze în spaţiu steril. Aerul trebuie de asemenea condiţionat (temperatură şi umiditate).
Spaţiile sterile trebuie supuse unui control minuţios al sterilizării (un control microbiologic) constând în plasarea de culturi sterile, aduse apoi în etuvă şi observându-se dacă s-au dezvoltat culturile, apreciindu-se asepsia sau lipsa de asepsie.
La fluxul laminare controlul se face cu anemometru, iar capacitatea de reţinere a impurităţilor cu aparate de numărare a particulelor.
A doua categorie de preparate parenterale este reprezentată de cele care după condiţionare (umplerea şi închiderea fiolelor sau flacoanelor) sunt supuse sterilizării. Acestea sunt realizate în industrie în cantităţi mari, în spaţii speciale, foarte curate, dar nu sterile, cu un grad de contaminare microbiană minim. Aceste preparate se realizează şi în farmaciile de spital în blocul steril, unde se realizează perfuzii.
Spre deosebire de sterilizare, care urmăreşte înlăturarea tuturor germenilor patogeni şi nepatogeni, o altă metodă dezinfecţia, reprezintă ansamblul de măsuri folosite pentru distrugerea germenilor patogeni. Conservarea constă într-o serie de măsuri folosite pentru a păstra un preparat farmaceutic în condiţii de calitate corespunzătoare de la preparare şi până la expirarea termenului de valabilitate, respectiv constă în limitarea acţiunii microorgansimelor prin păstrarea medicamentelor în anumite condiţii: la rece, la loc racoros, la temperatura camerei şi adausul de agenţi antimicrobieni (conservanţi).
Pentru obţinerea unor preparate farmaceutice sterile este necesar să ţinem cont de o serie de recomandări în timpul preparării:
¾materiile prime să prezinte un conţinut cât mai mic în microorgansime sau să fie sterile; la denumirea substanţelor farmaceutice, folosite la prepararea medicamentelor paraenterale, va exista precizarea „pro injectiones”;
¾etapele de lucru vor fi efectuate fără întrerupere, respectiv se va lucra „în flux continuu”;
¾în timpul preparării se va evita contaminarea cu microorganisme a produsului, activitatea desfăşurându-se în spaţiile special amenajate:
113
încăperi cu pereţi şi pardoseală lavabilă, ustensile şi aparatură folosită numai în aceste încăperi, sterilizarea încăperilor şi ustensilelor cu radiaţii UV.
Distrugerea microorgansimelor se poate realiza prin metode de sterilizare: fizice, chimice şi mecanice.
A.Metode fizice de sterilizare:
•sterilizarea prin caldura - uscată;
-umedă;
•sterilizarea cu radiaţii - radiaţii UV;
-radiaţii ionizante.
B.Metode mecanice de sterilizare:
•sterlizarea prin filtrare;
•prepararea pe cale aseptică.
C.Metode chimice de sterilizare:
•sterilizarea cu gaze;
•sterilizarea folosind substanţe antiseptice (prin adaus de conservanţi).
Sterilizarea cu căldură uscată se realizează în etuve încălzite electric şi construite astfel încât să asigure o temperatură constantă şi uniformă în tot spaţiul de sterilizare. Pentru a permite transferul căldurii, este realizată o circulaţie forţată, materialul supus sterilizării să aibă o suprafaţă cât mai mică, să se facă o încărcare a etuvei, care să permită circulaţia optimă a aerului cald (deci nu trebuie să fie prea încărcată pentru a avea spaţii pentru circulaţia căldurii).
Înainte de încărcare, etuva poate fi preîncălzită până aproape de temperatura cerută, pentru a micşora timpul eficient de încălzire. Durata de sterilizare este variabilă şi destul de mare: 1600C – 3ore; 1700C -1 oră; 1800C – 30 minute.
Sunt admise şi alte condiţii de timp şi temperatură eficiente cel puţin şi prevăzute în monografii.
La etuvă se vor steriliza produsele rezistente la căldură şi produsele neapoase: pulberi, produse uleioase, materiale de laborator din sticlă sau porţelan, instrumentar medical fără sudura.
Produsele care sunt supuse sterilizării trebuiesc ambalate în prealabil, evitându-se contaminarea ulterioară, după sterilizare.
În industrie se întâlnesc şi cuptoare tunel, respectiv tunele de uscare şi sterilizare, care permit sterilizarea continuă, pentru fiolele şi flacoanele folosite pentru condiţionarea aseptică, deci ele trebuie să iasă din tunel, într-un spaţiu aseptic.
Este o metoda inscrisa în FR X.
Sterilizarea cucaldura umeda cere temperatură şi timp de sterilizare, cu valori mult mai mici decat sterilizarea cu aer cald.
Aceasta metoda se realizeaza în aparate speciale numite autoclave. Autoclavul este vertical dar în industrise folosesc cele orizontale, cu deschideri
114
laterale, pentru a permite încărcarea şi descărcarea uşoară a materialului după platforme speciale.
Închiderea este realizată cu un capac special, având un dispozitiv de securitate, ce împiedică deschiderea autoclavului sub presiune. Au două deschideri pentru siguranţă şi funcţionare.
Eficienţa sterilizării este condiţionată de evacuarea aerului. Sunt prevăzute cu dispozitive de vid, pentru eliminarea aerului.
Vaporii de apă sunt furnizaţi de un generator exterior. Omogenizarea temperaturii este accelerată cu un ventilator.
Pentru a se grăbi răcirea, sunt prevăzute cu un dispozitiv, ce introduce un curent de aer rece, după timpul de sterilizare. Este necesară o răcire mai rapidă în special pentru soluţii cu substanţe termolabile, care se descompun.
Pentru a se evita scăderea prea bruscă a presiunii, unele aparate funcţionează cu aer comprimat, evitându-se spargerea recipientelor (dispozitiv de compresiune).
Aparate prevăzute cu sistem de programare, ce asigură succesiunea operaţiunilor - înregistrator de presiune şi de temperatură, prin al căror grafic se poate urmări dacă fiecare lot a fost supus ciclului complet de sterilizare conform programului.
Sterilizarea cu vapori sub presiune este o metoda inscrisa în FR X şi utilizată pentru soluţiile apoase, pansamente. Timpul de sterilizare variază cu temperatura - cel puţin 15 minute pentru temperatura de 1210C, şi cel puţin 30 minute la 1150C şi presiunea de 2 atmosfere. Se admit şi alte condiţii de temperatură şi timp a căror eficienţă a fost dovedită.
Pansamentele chirurgicale se sterilizează la 1340 -1380C la presiunea de 2 atmosfere, timp de 5 minute, fiind condiţionate în recipiente, ce asigură penetrarea vaporilor de apă.
Articolele de sticlă, porţelan, metal la 1210C - 1240C timp de 20 de minute. Durata de sterilizare trebuie măsurată din momentul realizării condiţiilor
prevăzute în acest sens.
Ca să fie corectă, în timpul sterilizării temperatura trebuie să poată fi măsurată cu o precizie de + 20C, iar presiunea de + 0,l atmosfere. Temperatura trebuie măsurată în partea cea mai rece a autoclavului, deci în partea de jos, aproape de tubul de evacuare a aerului - tubul de purjare.
Pentru controlul parametrilor de sterilizare se foloses tuburi de control, mici, din sticlă, închise ermetic, cu o substanţă chimică solidă - pulbere, cu urme de colorant miscibil; plasate în diverse părţi ale autoclavului.
Când temperatura este superioară (punctului de topire) al substanţei, aceasta se topeşte şi se colorează uniform (chiar dacă se solidifică la deschiderea autoclavului). Astfel se pot folosi: β - naftolul care are p.t. 1100C, antipirina cu p.t. 1140C, acidul benzoic cu p.t. 1210C sau fenacetina cu p.t. 1350C. Dar în acest fel nu se indică decât temperatura maximă atinsă, dar nu şi durata cât ea a fost maximă.
115
Se mai folosesc benzi adezive, lipite pe obiectele de sterilizat şi a căror coloraţie variază cu temperatura şi timpul de sterilizare. Eficacitatea sterilizării este controlată prin inocularea probelor-test cu germeni termorezistenţi Bacillus stearotermophillus, autoclavul trebuie încărcat în acelaşi fel.
F.R. X. nu prevede alte metode de sterilizare, dar în F.R. IX. erau prevăzute: sterilizarea prin încălzire repetată (Tindalizarea sau sterilizarea fracţionată) şi fierberea la 1000C timp de 60 minute. Mentionam ca nu sunt metode care sa asigure pe deplin sterilitatea preparatelor farmaceutice.
Pentru mai multă siguranţă, tindalizarea poate fi asociată cu filtrarea sterilizantă sau prepararea pe cale aseptică.
Se poate realiza şi prin fierbere pe baie de apa sau introducerea recipientelor în autoclav, căruia i se menţine deschis robinetul de vapori: sterilizarea cu vapori fluenţi.
Farmacopeea Britanică prevede pentru cazuri speciale sterilizarea la 1000C, dar asociindu-se cu un agent antimicrobian (bactericid) clorocrezolul 0,2%, acetat sau borat de fenil mercur 0,002%. În aceste cazuri, trebuie să ţinem seama de recomandările din F.R. X: nu se admite adaosul conservanţilor antimicrobieni în cazul preparatelor injectabile care sunt folosite într-un volum mai mare de l0 ml, indiferent de modul de administrare şi în cazul soluţiilor care se administrează intracisternal, iintracardiac, intrarahidian, intraocular, peridural indiferent de modul de administrare.
Flambarea este un procedeu rudimentar (care nu-i prevăzut în nici o farmacopee) şi este folosit în farmacie, pentru obiecte neinflamabile şi stabile la temperaturi înalte. Se trec obiectele prin flacără (de exemplu: spatulele metalice) sau se umectează obiectul cu alcool, se aprinde şi se incinerează microorganismele de la suprafaţă. Se poate folosi pentru mojare şi pistile.
Dezavantajul acestei metode consta în faptul ca microorganismele omorâte rămân la suprafaţa obiectului şi pot fi surse de pirogene.
Sterilizarea prin filtrare, numită filtrare sterilizantă reprezintă o metodă de eliminare a germenilor microbieni, prin trecerea fluidului de sterilizat, printr-un material poros, cu pori foarte fini, sub influenţa unei diferenţe de presiune.
În domeniul farmaceutic, filtrarea sterilizantă se aplică:
-soluţiilor apoase cu substanţe termolabile;
-pentru sterilizarea aerului necesar în spaţiile în care se prepară aseptic medicamentul (în boxele sterile).
Sterilizarea prin filtrare, diferă de celelalte tipuri de sterilizare, pentru că microorganismele nu sunt distruse, ci îndepărtate fizic.
Reţinerea microorganismelor are loc prin fenomenul:
-de strecurare – cernere (pur mecanic), prin care sunt reţinute microorganismele cu dimensiuni mai mari decât porii filtrului;
116
-prin adsorbţie - reţinerea particulelor în interiorul canaliculelor filtrului, când intervin fenomene ca: tensiune superficială, capilaritate, adeziune, sarcini electrice (deci fenomene fizico-chimice).
Prin aceste fenomene, sunt îndepărtate şi particule mai mici decât dimensiunea porilor, se face şi o clarificare a soluţiei.
Eficacitatea sterilizantă a filtrării, respectiv adsorbţia este influenţată de caracteristicile soluţiei: pH; forţa ionică, polaritate, prezenta substanţelor tensioactive ce intră în competiţie cu particulele de adsorbit.
Pentru eficienţă, porii filtrelor trebuie să fie foarte mici, dar în acest caz traversarea filtrului de soluţie se face încet. Pentru reducerea timpului de filtrare se aplică filtrarea sub presiune (exercitată deasupra soluţiei), sau filtrarea în vid (în vasul de culegere) deci folosind presiunea.
Tipuri de filtre sterilizante
1.Filtrele ceramice: de porţelan poros, caolin sau kieselgur sunt cele mai vechi. Au o formă cilindrică şi sunt numite bujii filtrante. Au fost concepute de Chamberland, Pasteur, Berkefeld şi sunt cunoscute sub numele inventatorilor.
Filtrarea se face de la exterior spre interior folosind vid; sau din interior spre exterior,folosind presiune.
Bujiurile filtrante au dimensiunea porilor: 0,6 - 3,5 µm, şi reţinerea microorganismelor se face prin adsorbţie.
După folosire, trebuiesc curăţate şi regenerate prin calcinare. Aceste filtre nu reţin microorganismele, fiind folosite mai mult pentru prefiltrare - clarificare, urmată de filtrare sterilizantă, cu filtre cu pori mult mai mici.
2.Filtre de sticla sinterizată (fritată), se obţin prin sudarea la topire a particulelor de sticlă neutră, deci sunt constituite dintr-o reţea poroasă rigidă. Au formă de discuri, care se aplică pe pâlnii de forme şi dimensiuni corespunzătoare.
Porii filtrelor variază ca dimensiune. Denumirile comerciale sunt: Schott, Jena şi sunt notate cu diverse litere însoţite de cifre: G0 - G7, M, F.
Pentru filtrarea sterilizantă se foloseşte filtrul G5, cu dimensiunea porilor de
1,5 µm.
Dezavantajele acestor filtre: sunt subţiri, fragile, scumpe. Filtrul G5 pentru a nu se sparge se aşează deasupra filtrului G3 (deci sub placa de G5 se aşează filtrul G3, care are dimensiunea porilor 15-40 µm) şi se numeşte filtrul G5/3.
Avantajul acestor filtre constă în faptul că au o mare inerţie chimică; filtrarea se face sub vid.
Curăţirea lor se face prin tratament chimic cu un amestec de H2SO4/KNO3.
3. Filtre de azbest şi celuloză - filtre Seitz. Sunt pl ăci aglomerate, absorbante, obţinute prin comprimare din azbest şi celuloză. Au porozitate mică de 1 µm sau mai puţin. Au o mare suprafaţă specifică, au putere adsorbantă, plăcile sau discurile sunt fixate pe un suport pâlnie cu fund mobil, din oţe1 inoxidabil.
117

Filtrarea se realizează cu ajutorul vidului. Denumirea comercială: EK, EKS I, EKS II, care indică mărimea porilor.
Dezavantaj - pot ceda din fibrele de azbest în soluţia filtrată; au acţiune cancerigenă.
4. Filtrele cu membrană sunt cele mai utilizate sisteme de filtrare. Sunt adevăratele filtre sterilizante, constituite pe bază de esteri ai celulozei (acetat sau nitrat) asociaţi cu polimeri sintetici - clorura de polivinil; naylon; clorură de poliviliden.
Se prezintă sub formă de discuri, subţiri; sunt foarte scumpe, fiind alcătuite dintr-o peliculă foarte fină de film, care prezintă pori cilindrici sau rectangulari, perpendiculari pe suprafaţă şi dimensiuni egale.
Fiecare cm2 conţine milioane de pori ce ocupă aproximativ 80% din volumul total al membranei (au randament de filtrare foarte mare). Au o gamă largă de porozitate, de 14 - 0,022 µm.
Pentru filtrarea sterilizantă să fie de 0,22 µm.
Grosimea membranei este de 150 µm (deci foarte subţiri).
Aceste filtre pot fi sterilizate la autoclav la 1200C timp de 30 minute. Se aplică pe suporturi rezistente fie din metal, sau din sticlă sinterizată sau material plastic. Pentru a se evita colmatarea se face o prefiltrare, prin filtru cu pori de dimensiuni mai mari. Aceste membrane acţionează în special prin cernere, având porozitate mare
(numărul de pori foarte mare) viteza de filtrare este mare, iar tendinţa de adsorbţie este minimă; deci pericolul ca microorganismele reţinute să se dezvolte în interiorul filtrului este minim. Denumirea comercială este - Filtre Millipore, filtre Sartorius, filtre Szigmondi, filtre Gelman.
Filtrarea sterilizantă se face sub vid.
Nu influenţează soluţia - nu cedează particule şi au o mare varietate de porozităţi.
Asupra lor se efectuează un control pentru a studia porozitatea şi debitul de filtrare. Se poate verifica eficacitatea filtrării cu o suspensie de microorganisme, după însămânţare pe medii de cultură corespunzătoare.
Fig.nr.14. Mecanismul de filtrare sterilizantă prin reţinerea la suprafaţa filtrului a microorganismelor cu dimensiuni mai mari decât porii
118
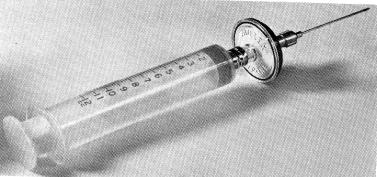
Fig.nr.15. Seringă cu filtru Millex (Millipore) adaptată cu ac hipodermic
Filtrarea sterilizantă este asociată cu înfiolarea aseptică a soluţiei în fiole sau flacoane, în paralel sterilizate. Pentru a asigura asepsia, tot materialul trebuie în prealabil sterilizat, se recomandă ca soluţia supusă sterilizării să fie săracă în microorganisme, materiale prime să fie pe cât posibil sterile sau cât mai puţin contaminate). Se asociază cu adaos de bacteriostatic. Trebuie să se asigure un debit regulat de filtrare, evitându-se suprapresiunea şi o durata mare de filtrare.
Proprietăţile sterilizante trebuiesc controlate pe toată durata filtrării. Filtrele reutilizabile trebuiesc controlate, pentru că în timp, porozitatea se poate modifica.
Sterilizarea cu gaze este o metoda chimica de sterilizare; prevăzută în F.R.
X. Se aplică pentru sterilizarea diferitelor materiale în condiţii bine determinate de temperatură, durată, umiditate şi concentraţie în gaz sterilizant. Nu există un gaz sterilizant, care să aibă proprietăţi sterilizante optime adică să distrugă rapid toate microorganismele şi să fie lipsit de toxicitate. Dintre gazele utilizate în acest scop folosim:
Oxidul de etilen este cel mai folosit, fiind inscris în FR X. Este utilizat pentru sterilizarea materialelor medico-chirurgicale care nu suportă sterilizare la autoclav, din mase plastice sau unele cauciucuri. Ca şi radiaţiile ionizante, oxidul de etilen este folosit pentru sterilizarea produselor şi articolelor introduse în ambalajul definitiv; pentru sterilizarea soluţiilor perfuzabile condiţionate în saci sau recipiente din material plastic.
Manipularea lui este periculoasă, necesită un personal calificat.
Proprietăţi: este un gaz cu punct de fierbere l0,70C şi punct de îngheţare p.c. = 1110C; este un gaz dens (ρ=1,52) foarte solubil în apă şi solvenţi organici. Dă amestecuri explozive, cu multe gaze; astfel în amestec cu aerul, în proporţie de 3-
83% dă amestec exploziv. Pentru a diminua caracterul exploziv, se amestecă cu CO2 sau freon.
Oxidul de etilen acţionează asupra microorganismelor prin alchilare, cele mai reacţionabile grupe fiind: - SH, - OH, - COOH, - NH2. aceste grupe pot fi înlocuite cu grupări hidroxietil, interferând activitatea metabolică a microorganismelor.
Rezistenţa sporilor faţă de oxidul de etilen este cu puţin mai mare decât a formelor vegetative (de maxim 5 ori mai rezistente).
119
Eficacitatea sterilizării cu oxid de etilen, depinde de factori mai uşor sau mai greu de controlat: numărul şi natura germenilor de distrus, concentraţia în gaz, temperatura la care are loc sterilizarea, 600C fiind temperatura optimă, durata tratamentului, natura materialului de sterilizat, presiunea parţială în incintă şi umiditatea atmosferică (randamentul maxim de sterilizare, la umiditate relativă 2833% în incinta de sterilizare).
Foarte importantă este eliminarea gazului din materialul sterilizat. Uşurinţa în cazul îndepărtării oxidului de etilen rezidual, depinde de natura materialului de sterilizat. Se elimină rapid din articole din bumbac – ţesături, mai greu din polietilenă, greu din policlorura de vinil, siliconi sau cauciucuri.
Desorbţia la temperatură ordinară durează zile întregi, depăşind uneori 15 zile. Pentru a grăbi desorbţia se foloseşte acţiunea conjugată a căldurii cu vidul.
Alte dezavantaje - pericol de explozie; materialul manipulat imediat după sterilizare, fără precauţii, dă dermatite; poate da produşi toxici, astfel împreună cu Cl2 dă etilenclorhidrina, urmele de oxid de etilen din material în contact cu ţesuturile, determină modificări ca hemoliza.
Pentru pulberi precauţii deosebite.
Aparatele sunt dispozitive cu închidere etanşă, rezistente la presiune cu sisteme de vid şi valve ce realizează introducerea gazului aflat în butelii, în stare lichidă, introdus în incintă, prin aceste valve.
Eficacitatea sterilizării se testează cu culturi de bacterii Bacilus stearotarmophilus sau Bacilus subtillis, introduse în aparat.
Dacă microorganismele sunt acoperite cu substanţe cristalizate, nu sunt omorâte, pentru că oxidul de etilen nu are putere de penetrare prin cristale.
Alte gaze utilizate pentru distrugerea microorganismelor sunt:
Formaldehida în stare pură, se află în stare gazoasă la temperatura camerei, având p.f. = 190C. Are proprietatea de a polimeriza rapid la o temperatură sub 800C pentru a forma o masă solidă albă – paraformaldehida. Pentru sterilizare se poate folosi fie ca paraformaldehidă încălzită la temperatura de 560C, soluţie apoasă 37% - formalina, care are şi 10% metanol pentru a preveni polimerizarea.
Este o molecula foarte reactivă, ca şi oxidul de etilen, existând o mică diferenţă între sensibilitatea formelor vegetative şi a sporilor. Este bactericid de suprafaţă, nu are putere de penetrare. Când se absoarbe în interior este greu de
îndepărtat. Este foarte reactivă în mediu umed folosit numai pentru sterilizarea materialelor mari şi a aparatului. Sterilizarea se face în anumite condiţii de concentraţie de gaz, pe unitate de suprafaţă, umiditate, timp de contact. După sterilizare, încăperile să se ventileze cu aer sterilizat, îndepărtând formaldehida, care este foarte iritantă, toxică, atacând ochii, nasul şi traheea.
Acţionează asupra microorganismelor ca agent mutagenic şi agent de alchilare.
Proteina |
|
NH +CH O |
|
Proteina |
|
NH |
|
CH OH |
||
|
|
|||||||||
2 |
2 |
|
metilolamina |
2 |
||||||
|
|
|
|
|
|
|||||
120
