
Захв_пародонта_Данилевський
.PDF
Рис. 115. Ортопантомограмма челюстей
рентгенографию каждой челюсти производят раздельно, при этом на каждом снимке получается изображение всей челюсти с полным зубным рядом. На снимке верхней челюсти получается изображение верхнечелюстных пазух, частично полости носа и скуловых костей.
Ортопантомография (панорамная томография) позволяет получить изображение обеих челюстей на одной пленке. Исследование проводится на ортопантомографе. Рентгеновскую трубку и кассету с пленкой, имеющей форму полуцилиндра, располагают на противоположных концах одной оси строго напротив. Рентгеновская трубка и пленка, вращаясь, описывают концентрическую неполную окружность вокруг головы больного, которая фиксирована неподвижно. Кассета с пленкой, вращаясь вокруг головы больного, перемещается и вокруг своей оси, при этом рентгеновское излучение последовательно засвечивает различные отделы челюстей и фиксирует их на пленке. Рентгеновской трубке можно придать вращение вокруг трех осей, что позволяет обеспечить перпендикулярное и орторадиальное направления лучей по отношению к снимаемой области.
Панорамная томография позволяет одномоментно получить изображение всей зубочелюстной системы как единого функционального комплекса (рис. 115). Недостатком метода является недостаточно четкое изображение структуры костной ткани, преимущественно в области передних зубов.
В последнее время все большее распространение получают дентальные рентгеновские аппараты, присоединенные к компьютеру. Они позволяют получать изображение зубов и челюстей как на специальной рентгеновской
Рис. 116. Рентгенограмма, обработанная при помощи компьютера
Рис. 117. ЭхоостеометрЭОМ-01ц
пленке, так и с помощью специальных датчиков, а также в десятки или даже сотни раз уменьшить лучевую нагрузку (дозу облучения), которой подвергается пациент при проведении рентгенографического исследования. В дальнейшем изображение обрабатывают с помощью специальной программы в компьютере и выводят на экран монитора. С помощью компьютера рентгеновское
98 |
99 |
|
изображение может быть тщательно проанализировано, его можно увеличить, выделив любой нужный участок. При необходимости изображению можно придать объемность, изменить цвет, провести цифровой анализ плотности изображения и т.п. (рис.116). Полученные данные заносятся компьютером в историю больного и могут храниться неограниченно долго, что очень удобно при следующих посещениях пациента и позволяет объективно проследить динамику патологического процесса.
Электрорентгенография дает возможность получить на обычной бумаге рентгеновское изображение исследуемого объекта. Для этого с помощью специального приспособления к рентгеновскому аппарату получают скрытое изображение исследуемого объекта на электрически заряженной пластинке. Рентгеновское излучение во время экспозиции разрушает заряд пластинки в зависимости от степени плотности структуры объекта. В результате получается скрытое электростатическое изображение, которое после опыления специальным порошком проявляется и переносится на бумагу. На электрорентгенограмме остается контрастное изображение структуры кости и мягких тканей, что представляет определенную ценность для клиники и экономически выгодно.
Эхоостеометрия позволяет количественно оценить состояние костной ткани челюстей при помощи эхоостеометра ЭОМ-ОШ. Передающие и принимающие эхосигналы датчики для лучшего контакта предварительно смазывают
• вазелином и плотно прижимают к слизистой оболочке или коже в области исследуемого участка кости. При заболеваниях пародонта наблюдается увеличение времени распространения ультразвуковой волны, что и регистрируется аппаратом. Данный метод можно использовать для дополнения рентгенологического исследования, при массовых обследованиях организованных контингентов населения он может заменить рентгенографию (рис. 117).
ЛАБОРАТОРНЫЕ МЕТОДЫ ДИАГНОСТИКИ
ЦИТОЛОГИЧЕСКИЕ МЕТОДЫ
Цитологический метод используют для исследования содержимого пародонтальных карманов и других очагов поражения пародонта. Содержимое изучают по методике П.М.Покровской и М.С.Макаровой (1942) в модификации И.А.Бенюмовой (1962). Пародонтальные карманы предварительно промывают изотоническим раствором хлорида натрия, стерильной иглой с турундой производят забор материала и переносят его на предметное стекло. Препарат фиксируют смесью Никифорова и окрашивают по Граму и Гимзе—Романовскому.
Микроскопически изучают клеточный состав экссудата, оценка которого позволяет получить представление о защитной реакции тканей пародонта (наличие или отсутствие фагоцитоза, незавершенный фагоцитоз). Определяют качественное состояние и количество нейтрофилов, стадию их дистрофии. Обращают внимание на состояние других клеточных элементов: лимфоцитов, полибластов, эпителиальных и плазматических клеток.
Эксфолиативная цитология позволяет вести динамические наблюдения за течением заболевания, так как степень кератинизации слизистой оболочки характеризует ее барьерную функцию. Материал для цитологического исследования берут с поверхности межзубных сосочков при помощи резиновых полосок или кубиков и переносят на предметное стекло. Окраска маз- ков-отпечатков определяется целью исследования. Для общего обзора мазки окрашивают по методу Романовского—Гимзы. Под микроскопом с помощью иммерсионной системы изучают качественный и количественный состав клеточных элементов крови, эпителиальных клеток. Гистохимические методы исследования позволяют уточнить состояние различных видов обмена веществ в клетках. Для определения индекса кератинизации подсчитывают общее количество эпителиальных клеток в поле зрения микроскопа, затем число обнаруженных ороговевших клеток умножают на 100 и делят на общее количество. Иногда индекс кератинизации высчитывают отдельно для слизистой оболочки каждой челюсти. Уменьшение степени кератинизации свидетельствует о снижении защитной функции.
Ротовая цитодиагностика основана на данных о циклических изменениях многослойного плоского эпителия полости рта синхронно с менструальным циклом. Материал для исследования берут со слизистой оболочки щеки выше линии смыкания зубов — это место, благодаря минимальному травмированию, наиболее удачное для такого исследования. Различают четыре степени эстрогенной насыщенности (М.Г.Синица, 1992):
I степень — резкая недостаточность эстрогенов (в мазках обнаруживают атрофические клетки);
II степень — средняя степень дефицита эстрогенов (мазки состоят преимущественно из парабазальных клеток с крупными ядрами);
III степень — умеренное снижение эстрогенов. В мазках встречаются промежуточные клетки с ядрами средней величины, единичные парабазальные и поверхностные клетки;
IV степень характерна для хорошей эстрогенной насыщенности (в мазках преобладают поверхностные клетки). Достоверное заключение о функциональной активности яичников можно получить при биохимических исследованиях гормонального статуса.
Реакция адсорбции микроорганизмов - РАМ (Н.Ф.Данилевский, А.П.Самойлов, Т.А.Беленчук, 1985; Т.А.Беленчук, 1985) клетками эпителия слизистой оболочки рта может быть применена для комплексного обследования больных, определения эффективности предпринятых лечебных мероприятий, при заболеваниях пародонта и слизистой оболочки полости рта (рис. 118). Путем соскоба берут мазок со здорового участка слизистой оболочки альвеолярной части десны и окрашивают по Романовскому, Лейшману или Паппенгейму. В окрашенных мазках изучают взаимоотношение микрофлоры полости рта с эпителиальными клетками слизистой оболочки. Флора полости рта в основном представлена кокками. Подсчитывают количество кокков, адсорбированных на поверхности эпителиальных клеток, и последние делят на 4 группы:
100 |
101 |
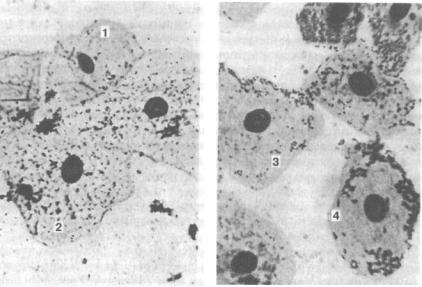
Рис. 118. Реакция адсорбции микроорганизмов (РАМ) эпителиальными клетками разных групп, х 200:
I— 1-й группы; 2 — 4-й группы; 3 — 2-й группы: 4 — 3-й группы
1)эпителиальные клетки, на поверхности которых нет адсорбированных микроорганизмов или встречаются единичные кокки;
2)адсорбция эпителиальной клеткой от 5 до 25 кокков;
3)эпителиальные клетки, имеющие на своей поверхности 26—50 кокков;
4)адсорбция 51 и более кокков на поверхности клеток типа муравейника. Расчет производится на 100 эпителиальных клетках. Клетки 1 -й и 2-й групп
относят к группе клеток с отрицательной РАМ, 3—4-й — с положительной РАМ. При микроскопии в каждом мазке выводят процент клеток с положительной и отрицательной РАМ. По проценту положительной РАМ судят о неспецифической резистентности организма: при РАМ 70% и выше функциональное состояние организма хорошее, 31—69% — удовлетворительное, 30% и ниже — неудовлетворительное.
Метод последовательных полосканий - миграция лейкоцитов
вполость рта (М.А.Ясиновский, 1931) позволяет судить о защитных реакциях тканей пародонта, степени фагоцитоза, характере воспалительной реакции. Подсчитывают количество мигрировавших в полость рта лейкоцитов
вединице объема смывной жидкости. Для полоскания рта используют 10 мл изотонического раствора хлорида натрия. Длительность полоскания — 30 с. Промежутки между полосканиями 5 мин. Первые 3 порции выплевывают, 3 следующие собирают в пробирки для исследования. Пробирки закрывают,
взбалтывают содержимое. Пипеткой отмеряют 1 мл смыва, переносят в другую пробирку, делают разведение в 9 раз. Тщательно взбалтывают, подкрашивают 1 % водным раствором трипанового синего и 1 % водным раствором конго красного (по 1 капле). Пипеткой заполняют камеру для подсчета. Через 5—10 мин после оседания лейкоцитов проводят подсчет в 30 полях зрения. Камера представляет собой предметное стекло, на которое наклеено второе толщиной 1 мм с отверстием в центре. Для работы используют окуляр с ограниченным полем зрения, равным 45 квадратикам по камере Горяева.
Подсчитывают в 10 полях зрения количество живых, мертвых лейкоцитов
иклеток плоского эпителия. Затем производят расчеты:
1)среднее число лейкоцитов в 1 поле зрения (живых и мертвых отдельно)
иклеток плоского эпителия;
2)среднее число лейкоцитов в 1 поле зрения (живых и мертвых отдельно)
иклеток плоского эпителия умножают на 400 и на разведение и делят на 45. Полученное число показывает количество мигрировавших лейкоцитов в 1 мл смывной жидкости по Ясиновскому.
Для суждения о качественном составе клеточных элементов смыва готовят мазки из осадка, которые фиксируют в этиловом спирте и окрашивают по Ро- мановскому—Гимзе. Затем в мазках проводят дифференцированный подсчет
относительного количества неизмененных нейтрофилов и находящихся в стадии дистрофии. Учитывают количество фагоцитов и лимфоцитов. Дифференцируют эпителиальные клетки по степени зрелости. Определяют количество ороговевших, промежуточных и парабазальных клеток. Степень ороговения устанавливают по клеточной морфологии в дополнение к реакциям окрашивания. Всего подсчитывают 100 клеток и выводят их процентное содержание. В норме 80% мигрировавших в полость рта жизнеспособных лейкоцитов сохраняют подвижность и функцию фагоцитоза в течение 2,5 ч. По интенсивности миграции лейкоцитов и десквамации можно судить о реактивности слизистой оболочки рта, степени тяжести патологического процесса.
Этот метод объективно оценивает результаты различных способов лечения заболеваний пародонта.
Гемограмма — совокупность качественного и количественного исследования крови. Для подсчета гемограммы мазки готовят по обычной методике. В морфологической картине периферической крови определяют отклонения от нормы: уменьшение числа эритроцитов, снижение уровня гемоглобина, сдвиг лейкоцитарной формулы, увеличение СОЭ и др.
Моноцитограмма (О.П.Григорова, 1958) — это тест функционального состояния активности мезенхимы, который определяют путем дифференцированного подсчета и определения процентного соотношения различных форм (юных и старых) моноцитов в периферической крови. В норме процентное соотношение различных групп моноцитов следующее: промоноцитов 20—23%, собственно моноцитов 26-32%, полиморфноядерных 42-62%, полинуклеаров0,1%.
102 |
1 |
0 |
3 |
МИКРОБИОЛОГИЧЕСКИЕ МЕТОДЫ
Микробиологическое исследование позволяет установить состав микрофлоры в поверхностной и глубоких зонах пародонтального кармана, провести дифференциацию ее, что важно для диагностики и дальнейшего выбора медикаментозных средств лечения. Забор материала и окраска его для микробиологического исследования такие же, как для цитологического (рис. 119).
Для определения микробного числа используют промывную жидкость (первые две порции), собранную для исследования интенсивности миграции лейкоцитов и десквамации эпителия. Готовят 6 разведений исследуемой жидкости: 10,102,103,104,105,106. Из 4 последних разведений берут по 1 мл для
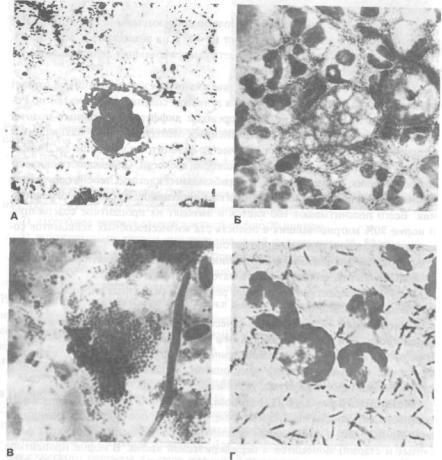
Рис. 119. Микрофлора пародонтальных карманов, х 90:
А - кокки; Б - простейшие; В - грибы; Г - фузобактерии и спирохеты
посева на агаре и выращивания в термостате при температуре 37 °С в течение 24—36 ч. Затем производят подсчет абсолютного числа микробных тел в 1 мл промывной жидкости.
Показатель обсемененности пародонтального кармана микроорганизмами отражает характер течения дистрофически-воспалительного процесса и эффективность лечения. Забор материала производят стерильной ватной турундой на глубине 2 мм. Затем концевую часть турунды промывают 10 мл изотонического раствора хлорида натрия и получают взвесь микроорганизмов. Посев культуры проводят в чашке Петри на мясопептонный агар, добавляя 1 мл взвеси культуры микроорганизмов, разведенной в 100 раз, затем помешают в термостат при температуре 37 °С на 48 ч, после чего подсчитывают количество колоний на поверхности и в толще агара.
У больных с хроническим и обострившимся течением заболеваний пародонта эти показатели коррелируют с характером течения: при хроническом они составляют до лечения примерно 36 колоний на 1 см2 поверхности агара; при обострившемся течении — в 10 раз больше. После проведенного курса лечения их содержание не превышает 1—2 колоний на 1 см2.
Исследование десневой жидкости цитологическими, гистохимическими, микробиологическими, иммунологическими методами способствует уточнению диагноза и динамическому контролю за эффективностью проводимого лечения. Ее собирают с помощью трубочек или фильтровальной бумаги, которую продвигают под десну на 1 мм и держат 3—5 мин. Материал для цитологического или микробиологического исследования берут с помошью платиновой петли и переносят на предметное стекло или питательную среду. Благодаря иммунологическим свойствам и фагоцитарной активности клеточных элементов десневая жидкость составляет важную часть защитного механизма тканей пародонта. В десневой жидкости могут быть обнаружены клетки эпителия борозды, бактерии, лейкоциты, лимфоциты, моноциты, тканевые базофилы, электролиты, глюкоза, мочевина, бактериальные эндотоксины, ферменты, иммунные тела и др.
БИОХИМИЧЕСКИЕ И ИММУНОЛОГИЧЕСКИЕ МЕТОДЫ
Биохимические методы. Для ранней диагностики болезней пародонта в последние годы используют определение в сыворотке крови и слюне содержания нейраминовой кислоты, фукозы, оксипролина в моче, содержание ферментов и их ингибиторов в сыворотке крови и слюне. Сравнительная оценка этих цифровых показателей до и после лечения рассматривается как тест эффективности лечения.
Содержание витамина Ев крови в определенной мере отражает содержание токоферола в организме. Его определение показано у подростков при физиологическом и особенно патологическом половом созревании. Концентрация токоферола при генерализованном пародонтите у подростков при физиологическом половом созревании (Н.Ф.Данилевский, Г.Н.Вишняк, А.М.Политун, 1981) составляет 0,67 мг% ± 0,01 мг%, что по сравнению с контрольными данными (0,89 мг% ± 0,05 мг%) свидетельствует о его дефиците.
104 |
105 |
|
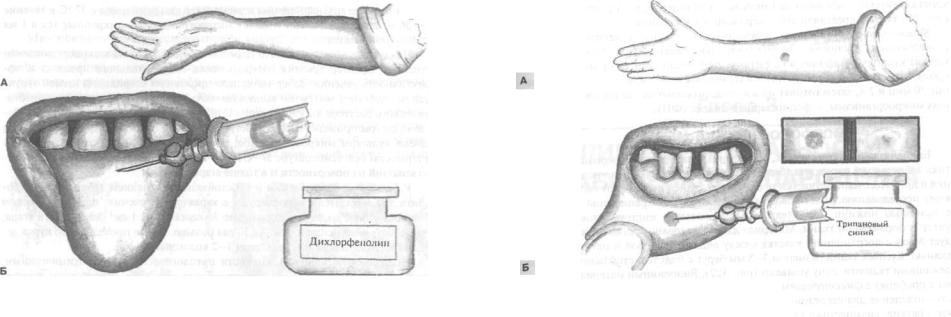
Рис. 120. Определение насыщенности тканей аскорбиновой кислотой:
А.— внутрикожная проба; Б — языковая проба
Насыщение тканей аскорбиновой кислотой уменьшает проницаемость капилляров, стимулирует функциональную деятельность органов и тканей, оказывает положительное влияние на обмен коллагена и др. Для определения тканевой насыщенности витамином С на слизистую оболочку спинки языка инъекционной иглой наносят каплю индикатора (0,06% раствор натриевой соли 2,6-дихлорфенолиндофенола), который восстанавливается аскорбиновой кислотой при комнатной температуре, — индикатор обесцвечивается. Время обесцвечивания раствора определяется в секундах. При анализе результатов языковой пробы следует учитывать сезонные колебания содержания в тканях аскорбиновой кислоты (рис.120).
Радиоизотопноеисследованиеприменяетсядляизученияобменныхпроцессов в тканях пародонта. Используются меченые вещества, активно участвующие в метаболизме (24Na, 45Ca, 3 2 Р и др.), что позволяет диагностировать ранние патологические нарушения в тканях пародонта и оценить эффективность различных методов лечения.
Иммунологические методы. Неспецифическая резистентность организма снижается соответственно степени тяжести патологического процесса в пародонте: угнетена функциональная активность соединительной ткани, снижены титр лизоцима, фагоцитарная активность лейкоцитов, комплементарная активность сыворотки крови, активность макрофагов; повышена повреждаемость нейтрофилов, высокие показатели лейкергии или реакции агломерации лейкоцитов (РАЛ). При заболеваниях пародонта увеличивается титр противодесневых аутоантител, количество тканевых базофилов, повышается митотическая активность клеточных элементов меж-
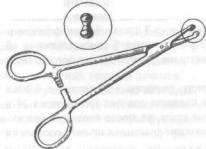
Рис. 121. Проба Кавецкого:
А - внутрикожная проба; Б - внутрислизистая проба
альвеолярных сосочков и др. Неспецифическими тестами аллергологического статуса организма являются также эозинофилия в периферической крови и тканях патологического очага десны, тромбопения, лейкопения, агранулоцитоз, изменение протеинограммы, реакция адсорбции микроорганизмов.
Кожная проба по Р.Е.Кавецкому в модификации С.М.Базарновой помогает
определить функциональное состояние соединительной ткани. Проба основана на способности ткани задерживать индифферентные красители. В слизистую оболочку нижней губы вводят 0,1 мл 0,25% раствора трипанового синего. О распространении краски судят по размеру пятна. Его диаметр измеряют сразу после инъекции и спустя 3 ч. Отношение квадрата радиуса пятна в момент введения краски к квадрату его радиуса через 3 ч является коэффициентом пробы. В норме он равен от 5 до 7. Значение ниже 5 свидетельствует об угнетении, выше — об активности функционального состояния системы соединительной ткани организма.
При внутрикожном введении указанного раствора в количестве 0,2 мл коэффициент вычисляют как отношение квадрата радиуса пятна через 24 ч после инъекции краски к квадрату радиуса сразу же после введения краски. При патологии пародонта наблюдается угнетение функционального состояния системы соединительной ткани (рис. 121).
Определениеуровнялизоцимавслюне(методЛоури)основаннаспособности лизоцима слюны расщеплять полисахариды клеточной оболочки бактерий. Активность фермента определяется нефелометрически по изменению мутности суспензии Micrococcus lysodectius и выражается в микрограммах
106 |
107 |
|
кристаллического лизоцима на 1 мг белка за 30 мин инкубации при температуре 37 °С; также определяют его содержание в 1 мл слюны.
Фагоцитарная активность лейкоцитов характеризует неспецифическую резистентность организма. Двухмиллиардную взвесь убитой нагреванием суточной культуры стафилококка (штамм 209) смешивают с 0,1 мл цитратной крови больного. Смесь инкубируют в термостате при температуре 37° С в течение 30 мин и 2 ч, затем готовят мазки, подсчитывают число клеток, поглотивших микроорганизмы, — фагоцитарный индекс (ФИ).
МОРФОЛОГИЧЕСКИЕ МЕТОДЫ
Биопсию проводят в случаях, если затруднена дифференциальная диагностика заболеваний пародонта (болезни крови, злокачественные новообразования и др.). Иссеченные участки пораженных тканей подвергают гистологическому исследованию. Под проводниковой или инфильтрационной анестезией с помощью ножниц, скальпеля или специальных инструментов иссекают участок пораженной ткани. Материал для исследования по возможности следует брать с пограничного участка между видимо здоровой и патологической тканью. Кусочек ткани размером 3—5 мм берут с подслизистой основой и подлежащими тканями, рану ушивают (рис. 122). Биопсийный материал помешают в пробирку с фиксирующим раствором и направляют в патологоанатомическое отделение для исследования. В сопроводительном направлении указывают краткие анамнестические данные, данные объективного исследования и предполагаемый диагноз.
Морфологические изменения при болезнях пародонта разнообразны и выявляются во всех тканях пародонта. Преимущественно наблюдаются дистро- фически-воспалительные и воспалительные процессы. При гингивите преобладают воспалительные изменения, при пародонтите — дистрофически-воспа- лительные, а при пародонтозе — дистрофические. При воспалительных процессах превалируют гиперемия, отек, лейкоцитарная или мелкоклеточная лимфоидная инфильтрация, накопление размножающихся соединительнотканных клеток, преимущественно лимфоцитов, фибробластов, плазматичес-
ких клеток, и формирование зрелой
Рис. 122. Инструмент для забора биоптатов слизистой оболочки
соединительной ткани, макрофагальная или остеокластическая резорбция альвеолярной кости.
Дистрофические изменения в эпителии проявляются нарушением ороговения, вакуольной и баллонирующей дистрофией клеток. В соединительной ткани и сосудах наблюдаются мукоидное набухание, фибриноидные изменения, фрагментация и глыбчато-зернистый распад волокон, гиалиноз и склероз, в костной ткани — остеопороз и остеосклероз.
Глава 3
КЛИНИКА И ДИАГНОСТИКА ЗАБОЛЕВАНИЙ ПАРОДОНТА
КЛАССИФИКАЦИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА
Болезни пародонта по происхождению, механизму развития, клиническому течению довольно разнообразны. Одни заболевания протекают преимущественно с проявлением хронического или острого и подострого воспаления, для других присущи дистрофические изменения. В пародонте могут развиваться глубокие воспалительные, деструктивные и дистрофические процессы одновременно, а также заболевания, которые носят опухолевый или опухолеподобный характер. Такое разнообразие форм и характера течения обусловило создание классификации болезней пародонта.
К настоящему времени в специальной литературе описано большое количество классификаций, в которых сделана попытка отразить этиологические, патогенетические или клинические принципы. Эти классификации отличались терминологией, различием взглядов на происхождение заболеваний.
Первую попытку создания единой классификации в ЗО-е годы XX в. предприняла Международная организация по изучению болезней пародонта (ARPA). Классификация пародонтопатий (ARPA) была основана на принципе выделения основных характерных патологических процессов — воспалительных, дистрофических и опухолевых и выглядела следующим образом:
I. Воспалительные пародонтопатий:
а) поверхностная воспалительная пародонтопатия (гингивит); б) глубокая воспалительная пародонтопатия (пародонтит).
II. Дистрофическая пародонтопатия (пародонтоз).
III. Смешанная пародонтопатия (дистрофический пародонтит, воспалительный пародонтоз).
IV. Идиопатический внутренний пародонтоз (десмодонтоз, юношеский пародонтоз).
V. Неопластическая пародонтопатия (пародонтома).
Данная классификация правильно объединяла основные поражения тканей пародонта, однако сам термин «пародонтопатия» был больше собирательным и не всегда отображал патогенетическую суть заболеваний.
Близка к классификации ARPA систематика заболеваний пародонта ВОЗ (1973):
I.Воспалительные процессы.
1.Гингивит: а) острый; б) хронический (простой, гипертрофический, язвенный, десквамативный).
2.Атрофия десны: а) генерализованная; б) локализованная.
3.Хронический пародонтит: а) простой; б) сложный.
II. Дегенеративные процессы. Периодонтоз.
111. Неопластические процессы. 1.Фиброматоз.
2.Локализованная гипертрофия десны.
В40—50-е годы широко пользовались классификациями, разработанными А.И.Евдокимовым, И.Г.Лукомским, И.О.Новиком, Е.Е.Платоновым, Я.С.Пеккером, классификацией ММСИ и др. Располагая многочисленными собственными наблюдениями, Н.Ф.Данилевский и Г.Н.Вишняк (1977) предложили собственную классификацию болезней пародонта с учетом патогенетических особенностей:
I. Воспалительные процессы в тканях пародонта (папиллит, гингивит, пародонтит).
По форме: катаральные, язвенные, гипертрофические и атрофические.
По глубине:
а) поражение мягких тканей пародонта; б) поражение мягких тканей и альвеолярной кости.
По локализации: ограниченный или диффузный процесс. 1Ь Дистрофические процессы в тканях пародонта.
Пародонтоз — генерализованная сосудисто-нервная дистрофия тканей пародонта:
а) дистрофическая форма; б) дистрофически-воспалительная форма.
III. Дистрофически-воспалительные процессы в тканях пародонта при заболеваниях внутренних органов и костной системы:
а) при заболеваниях органов кроветворения: лейкоз, агранулоцитоз, ретикулогистиоцитозы (эозинофильная гранулема, болезнь Леттерера—Зиве, болезнь Хенда—Шюллера—Крисчена);
б) при врожденной патологии: болезнь Гоше, болезнь Ниманна—Пика, болезнь Папийона—Лефевра, болезнь Такахара (акаталазия), нейтропения, фиброзная остеоплазия и др.
IV. Продуктивные процессы тканей пародонта:
а) доброкачественные (фиброматоз, эпулид и др.); б) злокачественные.
Классификация позволяет определить патогенетическую сущность, клини- ко-морфологическую, нозологическую форму той или иной болезни пародонта и, исходя из этого, наметить правильную врачебную тактику.
Решением XVI пленума Всесоюзного научного общества стоматологов (1983) была утверждена классификация болезней пародонта для применения в научной, педагогической и лечебной работе. В ее основу также был положен нозологический принцип, который использует ВОЗ.
I. Гингивит — воспаление десны, обусловленное неблагоприятным воздействием местных и общих факторов и протекающее без нарушения целостности зубодесневого соединения.
Форма: катаральный, гипертрофический, язвенный. Тяжесть процесса: легкая, средняя, тяжелая.
Течение: острое, хроническое, обострившееся, ремиссия. Распространенность процесса: локализованный, генерализованный.
110 |
111 |
II. Пародонтит — воспаление тканей пародонта, характеризующееся прогрессирующей деструкцией периодонта и кости.
Тяжесть процесса: легкая, средняя, тяжелая.
Течение: острое, хроническое, обострившееся (в том числе и абсцедирующее), ремиссия.
Распространенность процесса: локализованный, генерализованный. III. Пародонтоз — дистрофическое поражение пародонта.
Тяжесть процесса: легкая, средняя, тяжелая. Течение: хроническое, ремиссия. Распространенность процесса: генерализованный.
IV. Идиопатические заболевания с прогрессирующим лизисом тканей пародонта (синдром Папийона—Лефевра, гистиоцитоз X, гаммаглобулинемия, сахарный диабет некомпенсированный и др.).
V. Пародонтомы — опухоли и опухолеподобные процессы в пародонте. Положительным в этой классификации является дифференцированный
подход к различным заболеваниям тканей пародонта в соответствии с клини- ко-морфологическими особенностями патологического процесса, в ней систематизирован весь комплекс заболеваний пародонта, использованы принятые международные термины. Вместе с тем, в данной систематике допущен ряд неточностей. Так, при определении течения генерализованного пародонтита трудно согласиться с предложением разделять его по тяжести на легкое, средней тяжести и тяжелое. Такое деление с патофизиологической точки зрения закономерно только лишь тогда, когда при развитии болезни возможна различная динамика ее течения и обратное развитие вплоть до полного выздоровления.
На самом же деле при генерализованном пародонтите наступает необратимая резорбция альвеолярной кости и добиться ее восстановления практически невозможно. Поэтому такое определение течения не отражает патогенетической сущности заболевания и более приемлима формулировка, отражающая стадию или степень прогрессирующей убыли альвеолярной кости.
Подобный подход и был отражен в предложенной классификации заболеваний пародонта (Н.Ф.Данилевский, 1994). Республиканская конференция стоматологов Украины (Одесса, 1998) рекомендовала использовать ее как рабочую классификацию в учебных и лечебных учреждениях страны.
I.ВОСПАЛИТЕЛЬНЫЕ
1.Папиллит, гингивит.
Форма: катаральный, гипертрофический, язвенный, атрофический. Течение: острое, хроническое.
Глубина поражения: мягкие ткани, остеопороз межальвеолярных перегородок.
Распространенность процесса: ограниченный, диффузный. 2. Локализованный пародонтит.
Форма: катаральный, гипертрофический, язвенный, атрофический. Течение: острое, хроническое.
Глубина поражения: мягкие ткани и альвеолярная кость.
Степень развития: начальная, I степень, II степень, III степень. Распространенность процесса: ограниченный.
II. ДИСТРОФИЧЕСКИ-ВОСПАЛИТЕЛЬНЫЕ 1. Генерализованный пародонтит.
Течение: хроническое, обострившееся, стабилизация.
Степень развития: начальная степень, I степень, II степень, III степень. Распространенность процесса: диффузное поражение пародонта.
2. Пародонтоз. Течение: хроническое.
Степень развития: начальная степень, I степень, II степень, III степень. Распространенность процесса: диффузное поражение пародонта.
III. ПРОГРЕССИРУЮЩИЕ ИДИОПАТИЧЕСКИЕ ЗАБОЛЕВАНИЯ
1.Сопровождающие заболевания крови: лейкоз, циклическая нейтропения, агранулоцитоз.
2.Гистиоцитоз X: болезнь Леттерера-Зиве, болезнь Хенда-Шюлле- ра—Крисчена, эозинофильная гранулема (болезнь Таратынова).
3.Сопровождающие нарушения обмена: болезнь Ниманна-Пика, болезнь Гоше, синдром Папийона—Лефевра.
4.При врожденных заболеваниях: болезнь Дауна, акаталазия, десмодонтоз. IV. ПРОДУКТИВНЫЕ ПРОЦЕССЫ (ПАРОДОНТОМЫ) Доброкачественные, злокачественные.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ЗАБОЛЕВАНИЙ ПАРОДОНТА
Причиной патологического процесса в тканях пародонта могут быть различные факторы как экзогенного, так и эндогенного происхождения. Несмотря на разнообразие этих факторов, воспалительный или дистрофически-вос- палительный процесс в тканях пародонта протекает довольно однотипно и в зависимости от локализации, длительности воздействия этиологических факторов проявляется различными морфологическими и патофизиологическими вариантами. Состояние физиологических защитных механизмов тканей пародонта и организма в целом определяет степень распространенности дис- трофически-воспалительного процесса и его интенсивность.
Реализация действия различных патогенных факторов осуществляется в случае, если они по силе превосходят приспособительно-защитные возможности тканей пародонта, а также при снижении реактивности организма. Условно все этиологические факторы можно разделить на общие и местные.
МЕСТНЫЕ ФАКТОРЫ
Из комплекса местных факторов, влияющих на состояние тканей пародонта, следует выделить зубные отложения, микрофлору, травматическую окклюзию, несанированную полость рта; неполноценные пломбы, протезы,
112 |
к, |
из |

ортодонтические аппараты; вредные привычки, неправильное расположение уздечек губ, языка и пр.
Зубные отложения. Среди местных повреждающих факторов, сочетающих в себе механическое, химическое и биологическое (микробы, токсины) действие, особое значение имеют отложения на зубах (рис.123). Многочисленными эпидемиологическими, биохимическими, микробиологическими исследованиями в клинике и эксперименте установлено патогенетическое значение зубного налета в возникновении воспалительных и дистрофически-воспали- тельных заболеваний пародонта.
Определяя место зубных отложений среди прочих патогенетических факторов, G.Cowley, T.Macphee (1969) считают, что на возникновение заболеваний пародонта влияют: 1) состояние и продукты обмена в зубных отложениях; 2) факторы полости рта, способные усиливать или ослаблять патогенетический потенциал микроорганизмов и продуктов их обмена; 3) общие факторы, от которых зависит ответная реакция организма на патогенные воздействия. Различают мягкие (неминерализованные) и твердые (минерализованные) зубные отложения, или зубной налет и зубной над- и поддесневой камень.
Из неминерализованных зубных отложений наиболее важное значение для возникновения поражения пародонта имеют мягкий зубной налет (белое вещество) и зубная бляшка. Белый зубной налет — это поверхностное приобретенное образование на зубах, покрывающее их пелликулу. Он представляет собой желтое или серовато-белое мягкое и липкое отложение, менее плотно прилегающее к поверхности зуба, чем зубная бляшка. Наибольшее количество зубного налета находится у шеек зубов, в межзубных промежутках, на контактных поверхностях и на щечных поверхностях коренных зубов. Налет довольно легко снимается ватным тампоном, струей воды, зубной щеткой и стирается при пережевывании твердой пищи.
В основном налет состоит из конгломерата пищевых остатков (пищевого дебриса), микроорганизмов, постоянно слущивающихся эпителиальных клеток, лейкоцитов и смеси слюнных протеинов и липидов (S.S.Socransky, 1977). Зубной налет содержит неорганические вещества — кальций, фосфор, натрий, калий, микроэлементы — железо, фтор, цинк и органические компоненты — белки, углеводы, протеолитические ферменты. Основную массу зубного налета составляют микроорганизмы: в 1 мг налета их может содержаться до нескольких миллиардов (до 2,5 х 1010). Из микроорганизмов превалируют стрептококки — 70% колоний, 15% составляют вейлонеллы и нейссерии, 15% — стафилококки, лептотрихии, фузобактерии, актиномицеты, дрожжеподобные грибы и др.
Интенсивность образования и ко- |
|
||
личество зубного налета зависят от |
|
||
многих факторов: количества и каче- |
|
||
ства пищи, вязкости слюны, харак- |
|
||
тера микрофлоры, степени очищения |
|
||
зубов, состояния тканей пародонта. |
|
||
При |
повышенном |
употреблении |
|
углеводов скорость образования на- |
|
||
лета и его количество увеличиваются. |
|
||
Разновидностью |
зубного налета |
|
|
является зубная бляшка. Это мягкое |
|
||
аморфное гранулированное образо- |
|
||
вание, |
накапливающееся на зубах, |
|
|
пломбах, протезах и др. Она плотно |
|
||
прилипает к их поверхности и отде- |
Рис.124. Схема налета и зубной |
||
ляется |
только путем механической |
бляшки |
|
очистки.
В малых количествах бляшка не видна, но когда ее скапливается много, она приобретает вид массы серого или желто-серого цвета. Бляшка образуется в равной степени на верхней и нижней челюстях, больше — на вестибулярных поверхностях боковых зубов и язычных поверхностях нижних фронтальных зубов.
Зубная бляшка состоит главным образом из воды — 70% и пролиферирующих микроорганизмов, эпителиальных клеток, лейкоцитов и макрофагов. В сухом остатке 70% составляют микроорганизмы, остальное — межклеточный матрикс. Матрикс в свою очередь состоит из комплекса гликозаминогликанов, в котором главными компонентами являются углеводы и протеины (примерно по 30% каждый), 15% липидов и продуктов жизнедеятельности бактерий бляшки, остатков их цитоплазмы и клеточной мембраны, пищи и производных слюнных гликопротеинов.
Главными неорганическими компонентами матрикса бляшки являются кальций, фосфор, магний, калий и в малых количествах натрий.
Зубная бляшка — это в основном бактериальное образование, которое характеризуется прогрессирующим ростом и довольно прочно присоединяется к твердым тканям зубов (W.Bowen, 1976). По мере роста и организации бляшки в ней возрастает количество микроорганизмов примерно до 70—80 % ее массы, в среднем составляя около 2,5 х 1010 бактерий в 1 мг. Изменяется и их видовой состав: от простого преобладания кокков (которые и в зрелой бляшке составляют до 50 % ее бактериальной флоры) до более сложных их популяций (J. Carlsson, 1967). Зрелая бляшка (рис. 124) имеет довольно организованную структуру и состоит из: 1) приобретенной пелликулы, обеспечивающей связь бляшки с эмалью; 2) слоя палисадникообразно размещенных волокнистых микроорганизмов, которые оседают на пелликулу; 3) густой сетки волокнистых микроорганизмов, в которых имеются колонии других видов микробов; 4) поверхностного слоя коккоподобных микроорганизмов (Z.Broukal,
114 |
8* |
115 |
|
|
I.Svejda, 1977). В зависимости от рас- |
||
|
положения по отношению к деснево- |
||
|
му краю |
различают |
наддесневые |
|
(коронковые и маргинальные) и под- |
||
|
десневые |
бляшки. На |
основании |
|
многочисленных исследований под- |
||
|
десневую бляшку подразделяют на 2 |
||
|
части: связанную с зубом и связан- |
||
|
ную с эпителием. Бактерии из под- |
||
|
десневой бляшки, связанной с эпите- |
||
|
лием, могут легко проникать в соеди- |
||
|
нительную ткань десны и альвеоляр- |
||
|
ной кости (R.Saglie и соавт., 1982). |
||
|
Бактерии бляшки используют пи- |
||
|
тательные вещества пищи для обра- |
||
|
зования компонентовматрикса. Наи- |
||
|
более легко используются легкоус- |
||
|
ваиваемые углеводы (сахароза, глю- |
||
|
коза), в меньшей мере — крахмал. |
||
|
Некоторые виды бактерий бляшки |
||
|
синтезируют из углеводов полисаха- |
||
Рис. 125. Схема воздействия зубной |
риды: декстраны и леваны, обладаю- |
||
бляшки надесну |
щие способностью адгезии к твердым |
||
|
тканям зубов (R.Gibbons, 1969). Ско- |
||
рость образования бляшки зависит от характера питания, гигиенического состояния полости рта, свойств слюны, но в среднем для созревания бляшки необходимо около 30 дней. По мере роста бляшка распространяется под десну, вызывая раздражение тканей пародонта, повреждение эпителия и развитие воспаления подлежащих тканей. Выделяемые микроорганизмами бляшки эндо- и экзотоксины оказывают токсическое действие на ткани пародонта, нарушают клеточный обмен, вызывают вазомоторные расстройства, сенсибилизацию тканей пародонта и организма в целом.
Микроорганизмы бляшки в результате активного выделения разнообразных ферментов (гиалуронидаза, хондроитинсульфатаза, протеазы, глкжуронидаза, коллагеназа и др.) обладают выраженной протеолитической активностью (Л.А.Хоменко, 1980). Эти ферменты способствуют развитию микроциркуляторных нарушений в пародонте, запускают ряд реакций воспаления, вызывают деполимеризацию гликозаминогликанов, белков тканей пародонта, в первую очередь коллагена. Такой механизм развития патологического процесса занимает важное место в патогенезе заболеваний пародонта воспалительной и дис- трофически-воспалительной природы (рис. 125, 126).
Со временем в зубной бляшке повышается концентрация неорганических веществ, и она становится матрицей для образования зубного камня. Фосфат кальция, преобладающий в бляшке, импрегнирует ее коллоидную основу, изменяя соотношение между гликозаминогликанами, микроорганизмами,
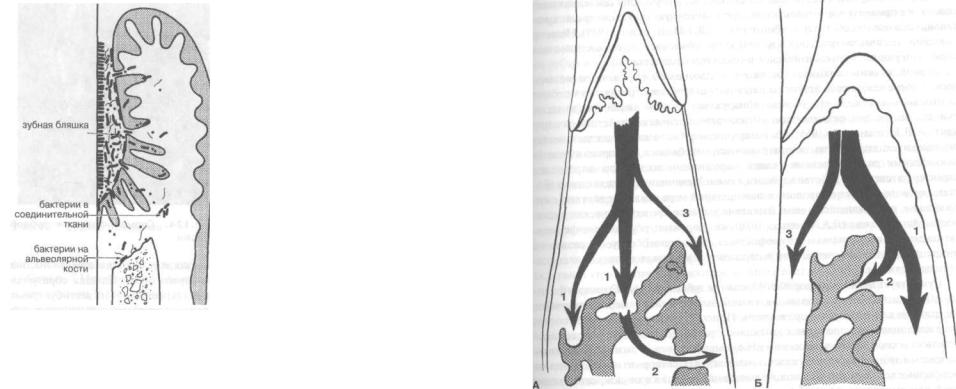
Рис. 126. Распространение воспалительного процесса в десне:
А - в межзубном промежутке; Б — с вестибулярной (язычной) стороны: I — из десны в альвеолярную кость; 2 — из кости в периодонт; 3 — из десны в периодонт
спущенным эпителием, лейкоцитами и пр. В зависимости от локализации по отношению к десневому краю различают наддесневой и поддесневой зубной камень. Минеральные компоненты (кальций, фосфор, магний, карбонаты, микроэлементы) наддесневого зубного камня слюнного происхождения, а поддесневого — из сыворотки крови. Примерно 75% из них составляет фосфат кальция, 3% карбонат кальция, остальное — фосфат магния и следы разных металлов. Чаще неорганическая часть зубного камня имеет кристаллическую структуру и представлена гидроксиапатитом и другими апатитами (H.T.Schroeder, H.U. Bambauer, 1966).
Органическую основу зубного камня составляет конгломерат протеинполисахаридного комплекса, десквамированных эпителиальных клеток, лейкоцитов и различных видов микроорганизмов. Значительную часть составляют углеводы, представленные галактозой, глюкозой, глюкуроновой кислотой, протеины и аминокислоты (M.F.Little и соавт., 1966).
117
116
