- •1. Загальні правила роботи в лабораторії
- •2. Запобіжні засоби і перша допомога при нещасних випадках
- •3. Основний лабораторний хімічний посуд
- •4. Зборка приладів
- •5. Миття і сушка хімічного посуду
- •5. Використання літератури і правила складання звіту
- •1. Нагрівання
- •2. Охолоджування
- •3. Вимірювання і регулювання температури
- •4. Подрібнення і перемішування
- •5. Розчинення і Властивості деяких органічних розчинників
- •6. Сушка і основні осушувачі
- •7. Фільтрування
- •1. Кристалізація
- •2. Возгонка (сублімація)
- •3. Екстракція
- •4. Перегонка
- •5. Хроматографія
- •1. Температура плавлення
- •2. Температура кипіння
- •3. Відносна густина
- •4. Показник заломлення
- •5. Молекулярна маса
- •1. Якісний аналіз
- •2. Фізико-хімічні методи встановлення структури речовини
- •3. Ідентифікація невідомої речовини
- •1. Відновлення воднем і реакції гідрУвання
- •2. Одержання металів, їх сплавів і деяких неметалів
- •Питомі теплові ефекти (q) відновлення оксидів алюмінієм
- •3. Одержання металів і деяких неметалів відновленням водних розчинів солей
- •4. Хлорування металів, неметалів і оксидів
- •5. Бромування металів і неметалів
- •6. Йодування металів, неметалів і оксидів
- •7. Одержання сульфідів, селенідів і телуридів
- •8. Нітрування. Одержання нітридів
- •9. Одержання карбідів
- •10. Термічне розкладання речовин з метою одержання оксидів
- •11. Зневоднення крісталогідратів
- •12. Одержання солей
- •1. НітрУвання
- •2. Нітрозування
- •3. Сульфування
- •4. Галогенування
- •5. Алкілювання
- •6. Ацилювання
- •7. ДіазоТуВаНня і Реакції діазосполук
- •8. АзоспОлуЧення
- •9. Відновлення
- •10. Окислення
- •11. Амінування
- •12. Гидроксилювання
- •13. Конденсація
- •14. Полімеризація і поліконденсація
2. Температура кипіння
Температура кипіння – це температура, при якій тиск пари рідини стає рівним зовнішньому тиску. Температура кипіння в значній мірі залежить від молекулярної маси речовини, її будови, складу, міжмолекулярної взаємодії і тиску.
Найпростіший прилад для визначення температури кипіння – це звичайний прилад для перегонки, що складається з круглодонної колби, термометра, холодильника, алонжа і приймача. В круглодонну колбу наливають до 1/4 об'єму колби рідину, температуру кипіння якої потрібно визначити. Кулька термометра знаходиться на невеликій відстані від поверхні рідини. Якщо ж визначають температуру кипіння розчину, то кульку термометра опускають в рідину. Щоб уникнути сильного перегріву рідини, для нагрівання при визначенні температури кипіння застосовують відповідні бані. Різниця температур початку і кінця кипіння для чистих речовин не повинна перевищувати 0,5 °С. Кипіння рідини в широкому інтервалі говорить про суміш рідин.
При визначенні температури кипіння слід пам'ятати про поправку на відхилення від нормального тиску. Для багатьох речовин у довідковій літературі є таблиці поправок температур кипіння при різному тиску для приведення їх до 760 мм рт. ст. Якщо ж таблиць немає, то можна обчислити поправку на відхилення від атмосферного тиску виходячи з того, що температура кипіння багатьох речовин при 760 мм рт. ст. змінюється приблизно на 3/80 зі зміною тиску на 1 мм рт. ст.
Якщо тиск А, при якому йде визначення температури кипіння, менше 760 мм рт. ст., то поправку n1 на відхилення можна обчислити з достатнім ступенем точності за рівнянням:
![]()
Якщо тиск А вище, то поправку n2 одержують з рівняння:
![]()
При роботі з малими кількостями речовини використовують метод Сиволобова. За цим методом 0,5 мл досліджуваної рідини наливають у скляну трубку діаметром ~6 мм, в яку занурюють незапаянним кінцем вниз капіляр для визначення температури плавлення. Трубку прикріплюють до термометра, як показано на рис. 61. Термометр поміщають у прилад для визначення температури плавлення. При повільному нагріванні спочатку спостерігається слабке, а потім і бурхливе виділення пухирців пари з капіляра. Температурою кипіння вважають дані термометра в той момент, коли починається бурхливе утворення пухирців. Помилки цього методу можуть складати +5°С.
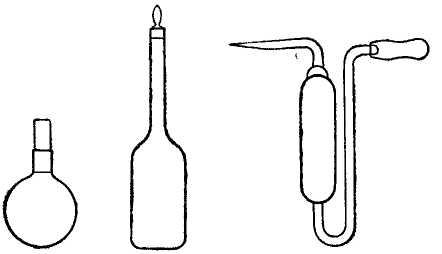
Точне визначення температури кипіння можливе за допомогою ебуліоскопів (рис. 62). Принцип їх дії оснований на тому, що рідину нагрівають зі зворотним холодильником до кипіння і вимірюють температуру; при відповідній конструкції виключаються теплові втрати і перегрів пари. Проте ці прилади вимагають, як правило, великих кількостей речовини (декілька мілілітрів).
|
|
|
|
Рис. 61. Спосіб кріплення трубки з речовиною до термометра при визначенні температури кипіння методом Сиволобова. |
Рис. 62. Ебуліоскоп. |
3. Відносна густина
Відносна густина – одна з найважливіших фізико-хімічних характеристик речовини, і її визначення є однією з найзвичайніших операцій у лабораторній практиці. Густина має велике значення для розпізнавання багатьох рідких ізомерів, характеристики сумішей, обчислення молекулярної рефракції і т.п.
Густиною речовини називають відношення маси цієї речовини до її об'єму:
![]()
де т – маса речовини; V – об'єм речовини.
Як правило, в лабораторній практиці користуються відносною густиною, яка є відношенням густини даної речовини до густини іншої речовини за певних умов. Відносну густину d речовини визначають по відношенню до густини дистильованої води:
![]()
де – густина речовини; в – густина дистильованої води при 4 °С.
Відносна густина виражається стороннім числом. Оскільки всі тіла змінюють свій об'єм залежно від температури, то ясно, що і величина густини коливатиметься в результаті зміни температури, при якій її визначають. Тому завжди приводять температуру, при якій робили визначення, і температуру води, об'єм якої був прийнятий за одиницю. Як правило, відносну густину визначають при 20 або 15°С і позначають за допомогою відповідних індексів, наприклад d415; наведене позначення вказує, що відносна густина була визначена при 15 °С і за одиницю для порівняння була взята густина води при 4°С.
Відносну густину можна визначити за допомогою ареометрів, пікнометрів, гідростатичних терезів і т.п. У найпростіших випадках для швидкого визначення відносної густини рідини застосовують так звані ареометри (рис. 63). Визначення густини за допомогою ареометрів основане на тому, що якщо тіло, занурене в рідину, не тоне, а плаває, то глибина його занурення залежить від густини даної рідини. Ареометр є скляною трубкою, що розширяється внизу і має на кінці скляну кульку, заповнену дробом або спеціальною масою, щоб під час вимірювання ареометр знаходився у вертикальному положенні. У верхній вузькій частині ареометра розміщена шкала з поділками. Чим менша відносна густина рідини, тим глибше занурюється в неї ареометр, тому на його шкалі вгорі нанесено якнайменше значення відносної густини, знизу найбільше. Іноді ареометри забезпечені термометрами (рис. 63, б), що дозволяє одночасно вимірювати температуру, при якій проводиться визначення.
|
|
|
|
Рис. 63. Ареометри: а – без термометра, б – з термометром. |
Рис. 64. Положення ареометра при вимірюванні густини. |
Для визначення відносної густини за допомогою ареометра рідину наливають у скляний циліндр місткістю не менше 0,5 л і обережно занурюють в нього ареометр. Ареометр повинен знаходитися в центрі циліндра, у жодному випадку не торкатися стінок або дна циліндра (рис. 64). Поділка, проти якої встановився верхній меніск рідини, характеризує величину густини.
Для визначення відносної густини рідин з точністю до четвертого знака користуються пікнометрами (рис. 65). Спочатку на аналітичних терезах з точністю до 0,0001 г визначають масу порожнього пікнометра, потім з водою, а потім з досліджуваною рідиною і знаходять маси рівних об'ємів досліджуваної рідини. Узявши відношення цих мас, добувають значення відносної густини d:
![]()
де р – маса порожнього пікнометра; р1 – маса пікнометра з досліджуваною рідиною; р2 – маса пікнометра з водою.
Вимірювання слід проводити двічі, причому при одній і тій же температурі.
Для визначення відносної густини рідини і твердого тіла з успіхом можна застосовувати гідростатичні терези. Ними можуть служити звичайні аналітичні терези. Щоб визначити відносну густину рідини, на ліву чашку терезів поміщають циліндрову судину з досліджуваною рідиною, а до гачка, на якому висить дужка з чашкою, підвішують циліндрове скляне грузило.
|
|
|
Рис. 65. Пікнометри. |
Спочатку зважують грузило на повітрі, потім визначають масу його в дистильованій воді, а потім у досліджуваній рідині і за формулою знаходять відносну густину даної рідини:
![]()
де р0 – маса грузила в повітрі; рв – маса грузила в дистильованій воді; р – маса грузила в досліджуваній рідині.
Для визначення відносної густини твердого тіла останнє прикріплюють замість грузила і зважують його на повітрі і в дистильованій воді. Якщо тіло на повітрі врівноважують вантажем р, а при зануренні цього тіла у воду – вантажем рв, то відносна густина тіла буде рівна:
![]()
тобто масі тіла, діленій на масу води, що витісняється ним.