- •1. Загальні правила роботи в лабораторії
- •2. Запобіжні засоби і перша допомога при нещасних випадках
- •3. Основний лабораторний хімічний посуд
- •4. Зборка приладів
- •5. Миття і сушка хімічного посуду
- •5. Використання літератури і правила складання звіту
- •1. Нагрівання
- •2. Охолоджування
- •3. Вимірювання і регулювання температури
- •4. Подрібнення і перемішування
- •5. Розчинення і Властивості деяких органічних розчинників
- •6. Сушка і основні осушувачі
- •7. Фільтрування
- •1. Кристалізація
- •2. Возгонка (сублімація)
- •3. Екстракція
- •4. Перегонка
- •5. Хроматографія
- •1. Температура плавлення
- •2. Температура кипіння
- •3. Відносна густина
- •4. Показник заломлення
- •5. Молекулярна маса
- •1. Якісний аналіз
- •2. Фізико-хімічні методи встановлення структури речовини
- •3. Ідентифікація невідомої речовини
- •1. Відновлення воднем і реакції гідрУвання
- •2. Одержання металів, їх сплавів і деяких неметалів
- •Питомі теплові ефекти (q) відновлення оксидів алюмінієм
- •3. Одержання металів і деяких неметалів відновленням водних розчинів солей
- •4. Хлорування металів, неметалів і оксидів
- •5. Бромування металів і неметалів
- •6. Йодування металів, неметалів і оксидів
- •7. Одержання сульфідів, селенідів і телуридів
- •8. Нітрування. Одержання нітридів
- •9. Одержання карбідів
- •10. Термічне розкладання речовин з метою одержання оксидів
- •11. Зневоднення крісталогідратів
- •12. Одержання солей
- •1. НітрУвання
- •2. Нітрозування
- •3. Сульфування
- •4. Галогенування
- •5. Алкілювання
- •6. Ацилювання
- •7. ДіазоТуВаНня і Реакції діазосполук
- •8. АзоспОлуЧення
- •9. Відновлення
- •10. Окислення
- •11. Амінування
- •12. Гидроксилювання
- •13. Конденсація
- •14. Полімеризація і поліконденсація
2. Возгонка (сублімація)
Сублімація – це процес випаровування твердої речовини з подальшою конденсацією пари в твердий стан, минуючи рідку фазу. Цим способом користуються для очищення твердих речовин, які мають достатньо великий тиск пари при порівняно невисокій температурі. Сублімація застосовується особливо в тих випадках, коли очищення твердої хімічної речовини від смолянистих домішок шляхом кристалізації не досягає мети. Найчастіше сублімація є відносно повільним процесом.
Швидкість сублімації прямо пропорційна тиску пари речовини при даній температурі і обернено пропорційна зовнішньому тиску в приладі. Чим менша різниця між зовнішнім тиском і тиском пари речовини, тим більша швидкість сублімації. Крім того, швидкість сублімації прямо пропорційна величині поверхні випаровуваної речовини і тому препарат потрібно дуже тонко подрібнювати.
Речовини, що мають відносно високий тиск пари, при нагріванні можуть набувати тиску пари, рівного атмосферному при температурі, що лежить нижче за температуру плавлення. Температура плавлення при нагріванні цих речовин не досягається, вони безпосередньо переходять у газоподібний стан, тобто переганяються. Температура, при якій тиск пари над твердою речовиною рівний зовнішньому тиску, називається температурою сублімації.
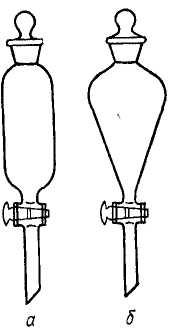
Сублімація проводиться як при атмосферному тиску, так і у вакуумі. Для сублімації при атмосферному тиску речовину поміщають на невелику фарфорову чашку, покривають її шматком фільтрувального паперу з отвором (щоб перегін не падав назад на речовину, що переганяється) і потім накривають фарфорову чашку перекинутою скляною воронкою (рис. 41, а). Відвідну трубку воронки закривають тампоном зі скляної вати. Чашку з речовиною нагрівають на маленькому полум'ї пальника або на пісочній бані. Для охолоджування на зовнішню поверхню воронки поміщають шматочок вологої вати або тканини. Нагрівати чашку з речовиною потрібно обережно; невеликий перегрів може сприяти швидкому термічному розкладанню речовини, що переганяється. Описаним вище шляхом рекомендується переганяти кристалічний йод, бензойну кислоту або нафталін.
|
|
|
Рис. 41. Прилади для сублімації: а – при атмосферному тиску; б – у вакуумі. |
При сублімації у вакуумі (рис. 41, б), знижуючи тиск, можна добитися того, щоб і у тих твердих речовин, які плавляться при нормальному тиску, температура сублімації була нижчою за температуру плавлення.
3. Екстракція
Для очищення речовин від домішок і для розділення суміші речовин часто застосовують метод екстрагування (витягування). Залежно від того, в якому вигляді знаходиться речовина, що виділяється, її можна екстрагувати як з суміші твердих речовин, так і з розчинів. Дуже важливою операцією в лабораторії хімічного синтезу є екстракція речовин з розчинів (переважно з водних), яка полягає в струшуванні розчину в певному розчиннику (як правило воді) з іншим розчинником, що не змішується з першим.
Для екстракції хімічних сполук з водних розчинів часто застосовують діетиловий і петролейний ефіри, бензин, бензол, хлороформ і ін. При цьому вибирають такий розчинник, в якому найкраще розчиняється речовина, що екстрагується, або який легше видалити з витяжки. Практично речовини, погано розчинні у воді, слід витягувати з водного розчину петролейним ефіром або бензином, а речовини, розчинні у воді – діетиловим ефіром, який володіє низькою температурою кипіння і великою здатністю розчиняти хімічні сполуки. Під час роботи з вогненебезпечними розчинниками слід погасити всі близько розташовані пальники.
Екстрагування речовин з водних розчинів і розділення рідин, що не змішуються, здійснюють за допомогою ділильних воронок різноманітної форми (рис. 42). Перед початком роботи верхню пришліфовану пробку і нижній кран ділильної воронки змазують вазеліном. Проте надлишку мастила слід уникати, оскільки при зіткненні з ефіром воно може перейти в розчин. Потім наливають в ділильну воронку розчин і додають туди розчинник (від 1/5 до 1/3 об'єму розчину); при цьому стежать, щоб кількість рідини у воронці не перевищувала 2/3 її об'єму. Ділильну воронку закривають пробкою і, однією рукою притримуючи пробку, а іншою – кран, обережно струшують її, плавно перевертаючи вгору і вниз протягом 5 – 15 хв. У жодному випадку не можна енергійно струшувати вміст воронки, оскільки при цьому утворюються стійкі емульсії, які важко руйнуються.
Як правило, при струшуванні підвищується тиск усередині воронки (частина розчину перетворюється на пару). Для вирівнювання його після короткочасного обережного струшування, тримаючи воронку в переверненому положенні, відкривають кран. Пари ефіру, що зібралися, виходять через відкритий кран, і тиск зрівнюється з атмосферним. Потім кран закривають і знов поволі струшують вміст воронки, після цього знову відкривають кран. Так повторюють кілька разів. Після закінчення струшування ділильну воронку закріплюють на штативі і дають рідині повністю розшаруватися на два шари, причому обидва шари (ефірний і водний) повинні бути прозорі. Потім відкривають пробку і обережно повертають кран, даючи поволі стікати нижньому шару в судину, при цьому стежать, щоб разом з нижнім шаром не злити частину верхнього. Верхній же шар завжди виливають через верхній отвір ділильної воронки в приймач.
|
|
|
Рис. 42. Ділильні воронки: а – циліндрова; б – конічна. |
За звичай, органічні продукти реакції переходять у верхній ефірний шар, а неорганічні солі, кислоти, основи – у водний шар. Проте в сумнівних випадках необхідно уточнити, який з двох шарів водний; для цього відбирають декілька крапель одного з шарів і додають їх в пробірку з водою; якщо краплі не розчинилися, значить це ефірний шар.
Для більш повного витягування речовини, що екстрагується, водний шар знову переносять у ділильну воронку і витягують речовину, новою порцією ефіру, поступаючи точно так, як і вперше. Речовини, погано розчинні у воді, екстрагуються двома порціями розчинника, для добре розчинних у воді сполук екстракцію потрібно проводити разів чотири.
Слід враховувати, що при проведенні екстрагування краще витягувати речовину кілька разів, невеликими порціями розчинника, ніж відразу обробляти розчин великою його кількістю. Оптимальні умови екстрагування визначають виходячи із закону розподілу Нернста, згідно з яким відношення концентрацій речовини, яка розчинена в двох розчинниках (наприклад, у воді і ефірі), що не змішуються і знаходяться в рівновазі, при даній температурі є величиною постійною:
![]()
де К – коефіцієнт розподілу; Са і Св – концентрації речовини, розчиненої в обох розчинниках.
Екстракція речовини здійснюється досить легко, якщо речовина розчиняється в екстрагуючому розчиннику значно легше, ніж в іншому розчиннику, і коефіцієнт розподілу, значно відрізняється від 1. Для речовини з коефіцієнтом розподілу К < 100 недостатньо однократної екстракції. В цьому випадку вдаються до багатократної повторної екстракції новим розчинником.
Сполучені ефірні витяжки, як правило, очищають від сторонніх речовин, найчастіше кислот або основ, з’єднаних з розчинником при екстракції. Для цього їх промивають, тобто струшують в ділильній воронці один – два рази з розбавленим водним розчином лугу (сода або бікарбонат натрію) або кислоти і на закінчення один – два рази промивають водою. При цьому завжди слід пам'ятати, що при промиванні екстракту содою може виділятися двооксид вуглецю і тиск в ділильній воронці може підвищитися, газ, який виділяється, потрібно обережно випускати через кран при його верхньому положенні.
Потім екстракт висушують відповідним осушувачем. Після сушки витяжку декантують або фільтрують через складчастий фільтр, видаляють ефір, відганяючи його на водяній бані, а залишок очищають шляхом кристалізації, сублімації або перегонки.
Часто при екстрагуванні з рідин, особливо з водних розчинів, утворюються емульсії, що важко розділяються. Суміші, схильні до утворення емульсій, в ділильній воронці сильно не струшують, а тільки злегка збовтують. Емульсії виникають з різних причин. Одна з причин – наявність малої кількості легкого осаду, що збирається на межі розділу шарів. Іншою причиною може бути великий поверхневий натяг у місці розділу двох рідин і, крім того, мала відмінність в їх густині.
Для руйнування емульсії користуються різними прийомами залежно від причин її виникнення. Емульсію, що утворюється, можна руйнувати додаванням декількох крапель етилового спирту, що зменшує поверхневий натяг, шляхом фільтрування з відсмоктуванням, шляхом тривалого відстоювання, а також насиченням розчину хлористого натрію для збільшення густини водного шару.
У багатьох випадках при екстрагуванні речовини з водного розчину рекомендується заздалегідь наситити цей розчин якою-небудь неорганічною сіллю, наприклад хлористим натрієм або сульфатом амонію. При цьому розчинність більшості органічних сполук у воді знижується і в той же час зменшуються втрати розчинника, оскільки розчинність останнього у воді також знижується. В тих випадках, коли речовина, що екстрагується, краще розчиняється у воді, ніж в органічних розчинниках, і екстракція в ділильній воронці не дає добрих результатів, застосовують безперервну екстракцію розчинів.
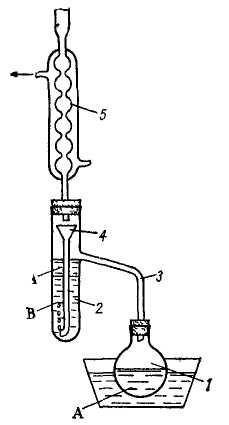
На рис. 43 зображений найпростіший прилад, придатний для роботи з невеликими кількостями розчину. Розчинник, налитий у круглодонну колбу, нагрівають на водяній бані до кипіння. Пари його через паровідвідну трубку потрапляють у зворотний холодильник, де конденсуються. Конденсат стікає у воронку, вставлену в широку пробірку, що містить рідину яка екстрагується. Оскільки густина рідини вища, ніж густина розчинника, то останній, витікаючи з воронки, проходить крізь шар розчину, що екстрагується, витягує розчинену в ньому речовину, підіймається на поверхню розчину і стікає назад в колбу.
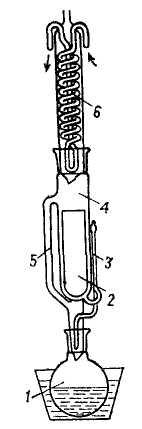
У лабораторії досить часто доводиться проводити екстрагування твердих речовин. Для цієї мети використовують так звані апарати Сокслета (найкраще на шліфах, рис. 44). Апарат складається з круглодонної колби, екстрактора і зворотного холодильника. До колби з розчинником приєднують екстрактор, в який вводять речовину, що екстрагується, добре загорнену у фільтрувальний папір або поміщену в спеціальну гільзу. Розчинник у колбі нагрівають на водяній бані до кипіння. Пари його через паровідвідну трубку поступають в екстрактор, а потім у холодильник, де конденсуються. Конденсат стікає в гільзу з речовиною, що екстрагується, витягує необхідні сполуки і через трубку для відведення екстракту переливається назад у колбу. При цьому відбувається поступове накопичення екстрагуючої речовини в колбі, причому кількість рідини практично не змінюється. Це дозволяє обмеженим об'ємом розчинника екстрагувати необмежену кількість речовини, оскільки вона весь час обробляється чистим розчинником. Після закінчення екстракції закривають воду, знімають холодильник, знімають екстрактор, дають стекти з нього залишкам рідини в колбу, потім відганяють розчинник.
|
|
|
|
Рис. 43. Прилад для безперервної екстракції розчинів: 1 – круглодонна колба; 2 – пробірка; 3 – паровідвідна трубка; 4 – воронка; 5 – зворотний холодильник, А – розчинник, В – розчин, що екстрагується. |
Рис. 44. Апарат Сокслета: 1 – круглодонна колба; 2 – гільза; 3 – труба для стоку екстракту; 4 – екстрактор; 5 – паровідвідна трубка; 6 – зворотний холодильник. |
Зонна плавка. Якщо кристалічну речовину нагрівати, повільно переміщаючи зону розплаву, то домішки концентруватимуться в цій зоні і рухатимуться разом з нею. При повторенні цього процесу кілька разів всі домішки змістяться до одного кінця і в основній масі буде отримано чисту речовину. Такий метод очищення твердих речовин, який можна розглядати як окремий випадок екстракції, отримав назву зонної плавки. Рідка фаза – розплав – знаходиться в рівновазі з твердою фазою і екстрагує з неї домішки, розчинність яких в твердій фазі відрізняється від їх розчинності в розплаві. Цей метод особливо привабливий для очищення сполук, які мають низький тиск пари або розкладаються при перегонці. В той же час він непридатний для речовин, схильних до утворення пересичених розчинів або нестійких при плавленні. Зонною плавкою не можна розділяти багатокомпонентні системи.
Очищення проводять на спеціальній установці. Речовину поміщають у вузьку, довгу ампулу, яку після відкачування повітря, запаюють і підвішують в довгій трубці з термостійкого скла, в якій створюється визначений для кожного конкретного випадку градієнт температури по висоті трубки. Ампула з речовиною за допомогою моторчика поволі підіймається усередині трубки з певною швидкістю. Після проходження всіх зон ампулу швидко повертають вниз і процес повторюють багато разів.
Можливі і інші методики, наприклад, багатократне пропускання циліндра з речовиною через кільце або просування нагрітої трубчастої печі, забезпеченої реостатом, що обігрівається, уздовж ампули з речовиною.
При проведенні зонної плавки необхідно вживати всіх заходів обережності від дії струму, опіків і можливості вибуху вакуумованої трубки, з речовиною. У приладі повинні бути діелектричні килимки, працюючі захищаються щитком, а при його відсутності одягають окуляри.