
- •Федеральное государственное образовательное учреждение высшего профессионального образования
- •А. А. Нестеров, э.А.Бикяшев теория химического строения и свойства веществ
- •Модуль №1
- •1 Развитие представлений о строении атома
- •Ранние модели строения атома
- •1.2 Квантово-механическое описание атомов
- •1.3 Правила квантования
- •1.4 Правила заполнение электронами атомных орбиталей
- •1.5 Электронное строение атомов в основном состоянии. Связь электронного строения атомов и структуры периодической системы элементов
- •1.6 Закономерности изменения атомных (ионных) радиусов
- •1.7 Закономерности изменения энергий (потенциалов) ионизации
- •1.8 Закономерности изменения сродства к электрону
- •1.9 Электроотрицательности атомов и закономерности их изменения
- •Модуль №2 Электростатические представления в теориях химической связи
- •2.1. Теория электрохимического дуализма
- •2.2. Теория валентности
- •2.3. Теория ионной связи
- •2.3.1. Основные положения теории ионной связи Косселя
- •2.3.2.Оценка энергии ионной связи.
- •2.3.3. Границы применимости теории ионной связи
- •2.3.4 Энергия кристаллической ионной решетки.
- •2.3.5. Ионные радиусы
- •2.3.6. Ионные структуры
- •2.3.6.1. Основные принципы модели жесткой сферы
- •2.3.6.2. Границы применимости модели жесткой сферы
- •2.3.7. Основные свойства ионной связи и её недостатки
- •2.4. Теория поляризации.
- •2.5. Межмолекулярное взаимодействие.
- •Модуль №3
- •3.1. Теория Льюиса и метод олэп.
- •3.2.Основные принципы описания молекул в квантовой химии и метод валентных связей (мвс).
- •3.2.1. Основные принципы описания молекул в квантовой химии
- •3.2.2.Описание механизмов образования химических связей в рамках мвс
- •3.2.3. Описание строения молекул в рамках мвс
- •3.2.5. Дипольный момент и полярность связей
- •3.2.6. Достоинства и недостатки мвс
- •3.3. Метод молекулярных орбиталей (ммо).
- •3.4. Cравнение мвс и ммо
- •Модуль №4 Теория связи в металлах и комплексных соединениях
- •4.1. Химическая связь в кристаллах металлов.
- •4.1.1 Теория «электронного газа».
- •4.2 Зонная теория химической связи для кристаллов металлов, полупроводников и диэлектриков.
- •4.3 Строение кристаллов металлов.
- •4.4 Координационная теория а.Вернера, современная трактовка ее основных понятий и положений
- •4.4.1 Предпосылки создания теории строения комплексов
- •4.4.2 Координационная теория а.Вернера: состав комплексов, поведение в растворах, структура (изомерия)
- •4.4.3 Современная трактовка основных понятий координационной теории
- •4.4.4 Номенклатура комплексных соединений
- •4.4.5 Классификация комплексных соединений
- •4.4.6 Изомерия комплексов
- •4.4.7 Некоторые типы реакций с участием комплексных соединений
- •4.5 Теории химической связи в комплексах
- •4.5.1 Электростатическая (ионная) теория
- •4.5.2 Квантово-механические теории описания химической связи в комплексах
- •4.5.2.1 Метод валентных связей
- •4.5.2.2 Теория кристаллического поля
- •4.5.2.3 Варианты проявления энергетического расщепления орбиталей
- •4.5.2.4 Недостатки ткп
- •4.5.3 Теория поля лигандов (метод молекулярных орбиталей)
- •Заключение
- •Оглавление
1.8 Закономерности изменения сродства к электрону
Сродством к электрону (Еē) называют энергетический эффект присоединения дополнительного электрона на валентную орбиталь изолированного (газообразного) атома:
![]() .
.
В большинстве случаев данный процесс идет самопроизвольно и при этом по давно сложившейся традиции энергии сродства приписывают положительный знак. Отрицательное сродство к электрону имеют лишь атомы с устойчивыми электронными конфигурациями: полузаполненными и полностью заполненными подуровнями (напомним, что такие атомы очень стабильны к изменению своей электронной конфигурации, в частности, имеют завышенные энергии ионизации – см. рис. 1.16). Но именно в отношении к этим элементам и только к ним применима хорошо известная многим школьникам фраза, что каким-то атомам (в качестве примера, обычно, называют кислород и галогены) "гораздо выгодней присоединить дополнительный электрон, чем потерять собственный". Так вот, потеря электрона никогда не проходит "с выгодой", – это всегда эндотермические процессы. Причем для ионизации, скажем, атомов бериллия, азота и неона действительно требуются большие затраты энергии, чем на присоединение дополнительного электрона к ним. Все прочие элементы второго периода присоединяют электрон экзотермично.
Прежде, чем приступать к анализу закономерностей изменения Еē, отметим, что определить смысл сродства к электрону можно и иначе: это энергия, которую необходимо затратить (ряде случаев она выделяется) удаления электрона из газообразного однозарядного аниона:
![]()

|
Рис. 1.22 – Изменение первой энергии ионизации, сродства к электрону и электроотрицательности (найденной по первоначальной, упрощенной модели Малликена) для элементов II–го и III–го периодов периодической системы. |
Теперь несложно сделать несколько важных обобщающих выводов:
Сродство к электрону зависит от тех же факторов, что и энергии ионизации (см. стр.65), но, поскольку в анионах Э– на один электрон больше, чем в нейтральных атомах, то схемы изменения I1 и Еē напоминают друг друга со сдвижкой на один элемент.
Для любого атома всегда |Еē| < |I1|, т.к. появление дополнительного электрона увеличивает эффект экранирования заряда ядра. Причем по периоду роль зарядового электрона в межэлектронном отталкивании должна повышаться из-за уменьшения размера электронного облака. Как следствие в целом растет разница между I1 и Еē (рис.1.22). В более крупных атомах III-го и последующих периодов, с одной стороны, растущий заряд ядра не так сильно стабилизирует некайносимметричные 3р–, 4р–… орбитали (I1 увеличиваются медленней), а, с другой, – в более крупных атомах 3р–, 4р–… элементов вклад дополнительного электрона в межэлектронное отталкивание будет выражен слабей, поэтому первые 3р–элементы (Na, Mg) имеют более низкое сродство к электрону, чем Li и Be, а последние (например, S, Cl) присоединяют электрон лучше, чем О и F, соответственно.
В подгруппах электронные конфигурации Э– сохраняются неизменными, поэтому сродство к электрону меняется в соответствие с растущим орбитальным радиусом, который, в свою очередь, формируется с учетом заряда ядра и эффектов экранирования и проникновения (zэфф) валентных электронов. В то же время, для р–элементов второго периода постепенно усиливается вклад зарядового электрона в межэлектронное отталкивание, поэтому их сродство к электрону постепенно становится все более низким по сравнению с элементами III-го преиода (рис.1.22).
|
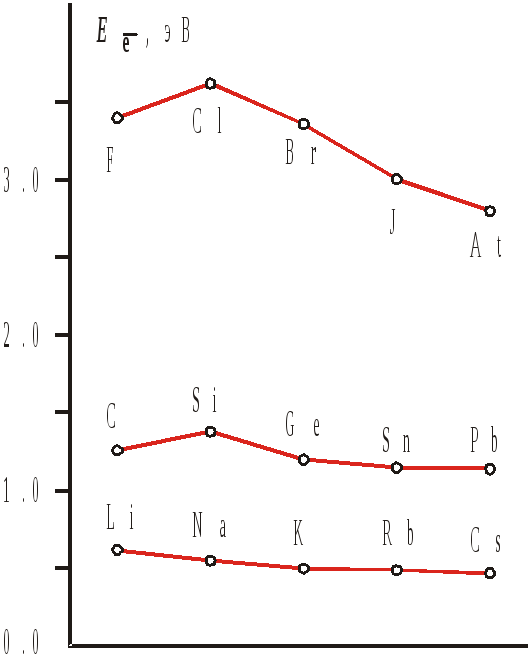
Рис. 1.23 – Изменение сродства к электрону в некоторых главных подгруппах периодической системы. |
При этом у крупных атомов больших периодов сродство к электрону оказывается настолько низким, что их абсолютные значения могут найдены только с большими погрешностями.
В заключение отметим, что сродство ко второму электрону не представляет особого интереса, т.к. сближение одноименно заряженных
![]() .
.
частиц никогда не происходит самопроизвольно. Двухзарядные одноатомные ионы (как катионы, так и анионы) могут быть стабилизированы только в составе ионных кристаллов за счет энергии кристаллической решетки или в растворах за счет энергии сольватации.
