- •Федеральное государственное образовательное учреждение высшего профессионального образования
- •А. А. Нестеров, э.А.Бикяшев теория химического строения и свойства веществ
- •Модуль №1
- •1 Развитие представлений о строении атома
- •Ранние модели строения атома
- •1.2 Квантово-механическое описание атомов
- •1.3 Правила квантования
- •1.4 Правила заполнение электронами атомных орбиталей
- •1.5 Электронное строение атомов в основном состоянии. Связь электронного строения атомов и структуры периодической системы элементов
- •1.6 Закономерности изменения атомных (ионных) радиусов
- •1.7 Закономерности изменения энергий (потенциалов) ионизации
- •1.8 Закономерности изменения сродства к электрону
- •1.9 Электроотрицательности атомов и закономерности их изменения
- •Модуль №2 Электростатические представления в теориях химической связи
- •2.1. Теория электрохимического дуализма
- •2.2. Теория валентности
- •2.3. Теория ионной связи
- •2.3.1. Основные положения теории ионной связи Косселя
- •2.3.2.Оценка энергии ионной связи.
- •2.3.3. Границы применимости теории ионной связи
- •2.3.4 Энергия кристаллической ионной решетки.
- •2.3.5. Ионные радиусы
- •2.3.6. Ионные структуры
- •2.3.6.1. Основные принципы модели жесткой сферы
- •2.3.6.2. Границы применимости модели жесткой сферы
- •2.3.7. Основные свойства ионной связи и её недостатки
- •2.4. Теория поляризации.
- •2.5. Межмолекулярное взаимодействие.
- •Модуль №3
- •3.1. Теория Льюиса и метод олэп.
- •3.2.Основные принципы описания молекул в квантовой химии и метод валентных связей (мвс).
- •3.2.1. Основные принципы описания молекул в квантовой химии
- •3.2.2.Описание механизмов образования химических связей в рамках мвс
- •3.2.3. Описание строения молекул в рамках мвс
- •3.2.5. Дипольный момент и полярность связей
- •3.2.6. Достоинства и недостатки мвс
- •3.3. Метод молекулярных орбиталей (ммо).
- •3.4. Cравнение мвс и ммо
- •Модуль №4 Теория связи в металлах и комплексных соединениях
- •4.1. Химическая связь в кристаллах металлов.
- •4.1.1 Теория «электронного газа».
- •4.2 Зонная теория химической связи для кристаллов металлов, полупроводников и диэлектриков.
- •4.3 Строение кристаллов металлов.
- •4.4 Координационная теория а.Вернера, современная трактовка ее основных понятий и положений
- •4.4.1 Предпосылки создания теории строения комплексов
- •4.4.2 Координационная теория а.Вернера: состав комплексов, поведение в растворах, структура (изомерия)
- •4.4.3 Современная трактовка основных понятий координационной теории
- •4.4.4 Номенклатура комплексных соединений
- •4.4.5 Классификация комплексных соединений
- •4.4.6 Изомерия комплексов
- •4.4.7 Некоторые типы реакций с участием комплексных соединений
- •4.5 Теории химической связи в комплексах
- •4.5.1 Электростатическая (ионная) теория
- •4.5.2 Квантово-механические теории описания химической связи в комплексах
- •4.5.2.1 Метод валентных связей
- •4.5.2.2 Теория кристаллического поля
- •4.5.2.3 Варианты проявления энергетического расщепления орбиталей
- •4.5.2.4 Недостатки ткп
- •4.5.3 Теория поля лигандов (метод молекулярных орбиталей)
- •Заключение
- •Оглавление
4.5 Теории химической связи в комплексах
Любая теория химического строения должна объяснять имеющиеся и предсказывать новые экспериментальные факты, касающиеся состава, структуры и свойств веществ. Применительно к комплексным соединениям теория связи должна, в частности, объяснить:
относительную стабильность комплексов к обмену лигандами (предрасположенность к связыванию тех или комплексообразователей с определенным типом лигандов) или изменению степени окисления центрального атома;
предпочтительность тех или иных координационных чисел и вариантов пространственного строения;
спектральные свойства комплексов (происхождение окрашенности, зависимость спектров поглощения от состава и структуры комплексов);
особенности магнитных свойств комплексных соединений.
Развитие представлений о химической связи в комплексных соединениях прошло четыре стадии. Оно началось с электростатической теории, которую сменили теория валентных связей (МВС) и теория кристаллического поля (ТКП), которые появились почти одновременно. Затем была разработана теория молекулярных орбиталей (ММО).
4.5.1 Электростатическая (ионная) теория
Электростатическая (ионная) теория химической связи в комплексах, основанная на использовании электронного строения атомов, была предложена Косселем и Магнусом в 1915–1922гг., т.е. еще до разработки современной квантово-механической модели атома. Неудивительно, что с ее помощью удалось решить лишь очень небольшой круг вопросов теории комплексов.
В основе ионной теории лежат представления об электростатическом притяжении положительно заряженного комплексообразователя и отрицательно заряженных лигандов. Причем, используя законы кулоновского взаимодействия, удалось расчетным путем обосновать энергетически выгодные КЧ в зависимости от зарядов и размеров комплексообразователя и лигандов.39 Например, образование комплекса [AgJ2]– энергетически выгодно, т.к. сила притяжения ионов Ag+ и J– определяемая формулой
![]() ,
(4.8)
,
(4.8)
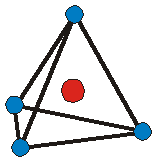
в четыре раза превышает силы отталкивания ионов J– (рис. 12.1):
![]() ,
(4.9)
,
(4.9)
где коэффициент 0.25называется коэффициентом экранирования (Кэкр). Он показывает, в какой степени притяжение комплексообразователь–лиганды скомпенсировано взаимным отталкиванием самих лигандов. Связывание дополнительных лигандов, увеличение КЧ возможно до тех пор, пока коэффициент экранирования не достигнет единицы. Расчеты показывают,

-
Рис.4.25 – Силовые взаимодействия при образовании
комплекса [AgJ2]–
что при взаимодействии однозарядных ионов в зависимости от концентрации L– в растворе возможно образование комплексов [ML2]–, [ML3]2– (образование иона [ML4]3– крайне маловероятно, табл. 4.10).
Таблица 4.10
Коэффициенты экранирования, координационные числа,
геометрическая
конфигурация комплексов состава ![]() .
.
|
КЧ |
Кэкр |
Геометрическая форма |
КЧ |
Кэкр |
Геометрическая форма |
|
2
3
4
4
|
0.25
0.58
0.92
0.96
|
|
5
6
6
|
1.38
1.66
1.83
|
|
Увеличение заряда комплексообразователя влечет за собой увеличение сил притяжения комплексообразователь–лиганды, что равносильно увеличению КЧ. Было показано, что однозарядные катионы должны иметь координационные числа 2 и 3, двухзарядные – 4, для трехзарядных ионов КЧ могут иметь значения 4, 5, 6. С другой стороны, увеличение заряда лигандов должно усиливать экранирование и приводить к уменьшению КЧ.
Однако такие расчеты справедливы лишь для сферически симметричных ионов (в том случае, если лиганды одноатомны, и, к тому же, подобно центральному иону, имеют заполненную оболочку инертного газа). Для комплексов переходных элементов данная теория часто давала результаты, которые не согласовывались с экспериментом.
В качестве положительного момента можно отметить, что ионная модель, опираясь на простые геометрические соображения, предлагала наглядное объяснение зависимости координационных чисел от размеров центрального атома и лигандов. Но, в то же время, в химии переходных элементов более крупные ионы 4d– и 5d–рядов нередко образуют более стабильные комплексы, чем меньшие по размеру ионы 3d–элементов.
Кроме значений координационных чисел, ионная теория не объясняла возможности образования квадратных координаций, не говоря уже об электронных состояниях комплексов. Например: фторидный комплекс Fe2+ ([FeF6]4–) обладает парамагнитными свойствами, свидетельствующими о наличии четырех неспаренных электронов, а цианидный ([Fe(CN)6]4–) – диамагнитен, т.е. неспаренных электронов не имеет; в аналогичных комплексах Fe3+ ([FeF6]3– и [Fe(CN)6]3–) обнаруживаются пять и один неспаренный электрон, соответственно.
В рамках данной простой электростатической модели не было никаких идейных подходов даже для качественного объяснения окрашенности комплексов, часто наблюдаемого изменения окраски даже при минимальном изменении состава внутренней сферы:
|
[Co(NH3)6]3+ – желтый |
[Co(NH3)6]3+ – желтый |
|
[Co(NH3)5Cl]2+ – пурпурнокрасный |
[Co(NH3)5NCS]2+ – оранжевый |
|
транс-[Co(NH3)4Cl2]+ – красный |
[Co(NH3)5ОН2]2+ – красный |
|
цис-[Co(NH3)4Cl2]+ – фиолетовый |
[Co(NH3)5ОН]2+ – розовый |