- •Федеральное государственное образовательное учреждение высшего профессионального образования
- •А. А. Нестеров, э.А.Бикяшев теория химического строения и свойства веществ
- •Модуль №1
- •1 Развитие представлений о строении атома
- •Ранние модели строения атома
- •1.2 Квантово-механическое описание атомов
- •1.3 Правила квантования
- •1.4 Правила заполнение электронами атомных орбиталей
- •1.5 Электронное строение атомов в основном состоянии. Связь электронного строения атомов и структуры периодической системы элементов
- •1.6 Закономерности изменения атомных (ионных) радиусов
- •1.7 Закономерности изменения энергий (потенциалов) ионизации
- •1.8 Закономерности изменения сродства к электрону
- •1.9 Электроотрицательности атомов и закономерности их изменения
- •Модуль №2 Электростатические представления в теориях химической связи
- •2.1. Теория электрохимического дуализма
- •2.2. Теория валентности
- •2.3. Теория ионной связи
- •2.3.1. Основные положения теории ионной связи Косселя
- •2.3.2.Оценка энергии ионной связи.
- •2.3.3. Границы применимости теории ионной связи
- •2.3.4 Энергия кристаллической ионной решетки.
- •2.3.5. Ионные радиусы
- •2.3.6. Ионные структуры
- •2.3.6.1. Основные принципы модели жесткой сферы
- •2.3.6.2. Границы применимости модели жесткой сферы
- •2.3.7. Основные свойства ионной связи и её недостатки
- •2.4. Теория поляризации.
- •2.5. Межмолекулярное взаимодействие.
- •Модуль №3
- •3.1. Теория Льюиса и метод олэп.
- •3.2.Основные принципы описания молекул в квантовой химии и метод валентных связей (мвс).
- •3.2.1. Основные принципы описания молекул в квантовой химии
- •3.2.2.Описание механизмов образования химических связей в рамках мвс
- •3.2.3. Описание строения молекул в рамках мвс
- •3.2.5. Дипольный момент и полярность связей
- •3.2.6. Достоинства и недостатки мвс
- •3.3. Метод молекулярных орбиталей (ммо).
- •3.4. Cравнение мвс и ммо
- •Модуль №4 Теория связи в металлах и комплексных соединениях
- •4.1. Химическая связь в кристаллах металлов.
- •4.1.1 Теория «электронного газа».
- •4.2 Зонная теория химической связи для кристаллов металлов, полупроводников и диэлектриков.
- •4.3 Строение кристаллов металлов.
- •4.4 Координационная теория а.Вернера, современная трактовка ее основных понятий и положений
- •4.4.1 Предпосылки создания теории строения комплексов
- •4.4.2 Координационная теория а.Вернера: состав комплексов, поведение в растворах, структура (изомерия)
- •4.4.3 Современная трактовка основных понятий координационной теории
- •4.4.4 Номенклатура комплексных соединений
- •4.4.5 Классификация комплексных соединений
- •4.4.6 Изомерия комплексов
- •4.4.7 Некоторые типы реакций с участием комплексных соединений
- •4.5 Теории химической связи в комплексах
- •4.5.1 Электростатическая (ионная) теория
- •4.5.2 Квантово-механические теории описания химической связи в комплексах
- •4.5.2.1 Метод валентных связей
- •4.5.2.2 Теория кристаллического поля
- •4.5.2.3 Варианты проявления энергетического расщепления орбиталей
- •4.5.2.4 Недостатки ткп
- •4.5.3 Теория поля лигандов (метод молекулярных орбиталей)
- •Заключение
- •Оглавление
2.3.6. Ионные структуры
2.3.6.1. Основные принципы модели жесткой сферы
Ионы, имеющие электронную структуру атомов инертных газов, можно считать сферически симметричными. В связи с этим силы их притяжения к ионам противоположного знака одинаковы в любом направлении. Поэтому структура ионных кристаллов определяется только геометрическими факторами: соотношением числа ионов различного сорта в кристаллической решетке (определяемого по формуле соединения) и их размерами. Последний фактор предопределяется отношением радиусов ионов, например г+/г–.
В основе прогноза строения кристалла также лежит принцип его электронейтральности как макрообъекта и принцип минимума энергии.
Составляющими, вносящими вклад в энергию кристаллической решетки вещества, являются:
- силы притяжения между противоположно заряженными ионами, которые возрастают с увеличением КЧ и уменьшением межядерного расстояния между противоположно заряженными ионами;
- силы отталкивания, возрастающие при сближении одинаково заряженных ионов.
В рамках концепции жёстких сфер минимальные расстояния между одинаковыми ионами равны сумме их ионных радиусов, когда они «касаются» друг друга в кристаллической решетке.
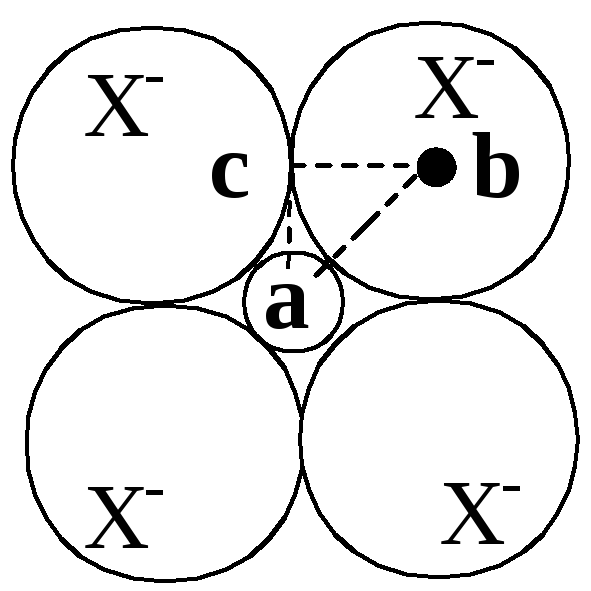
Рассмотрим с учетом вышеизложенного соединение типа МХ (т.е. с равным числом катионов и анионов), в котором КЧ = 6 (октаэдрическое расположение ионов Х– вокруг иона М+ и ионов М+ вокруг ионов Х– (рис. 4.2).
|
|
|
|
Рис. 4.2 – Структура NaCl (элементарная ячейка хлорида натрия изображена сплошными линиями).
|
Рис. 5.2 – расположение ионов М+ и Х–, находящихся в плоскости основания. |
Тогда cb = ab · cos450 где ab = r0 M–X cb=rx-
rX- = (rM+ + rX-) / √2
![]() =
√2 – 1 = 0,414
=
√2 – 1 = 0,414
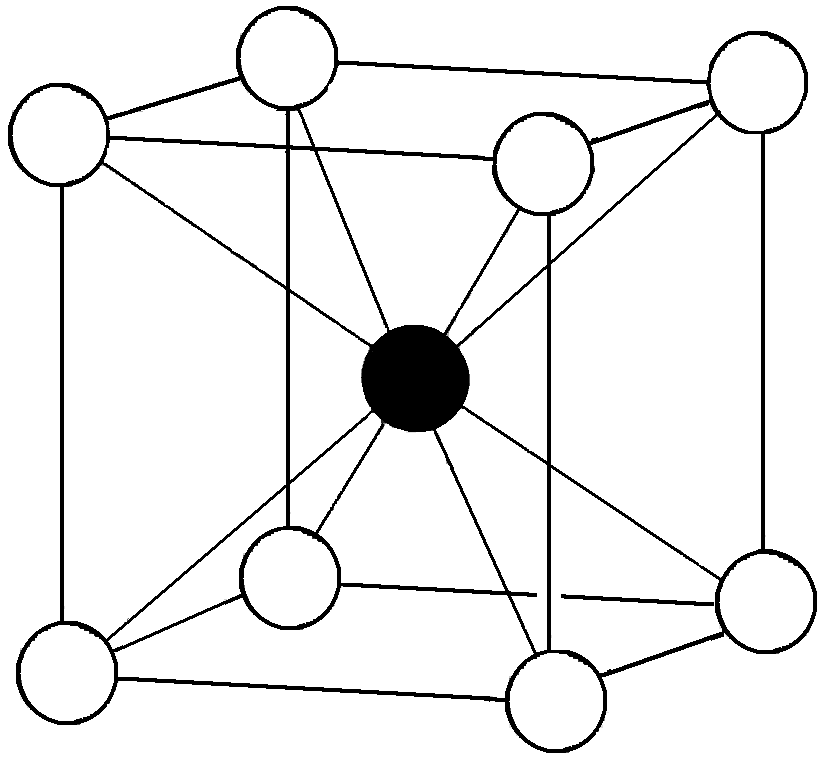
т.е. это величина отношения радиусов катиона и аниона предельно возможная для данной структуры. При дальнейшем росте радиуса аниона (или уменьшении гм+), должно произойти уменьшение КЧ, в частности, может формироваться структура типа ZnS с КЧ=4, для которой критическое соотношение радиусов ионов равно 0,22. Если же значения rм+ и rх- будут сближаться, то при соотношении rм+/rх- >0,732 будет наблюдаться рост КЧ до 8 и образуется структура типа CsCl (рис. 6.2).
Рис. 6.2. Структура CsCl (справа – элементарная ячейка).
|
|
|
|
| |
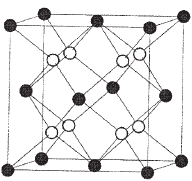
Если ионов одного вида вдвое больше, чем другого (т.е. состав соединения M2X или МX2), то в структурах с учетом указанного состава координационные числа этих двух видов ионов должны быть в отношении 1:2 или 2:1, соответственно. При соотношениях ионных радиусов >0,732 образуется структура типа флюорита (СаF2), в которой каждый ион Са2+ окружен восьмью ионами F–, расположенных по углам куба, а каждый ион F– – четырьмя ионами Са2+.
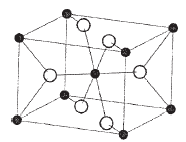
При соотношении rм+/rх- от 0,414 до 0,732 образуется структура типа рутила (TiО2) (рис. 7.2 и 8.2).
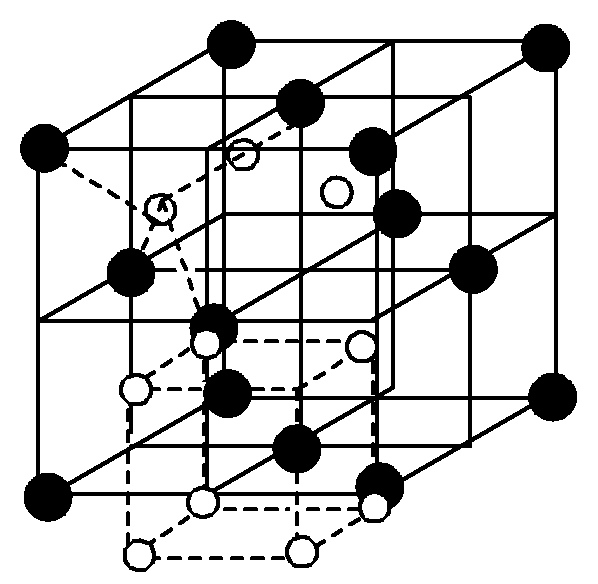

Рис. 7.2 – Структура флюорита Рис.8.2 – Структура рутила.
|
|
|
|
Рис. 7.2а– структура CaF2 |
Рис. 8.2а –структура TiO2 |
В рутиле каждый ион титана октаэдрически окружен шестью ионами кислорода, а вокруг каждого иона кислорода расположены по вершинам равнобедренного треугольника три иона титана. Так образом КЧ ионов титана равно 6, а КЧ ионов кислорода - 3.