
- •Федеральное государственное образовательное учреждение высшего профессионального образования
- •А. А. Нестеров, э.А.Бикяшев теория химического строения и свойства веществ
- •Модуль №1
- •1 Развитие представлений о строении атома
- •Ранние модели строения атома
- •1.2 Квантово-механическое описание атомов
- •1.3 Правила квантования
- •1.4 Правила заполнение электронами атомных орбиталей
- •1.5 Электронное строение атомов в основном состоянии. Связь электронного строения атомов и структуры периодической системы элементов
- •1.6 Закономерности изменения атомных (ионных) радиусов
- •1.7 Закономерности изменения энергий (потенциалов) ионизации
- •1.8 Закономерности изменения сродства к электрону
- •1.9 Электроотрицательности атомов и закономерности их изменения
- •Модуль №2 Электростатические представления в теориях химической связи
- •2.1. Теория электрохимического дуализма
- •2.2. Теория валентности
- •2.3. Теория ионной связи
- •2.3.1. Основные положения теории ионной связи Косселя
- •2.3.2.Оценка энергии ионной связи.
- •2.3.3. Границы применимости теории ионной связи
- •2.3.4 Энергия кристаллической ионной решетки.
- •2.3.5. Ионные радиусы
- •2.3.6. Ионные структуры
- •2.3.6.1. Основные принципы модели жесткой сферы
- •2.3.6.2. Границы применимости модели жесткой сферы
- •2.3.7. Основные свойства ионной связи и её недостатки
- •2.4. Теория поляризации.
- •2.5. Межмолекулярное взаимодействие.
- •Модуль №3
- •3.1. Теория Льюиса и метод олэп.
- •3.2.Основные принципы описания молекул в квантовой химии и метод валентных связей (мвс).
- •3.2.1. Основные принципы описания молекул в квантовой химии
- •3.2.2.Описание механизмов образования химических связей в рамках мвс
- •3.2.3. Описание строения молекул в рамках мвс
- •3.2.5. Дипольный момент и полярность связей
- •3.2.6. Достоинства и недостатки мвс
- •3.3. Метод молекулярных орбиталей (ммо).
- •3.4. Cравнение мвс и ммо
- •Модуль №4 Теория связи в металлах и комплексных соединениях
- •4.1. Химическая связь в кристаллах металлов.
- •4.1.1 Теория «электронного газа».
- •4.2 Зонная теория химической связи для кристаллов металлов, полупроводников и диэлектриков.
- •4.3 Строение кристаллов металлов.
- •4.4 Координационная теория а.Вернера, современная трактовка ее основных понятий и положений
- •4.4.1 Предпосылки создания теории строения комплексов
- •4.4.2 Координационная теория а.Вернера: состав комплексов, поведение в растворах, структура (изомерия)
- •4.4.3 Современная трактовка основных понятий координационной теории
- •4.4.4 Номенклатура комплексных соединений
- •4.4.5 Классификация комплексных соединений
- •4.4.6 Изомерия комплексов
- •4.4.7 Некоторые типы реакций с участием комплексных соединений
- •4.5 Теории химической связи в комплексах
- •4.5.1 Электростатическая (ионная) теория
- •4.5.2 Квантово-механические теории описания химической связи в комплексах
- •4.5.2.1 Метод валентных связей
- •4.5.2.2 Теория кристаллического поля
- •4.5.2.3 Варианты проявления энергетического расщепления орбиталей
- •4.5.2.4 Недостатки ткп
- •4.5.3 Теория поля лигандов (метод молекулярных орбиталей)
- •Заключение
- •Оглавление
2.3.5. Ионные радиусы
Условный размер иона определяется силой притяжения между внешними электронами и ядром с учетом уменьшения положительного заряда последнего за счет эффекта экранирования. Поэтому, при превращении атома в положительный ион, т.е. при уменьшении числа электронов в системе, сила притяжения, действующая на каждый из оставшихся электронов, возрастает, что способствует уменьшению размера иона по сравнению с атомом. Наоборот, при образовании отрицательного иона за счет увеличения числа электронов на внешнем энергетическом уровне его размер будет увеличиваться по сравнению с исходным атомом.
Экспериментально расстояние между ионами в кристаллической решетке может быть определено с помощью дифракционных методов. Значения межионных расстояний для кристаллов ряда галогенидов щелочных металлов приведены в таблице 6.2.
Таблица 6.2 – Межионные расстояния в кристаллах галогенидов щелочных металлов.
|
Состав |
г0(Ме+-Г–), Å |
∆r = ro КГ – ro NaГ , Å |
Состав |
ro(Me+–Г–), Å |
∆r= ro КГ – ro NaГ, Å |
|
КF NaF |
2,67 2,31 |
0,36 |
КBr NaBr |
3,30 2,99 |
0,31 |
|
КCl NaCl |
3,14 2,82 |
0,32 |
КI NaI |
3,51 3,22 |
0,30 |
Если вычесть из rо(К-Г) rо(Nа-Г), то, как видно из таблицы, получим почти постоянную разность ∆r. Данный факт можно объяснить, предположив, что каждый ион представляет собой сферу постоянного радиуса. Тогда измеренное межядерное расстояние rо представляет собой сумму радиусов двух соприкасающихся сфер противоположного заряда r++r–. Может показаться удивительным, что это предположение достаточно хорошо подтверждается экспериментальными данными, несмотря на то, что вероятность нахождения электрона даже на значительном расстоянии от ядра не равна нулю. Однако, исходя из радиального распределения электронной плотности в ионах подобного типа, можно сделать вывод, что она быстро уменьшается с ростом r и предположения о том, что ион имеет конечный радиус, хотя принципе и неверно, но позволяет в первом приближении интерпретировать строение ионных кристаллов.
Таким образом, если радиус одного из ионов известен и экспериментально определено межионное расстояние, можно определить радиус иона-партнера:
r – = ro – r +
Для определения радиусов ионов предложено несколько методов:
а) в кристаллах, образованных небольшими по размеру катионами и анионами большого радиуса, анионы соприкасаются друг с другом и, следовательно, половина расстояния между анионами равна их ионному радиусу (Ланде, 1920 г.);
б) межионное расстояние го делят в отношении значений поляризуемости ионов, т.к. поляризуемость пропорциональна объему иона (Вазастьерн, 1923 г.);
в) межионное расстояние го делят в отношении эффективных зарядов ядер ионов (заряд ядра иона с учетом эффекта экранирования) (Полинг,1927г).
г) в последние годы дифракционные методы позволили экспериментально измерить электронные плотности в кристаллах типа хлорида натрия. В двумерном сечении контуры изоэлектронной плотности представляют собой концентрические окружности, центры которых совпадают с упорядоченно расположенными ядрами ионов натрия и хлора. Электронная плотность имеет минимум на линии, соединяющей эти ядра. Если положение этого минимума принять за точку, в которой соприкасаются сферические катион и анион, можно определить радиусы последних.
Исходя из выше сказанного, можно сделать вывод, что в связи с различными методами определения, абсолютные значения радиусов ионов в различных системах будут отличаться друг от друга.
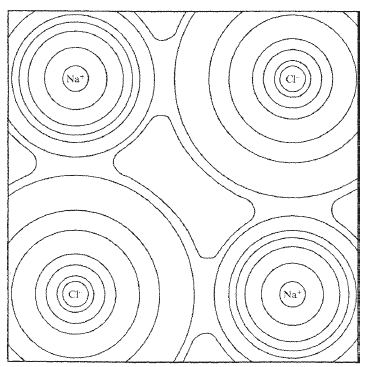
Рисунок 3.2 – Фрагмент карты электронной плотности решетки NaCl.
Кроме того, значения ионного радиуса данной частицы зависят от ее координационного числа (КЧ) в кристаллической решетке (число ближайших противоионов, окружающих данный ион в кристаллической решетке). Обычно в таблицах приводятся значения ионных радиусов для КЧ=6, с указанием поправок для других КЧ.
Однако, несмотря на указанные недостатки, концепция ионных радиусов широко используется в неорганической химии, кристаллохимии и геохимии. Это связано с тем, что независимо от того, какая система ионных радиусов используется, основной принцип подхода к понятию ионного радиуса сохраняется (го=г++г–), что дает возможность определить длину химической связи в кристалле. Кроме того, понятие ионных радиусов успешно применяется для прогноза строения кристаллических веществ различного состава.
