
- •Федеральное государственное образовательное учреждение высшего профессионального образования
- •А. А. Нестеров, э.А.Бикяшев теория химического строения и свойства веществ
- •Модуль №1
- •1 Развитие представлений о строении атома
- •Ранние модели строения атома
- •1.2 Квантово-механическое описание атомов
- •1.3 Правила квантования
- •1.4 Правила заполнение электронами атомных орбиталей
- •1.5 Электронное строение атомов в основном состоянии. Связь электронного строения атомов и структуры периодической системы элементов
- •1.6 Закономерности изменения атомных (ионных) радиусов
- •1.7 Закономерности изменения энергий (потенциалов) ионизации
- •1.8 Закономерности изменения сродства к электрону
- •1.9 Электроотрицательности атомов и закономерности их изменения
- •Модуль №2 Электростатические представления в теориях химической связи
- •2.1. Теория электрохимического дуализма
- •2.2. Теория валентности
- •2.3. Теория ионной связи
- •2.3.1. Основные положения теории ионной связи Косселя
- •2.3.2.Оценка энергии ионной связи.
- •2.3.3. Границы применимости теории ионной связи
- •2.3.4 Энергия кристаллической ионной решетки.
- •2.3.5. Ионные радиусы
- •2.3.6. Ионные структуры
- •2.3.6.1. Основные принципы модели жесткой сферы
- •2.3.6.2. Границы применимости модели жесткой сферы
- •2.3.7. Основные свойства ионной связи и её недостатки
- •2.4. Теория поляризации.
- •2.5. Межмолекулярное взаимодействие.
- •Модуль №3
- •3.1. Теория Льюиса и метод олэп.
- •3.2.Основные принципы описания молекул в квантовой химии и метод валентных связей (мвс).
- •3.2.1. Основные принципы описания молекул в квантовой химии
- •3.2.2.Описание механизмов образования химических связей в рамках мвс
- •3.2.3. Описание строения молекул в рамках мвс
- •3.2.5. Дипольный момент и полярность связей
- •3.2.6. Достоинства и недостатки мвс
- •3.3. Метод молекулярных орбиталей (ммо).
- •3.4. Cравнение мвс и ммо
- •Модуль №4 Теория связи в металлах и комплексных соединениях
- •4.1. Химическая связь в кристаллах металлов.
- •4.1.1 Теория «электронного газа».
- •4.2 Зонная теория химической связи для кристаллов металлов, полупроводников и диэлектриков.
- •4.3 Строение кристаллов металлов.
- •4.4 Координационная теория а.Вернера, современная трактовка ее основных понятий и положений
- •4.4.1 Предпосылки создания теории строения комплексов
- •4.4.2 Координационная теория а.Вернера: состав комплексов, поведение в растворах, структура (изомерия)
- •4.4.3 Современная трактовка основных понятий координационной теории
- •4.4.4 Номенклатура комплексных соединений
- •4.4.5 Классификация комплексных соединений
- •4.4.6 Изомерия комплексов
- •4.4.7 Некоторые типы реакций с участием комплексных соединений
- •4.5 Теории химической связи в комплексах
- •4.5.1 Электростатическая (ионная) теория
- •4.5.2 Квантово-механические теории описания химической связи в комплексах
- •4.5.2.1 Метод валентных связей
- •4.5.2.2 Теория кристаллического поля
- •4.5.2.3 Варианты проявления энергетического расщепления орбиталей
- •4.5.2.4 Недостатки ткп
- •4.5.3 Теория поля лигандов (метод молекулярных орбиталей)
- •Заключение
- •Оглавление
1.4 Правила заполнение электронами атомных орбиталей
Применяя законы термодинамики, следует ожидать, что при низких температурах электроны будут самопроизвольно заселять АО с минимальной энергией (принцип минимума энергии для основного состояния атома). Как было показано ранее (стр.23), точно определить энергию АО в многоэлектронном атоме невозможно, но, поскольку энергия электрона зависит от главного и орбитального квантовых чисел, то были предложены эмпирические правила, которые позволяют сравнить энергии АО, не рассчитывая их (правила В.Клечковского):
минимальную энергию имеет атомная орбиталь с минимальной суммой n+l;
если для нескольких атомных орбиталей эта сумма совпадает, то меньшую энергию имеет орбиталь с меньшим значением главного квантового числа n.
Применим эти правила для сравнения атомных орбиталей первых четырех энергетических уровней.
Как видно из таблицы 1.4, в первых двух энергетических уровнях энергия атомных орбиталей меняется достаточно просто. А вот затем в конкуренцию с орбиталями третьего энергетического уровня "включается" 4s–орбиталь. Применяя правила В.Клечковского, нетрудно понять, что 4d– и 4f–орбитали реально имеют более высокую энергию, чем некоторые орбитали пятого и даже шестого энергетического уровня! (не приведены в таблице и на энергетической схеме). Все это косвенно указывает на то, что постепенно уменьшается разница между разными уровнями, но одновременно
Таблица 1.4
Применение правил Клечковского
для определения порядка заселения АО электронами
|
Номер энергетического уровня |
Название АО |
n |
l |
n + l |
Очередность заселения АО |
|
|
|
|
|
|
|
|
первый |
1s |
1 |
0 |
1 |
1 |
|
|
|
|
|
|
|
|
второй |
2s 2рx;2py;2pz |
2 2 |
0 1 |
2 3 |
2 3 |
|
|
|
|
|
|
|
|
третий |
3s 3рx;3py;3pz 3dxy; 3dxz; 3dyz; 3dx2–y2; 3dz2 |
3 3 3 |
0 1 2 |
3 4 5 |
4 5 7 |
|
|
|
|
|
|
|
|
четвертый |
4s 4р–орбитали 4d–орбитали 4f–орбитали |
4 4 4 4 |
0 1 2 3 |
4 5 6 7 |
6 8 10 13/14 |
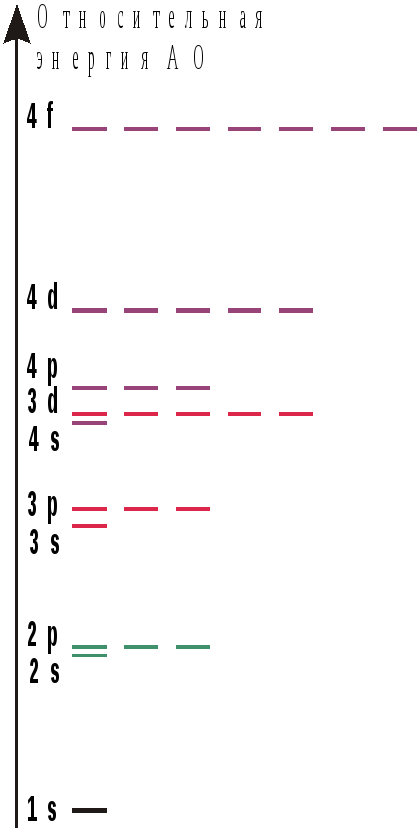
усиливается энергетическая разница между подуровнями, особенно между р– и d–орбиталями (d– и f–орбиталями) одного энергетического уровня.
Рис.
1.10 – Примерные соотношения энергий
подуровней первых четырех энергетических
уровней.
Следующим важным правилом, определяющим электронное строение атомов, является принцип или запрет В.Паули:
в атоме не может быть даже двух электронов с одинаковым набором всех четырех квантовых чисел.
Обоснование принципа В.Паули выходит за рамки данного пособия, но следует иметь в виду, что данное утверждение является абсолютно категоричным, не допускающим исключения.
Из запрета В.Паули следует, что на каждой атомной орбитали может "находиться" на более двух электронов с противоположными по знаку спиновыми квантовыми числами.2 Такие электроны называют спаренными, в отличие от одиночных (неспаренных) электронов. Часто при
а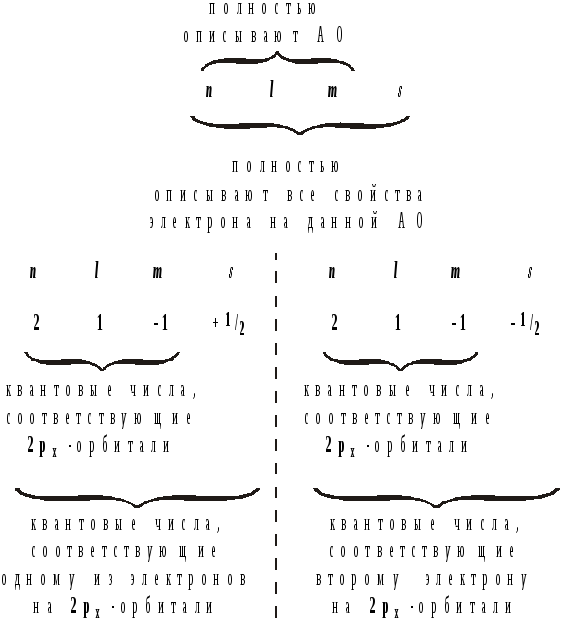 нализе
электронного строения упоминаются и
"пустые
АО".
Справедливость следствия из принципа
В.Паули можно продемонстрировать, если,
например, рассмотреть какие квантовые
числа описывают движение электронов
на 2рx-орбитали:
нализе
электронного строения упоминаются и
"пустые
АО".
Справедливость следствия из принципа
В.Паули можно продемонстрировать, если,
например, рассмотреть какие квантовые
числа описывают движение электронов
на 2рx-орбитали:
Схематично орбитали и электроны на них изображают следующим образом:
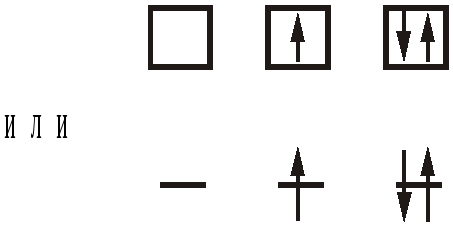
Применение принципа минимума энергии и принципа В.Паули позволяет правильно заселить только 1s- и 2s-орбитали, т.к. следом за ними по энергии идут три орбитали 2р-подуровня, которые различаются только взаимным расположением в пространстве. Очередность их заполнения определяется правилом В.Хунда:
орбитали одного энергетического подуровня заселяются электронами так, чтобы абсолютное значение (модуль) суммы спиновых чисел был максимальным.
Т.е. подразумевается, что поначалу все 2р-орбитали равноправны (равновыгодны) и первый электрон может быть размещен на любой из них (спиновое квантовое число может быть произвольным):

Следующий электрон из-за межэлектронного отталкивания "будет располагаться" на одной из двух вакантных орбиталей (будет создавать собственное электронное облако), причем спиновые квантовые числа двух электронов должны совпадать:
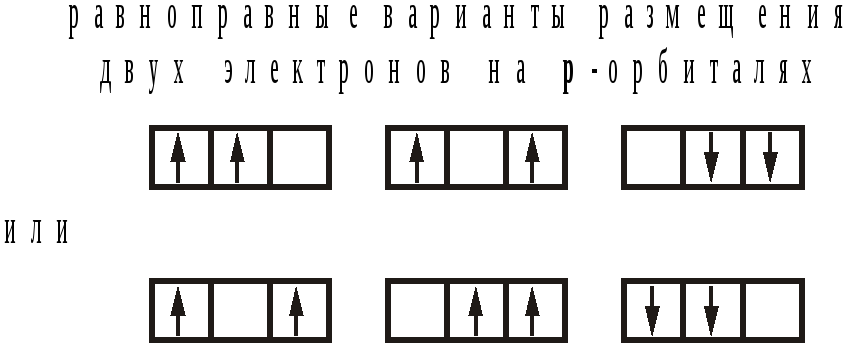
Для размещения трех электронов на р-орбиталях имеется только два энергетически выгодных варианта:
![]()
В обоих случаях модуль суммы спиновых квантовых чисел составляет 3/2. При этом все три орбитали вновь становятся абсолютно равноправными, и четвертый электрон может быть размещен на любой из них. Для соблюдения принципа В.Паули требуется, чтобы спиновые квантовые числа электронов на одной орбитали были различны, например:
![]() .
.
Из-за особых межэлектронных взаимодействий повышенной устойчивостью отличаются электронные конфигурации с полузаполненными и полностью заполненными орбиталями одного подуровня: p3, p6, d5, d10 и т.п. Ради достижения таких состояний, как мы увидим позднее, порой происходят, так называемые, "электронные провалы" или "электронные проскоки" между близкими по энергии (n-1)d– и ns–орбиталями (например, между 3d– и 4s–орбиталями в атомах хрома и меди).
