
- •1. Стабильность Si-c-связей, влияние заместителей в связанном с атомом кремния остатке.
- •2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
- •3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений.
- •4. Способы получения и химические свойства литийорганических соединений.
- •5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта.
- •6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами.
- •7. Номенклатура фосфорорганических соединений и органических производных серы.
- •8. Роль растворителей при получении литий- и магнийорганических соединений.
- •9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса.
- •10. Способы получения, токсические характеристики и практическое использование органических производных свинца
- •11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
- •12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов.
- •13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
- •1) Получение:
- •2) Получение силамепробамата
- •3) Эффект замены
- •14. Метаболизм кремнийорганических соединений.
- •15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров
- •16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты.
- •17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки.
- •18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
- •19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных.
- •20. Получение кремнийорганических соединений
- •21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование.
- •22. Реакции Барта и Несмеянова.
- •23. Способы получения диэфиров фосфористой кислоты.
- •24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. Механизм выработки резистентности на примере карбофоса.
- •25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием.
- •27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений.
- •28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути.
- •29. Превращения функционализированных по β-положению кремнийорганических соединений.
- •30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера.
- •31. Способ получения и биологическая активность силатранов
- •32. Способы получения и биологическая активность органических производных германия, герматраны.
- •33. Получение триариловых и триалкиловых эфиров фосфористой кислоты.
- •34. Способы получения и практическое использование оловоорганических соединений.
- •35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция.
- •36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан
- •37. Механизм реакции Михаэлиса-Беккера, получение натриевой соли диалкилфосфористой кислоты, ее реакционная способность, побочные продукты в реакции Михаэлиса- Беккера.
- •38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза
- •39. Способы получения и свойства борорганических соединений.
- •40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности.
- •41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов.
- •43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим.
- •44.Синтез и свойства тиольных соединений алифатического ряда
- •46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата.
- •47. Синтез и свойства тиольных соединений ароматического ряда.
- •48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
- •49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера.
- •50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера.
- •51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности.
- •52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид.
- •53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение о-метил-о-этилового эфира хлорангидрида тиофосфорной кислоты.
- •54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило жмко в реакции их солей с органическими галогенидами
- •55. Получение трифенилфосфина, образование илидов трифенилфосфония, механизм реакции Виттига. Синтез сквалена по реакции Виттига.
- •56. Реакция Хорнера-Вадсворта-Эммонса, синтез фосфонацетатов по реакции Михаэлиса-Арбузова и по реакции Михаэлиса-Беккера.
- •57. Способы получения и свойства сульфокислот алифатического и ароматического ряда.
- •58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена.
- •59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента
- •60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина.
8. Роль растворителей при получении литий- и магнийорганических соединений.
Литий
Основной способ получения литийорганических соединений основан на реакции 1)металлического лития с соответствующим галогенидом. Течение этой реакции во многом определяется природой галогена и используемым растворителем
Все литийорганические соединения, за исключением метиллития и фениллития, растворимы в апротонных органических растворителях. Это связано с тем, что они образуют ассоциаты, в которых понижена полярность связи атома лития с атомом углерода.
В растворах в образовании координационных связей в кластерах литийорганических соединений могут принимать участие и молекулы растворителей. При переходе от малоосновных растворителей к более основным степень ассоциации органических производных лития снижается.
При выборе растворителя для проведения реакции органического галогенида с металлическим литием надо учитывать особенности, связанные с его очисткой от пероксидов и с освобождением от следов воды. Большое значение для растворителя имеют также температура кипения и температура перехода в кристаллическое состояние. Так, например, легко чистятся и абсолютируются углеводороды, но циклогексан и бензол с температурой плавления соответственно 6,5 и 5,5 °С редко используются для работ с литийорганическими соединениями, так как последующие превращения органических производных лития чаще всего протекают при минусовых температурах. Хорошим растворителем для получения литийорганических соединений является диэтиловый (серный) эфир. Он не так легко, как считается, реагирует с ними. Во всяком случае в течение дня в среде диэтилового эфира можно провести как получение литийорганического соединения, так и реакцию с его участием. Высокое давление паров эфира также играет положительную роль – создаваемая ими «подушка» достаточно хорошо защищает литийорганическое соединение от контакта с воздухом и позволяет работать без заполнения аппаратуры азотом или аргоном. Альтернативой эфиру может служить тетрагидрофуран, но его трудно абсолютировать. Обычно его перегоняют над алюмогидридом лития или добавляют к высушенному над твёрдой щелочью тетрагидрофурану раствор реактива Гриньяра, взаимодействующего с остающимися в высушенном над щелочью тетрагидрофуране водой и спиртами. К недостаткам тетрагидрофурана как растворителя для реакций с литийорганическими соединениями можно отнести его сравнительно высокую реакционную способность по отношению к этим реагентам и недостаточно низкую температуру плавления –65 °С, осложняющую проведение реакций при охлаждении сухим льдом (–70°С).
Хорошие результаты получаются при проведении реакций в смесях растворителей, так, например, тетрагидрофуран можно использовать в смеси с углеводородными растворителями. В частности, для работы при низких температурах можно брать смесь эфира, тетрагидрофурана и пентана (или петролейного эфира) в соотношении 4:4:1. Редко используются для работы с литийорганическими соединениями среды, содержащие третичные амины, но в отдельных случаях их можно добавлять в качестве промоторов.
Реактивы Гриньяра
Реактивы Гриньяра легко получаются из соответствующих галогенидов и металлического магния при отсутствии в среде для проведения реакции следов воды и других протонодонорных веществ. Важно, что реактивы Гриньяра удобны в обращении. Для их получения можно использовать практически любые алифатические и ароматические галогениды, за исключением, конечно, фторидов. Реакция протекает в соответствии с общей схемой:
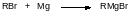
Накопленный опыт по проведению реакции Гриньяра показал, что растворитель играет важную роль при получении магнийорганических соединений. Более всего для этого подходит диэтиловый эфир, но можно использовать также дипропиловый, дибутиловый и диизопентиловый эфиры, а также тетрагидрофуран и диоксан. В качестве растворителя могут быть использованы ацетали формальдегида, например, диизопропоксиметан и диизобутоксиметан:
-

и

Используемый для проведения реакции эфир должен быть абсолютным, т.е. он должен быть очищен от влаги и спирта. Для этого эфир в течение достаточно длительного времени выдерживают над металлическим натрием. Количество растворителя должно соответствовать образованию раствора реактива Гриньяра с концентрацией от 1 до 2 молей в литре.
Простые эфиры выполняют функцию растворителя для образующегося магнийорганического соединения, которое чаще всего нерастворимо в других инертных органических растворителях. Переходом магнийорганического соединения в раствор поддерживается свободная поверхность металлического магния. Магнийорганическое соединение растворяется в эфире в виде аддукта, экзотермический эффект образования которого поддерживает реакционную массу в состоянии кипения. Эфираты продуктов реакции магния с органическими галогенидами могут быть выделены в виде бесцветных кристаллических веществ состава, например, R2Mg∙MgX2∙4(C2H5)2O. Состав органических соединений магния в эфирном растворе представляется динамическим равновесием Шленка:

При этом соотношение между алкилмагнийгалогенидом и диалкилмагнием может меняться в зависимости от растворителя. Так, например, в диоксане повышено содержание диалкилмагния из-за того, что хлорид магния образует с диоксаном нерастворимое комплексное соединение, выводящее неорганический хлорид из равновесия. В диэтиловом эфире реактивы Гриньяра с ионами брома и иода находятся в виде мономеров, а в виде димеров они находятся в тех случаях, когда атом галогена представлен хлором или фтором. В тетрагидрофуране все реактивы Гриньяра находятся преимущественно в мономерном состоянии. Однако особенности межмолекулярных взаимодействий у магнийорганических соединений практически не сказываются на их реакционной способности.
Реактивы Гриньяра растворимы во многих апротонных растворителях с атомами кислорода или азота, образующими донорно-акцепторные связи с атомами магния. В сравнении с литийорганическими соединениями реактивы Гриньяра менее оснóвны, а их растворы в эфире достаточно стабильны при комнатной температуре или даже при повышенных температурах.
