
- •1. Стабильность Si-c-связей, влияние заместителей в связанном с атомом кремния остатке.
- •2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
- •3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений.
- •4. Способы получения и химические свойства литийорганических соединений.
- •5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта.
- •6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами.
- •7. Номенклатура фосфорорганических соединений и органических производных серы.
- •8. Роль растворителей при получении литий- и магнийорганических соединений.
- •9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса.
- •10. Способы получения, токсические характеристики и практическое использование органических производных свинца
- •11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
- •12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов.
- •13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
- •1) Получение:
- •2) Получение силамепробамата
- •3) Эффект замены
- •14. Метаболизм кремнийорганических соединений.
- •15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров
- •16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты.
- •17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки.
- •18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
- •19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных.
- •20. Получение кремнийорганических соединений
- •21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование.
- •22. Реакции Барта и Несмеянова.
- •23. Способы получения диэфиров фосфористой кислоты.
- •24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. Механизм выработки резистентности на примере карбофоса.
- •25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием.
- •27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений.
- •28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути.
- •29. Превращения функционализированных по β-положению кремнийорганических соединений.
- •30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера.
- •31. Способ получения и биологическая активность силатранов
- •32. Способы получения и биологическая активность органических производных германия, герматраны.
- •33. Получение триариловых и триалкиловых эфиров фосфористой кислоты.
- •34. Способы получения и практическое использование оловоорганических соединений.
- •35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция.
- •36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан
- •37. Механизм реакции Михаэлиса-Беккера, получение натриевой соли диалкилфосфористой кислоты, ее реакционная способность, побочные продукты в реакции Михаэлиса- Беккера.
- •38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза
- •39. Способы получения и свойства борорганических соединений.
- •40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности.
- •41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов.
- •43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим.
- •44.Синтез и свойства тиольных соединений алифатического ряда
- •46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата.
- •47. Синтез и свойства тиольных соединений ароматического ряда.
- •48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
- •49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера.
- •50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера.
- •51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности.
- •52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид.
- •53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение о-метил-о-этилового эфира хлорангидрида тиофосфорной кислоты.
- •54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило жмко в реакции их солей с органическими галогенидами
- •55. Получение трифенилфосфина, образование илидов трифенилфосфония, механизм реакции Виттига. Синтез сквалена по реакции Виттига.
- •56. Реакция Хорнера-Вадсворта-Эммонса, синтез фосфонацетатов по реакции Михаэлиса-Арбузова и по реакции Михаэлиса-Беккера.
- •57. Способы получения и свойства сульфокислот алифатического и ароматического ряда.
- •58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена.
- •59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента
- •60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина.
48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
Речь идет про химию БАВ, поэтому тут ни слова про полимеры. Но если что там всякие силиконы и т.д.
В общем случае биологически активные кремнийорганические соединения можно разделить на три основные группы:
- первая группа включает силилированные производные известных органических соединений, используемых в качестве лекарств;
- вторая группа биоактивных органических производных кремния представлена кремнийорганическими соединениями, у которых нет никаких аналогов в обычной органической химии;
- третья группа включает соединения, строение которых аналогично строению известных биоактивных соединений, но атомы кремния в их структурах занимают место атомов углерода. Данное направление называют «Sila Pharmaca»
1) Практически все силилированные производные соединений с известной фармакологической активностью представлены веществами, в составе которых триметилсилильные или диметилтретбутилсилильные группы связаны с атомами кислорода, азота или углерода. Соответствующие силильные производные биоактивных соединений заметно отличаются от исходных веществ по физико-химическим свойствам. В частности, они становятся более липофильными, в то же время они легко гидролизуются водой, превращаясь в активные фармсубстанции. Такие триметилсилильные производные были получены, например, на основе местного анестетика лидокаина, жаропонижающего средства парацетамола и других активных начал лекарственных средств. Вызванное силилированием изменение гидрофильно-липофильного баланса молекул приводит к улучшению фармакокинетических параметров. Блокирование полярных центров в молекуле и постепенное гидролитическое отщепление триметилсилильных групп в жидких средах организма представляет собой перспективный путь к получению новых пролекарств, которые проникают через липидные зоны клеточных мембран и постепенно выделяют активное вещество в результате гидролиза.
-Преимущество такого подхода к модификации активных начал показано в экспериментах с триметилсилильным производным тестостерона

В стандартном опыте с кастрированными самцами крыс с введением инъекционным путём тестостерона и его триметилсилильного производного была продемонстрирована эффективность соединения с защищённой гидроксильной группой, показавшего более высокую андрогенную и миотропную активность.
-Интересные данные были получены на силилированных производных 2- дибутиламиноэтанола, проявляющего свойства репеллента по отношению к эктопаразитам. Полученные на основе этого соединения силоксановые производные значительно превосходили 2-дибутиламиноэтанол по репеллентной активности и по длительности защитного действия в опытах на крысиных блохах Xenopsylla cheopis. При этом максимальную эффективность показало соединение формулы:

В дозе 20 г/м2 этот аминосилоксан был в полтора раза эффективнее исходного аминоэтанольного репеллента, а продолжительность защитного действия этого кремнийорганического соединения, составлявшая несколько часов для аминоэтанола, увеличивалась до 12 дней.
-Некоторые силилированные амидные производные индометацина – лекарства с широким спектром действия, относящегося к нестероидным противовоспалительным средствам, – были получены с целью повышения эффективности и безопасности этого препарата при использовании его в качестве противоракового средства. Индометацин блокирует обе циклооксигеназы СОХ-1 и СОХ-2, что осложняет его лекарственное применение. Силилированные амидные производные индометацина (n = 1 и 3, R = CH3 и C6H5) были получены по схеме:

Изучение биологической активности полученных соединений показало, что они являются более избирательными ингибиторами циклооксигеназ: СОХ-2 блокируется ими на три порядка эффективнее, чем СОХ-1. Кроме того, силилированные производные индометацина оказались и лучшими цитостатиками для клеток злокачественных опухолей поджелудочной железы и клеток множественной миеломы. Введение силильных групп в известные активные соединения с образованием стабильных Si–C-связей не может быть использовано для получения пролекарств, но в то же время это ещё одна возможность модифицирования структуры с целью получения соединений с новыми свойствами.
2) Синтез и исследование биоактивности кремнийорганических соединений, у которых нет аналогов среди обычных органических соединений (или эти аналоги есть, но их биологическая активность неизвестна) представляет собой достаточно трудоёмкую работу. Тем не менее такие исследования ведутся, и уже получены сотни новых кремнийорганических соединений с интересными видами фармакологической активности, некоторые из которых будут представлены далее.
-Циклические органосилоксаны с невысокими молекулярными массами могут взаимодействовать с биомишенями. Так, например, оказалось, что циклотетрасилоксаны, получаемые из соответствующего трисилоксана и дихлордиметилсилана по схеме:

оказывают ярко выраженный эффект на мужскую и женскую репродуктивную системы. В частности, они вызывают атрофию клеток мужской эндокринной системы, что позволяет использовать их в качестве средств для лечения опухолей предстательной железы. Одно из таких соединений с трансоидным расположением фенильных групп зарегистрировано в качестве лекарственного средства под названием Цисобитан.
-Стабильный дифенилсиландиол, аналогов для которого в химии углерода нет, показывает хорошую антиконвульсантную активность, сравнимую с активностью известного противоэпилептического средства дифенилгидантоина (дифентоин, дифенин):

-В 1960 г. (A. B. Finestone, США) был запатентован способ получения одного из самых интересных и необычных типов кремнийорганических соединений – каркасных силатранов:

-Фенилсилатран неожиданно проявил очень высокую токсичность для млекопитающих (ЛД50 0,33 мг/кг, мыши, в.б.), а для пресмыкающихся, растений и микроорганизмов арилсилатраны оказались малотоксичными. Хорошие токсикологические показатели позволяют использовать арилсилатраны в качестве средств для борьбы с грызунами. Так, например, при введении через рот эти вещества на порядок менее токсичны для уток и обезьян.
В настоящее время считается, что механизм действия арилсилатранов основан на блокировке хлорных каналов ГАМК-эргической нервной системы, передающей сигналы торможения. Другие металлатраны оказались малотоксичными соединениями.
-Ускоренное заживление ран вызывают малотоксичные 1-хлорметил- силатран (Мивал) и 1-этоксисилатран. Хлорметилсилатран (20 %) вместе с ауксином 2- метилфеноксиуксусной кислотой (80 %) входит в состав разработанного в России регулятора роста растений Мивал-Агро, где он, очевидно, играет роль источника биодоступного кремния. Кроме того, мази с 1-хлорметилсилатраном и 1-этоксисилатраном стимулируют рост волос. В СССР были проведены широкие клинические испытания, показавшие перспективность использования этих соединений в качестве средств для лечения самых разных видов алопеции (облысения).
-Наряду с ярко выраженной репеллентной активностью многие аминосиланы и силоксаны проявляют противомикробные и противогрибковые свойства. В частности, соединения общей формулы
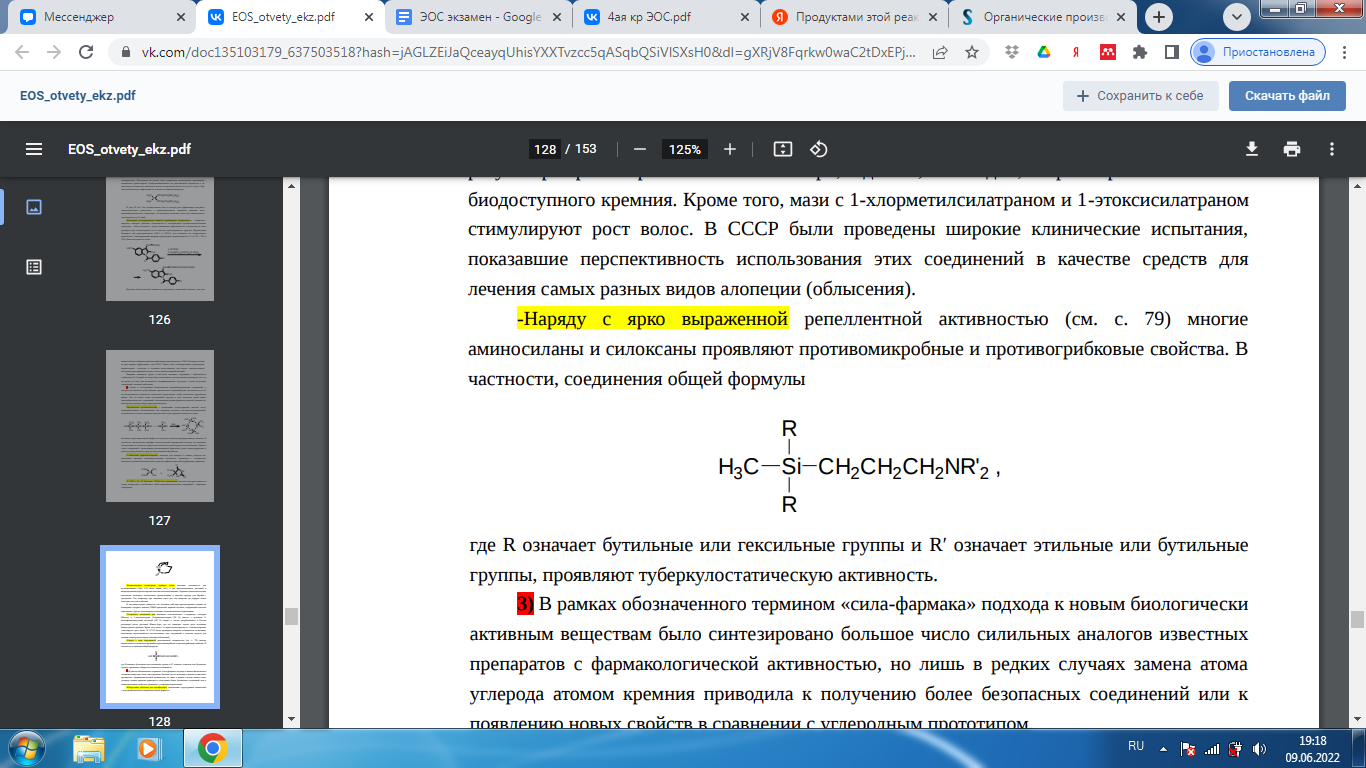
, где R означает бутильные или гексильные группы и R′ означает этильные или бутильные группы, проявляют туберкулостатическую активность.
3) В рамках обозначенного термином «сила-фармака» подхода к новым биологически активным веществам было синтезировано большое число силильных аналогов известных препаратов с фармакологической активностью, но лишь в редких случаях замена атома углерода атомом кремния приводила к получению более безопасных соединений или к появлению новых свойств в сравнении с углеродным прототипом. -Интересным объектом для модификации силильными структурными элементами стали трициклические соединения общей формулы,

где R означает γ-аминозамещённую пропильную группу и Х означает атом серы, кислорода, пропилиденовую, этиленовую и другие группы. В зависимости от природы структурного элемента Х трициклическая основа молекулы может быть почти планарной или же угловой, когда сконденсированные с центральным гетероциклом бензольные кольца лежат в пересекающихся под углом плоскостях. Планарные структуры проявляют антипсихотическую активность, тогда как угловые являются прежде всего антидепрессантами (тимолептиками).
Эти данные по зависимости активности от строения послужили основой для получения широкого ряда структурных аналогов этих соединений с силильными группами в шестичленном или семичленном центральном гетероциклическом структурном элементе (Х = Si(CH3)2, СН2Si(CH3)2, Si(CH3)C6H5, Si(CH3)H, Si(CH3)OH и др.). Все полученные соединения проявляли антипсихотическую или седативную активность, но никаких особых преимуществ в сравнении с углеродными аналогами они не показали.
-Определённый интерес представляют соединения с двумя четвертичными аммонийными группами, которые были получены как аналоги алкалоида кураре с парализующим действием. У этих блокаторов нервномышечной передачи наблюдается зависимость активности от расстояния, разделяющего четвертичные атомы азота. Пары четвертичных атомов азота в этих соединениях разделены десятью атомами углерода (декаметоний) или восемью атомами углерода и двумя атомами кислорода (дитилин). Практически все полученные соединения оказались примерно на порядок более активными, чем декаметоний. В качестве примера приводится ajhvekf одного из кремнийорганических аналогов декаметония.

Синтезированное по представленной схеме соединение оказалось очень эффективным блокатором нервномышечной передачи с деполяризующим действием.
-Широким спектром биологической активности отличаются синтетические структурные аналоги пространственных изомеров ретиноевой кислоты. В частности, они могут использоваться для лечения некоторых болезней кожи и в области онкологии. Одним из вошедших в практику агонистов ретиноевых рецепторов является 1-(1,1,4,4,7-пентаметил-1,2,3,4-тетрагидронафт-6-ил)-1-(4-карбоксифенил)-этилен (таргретин, бексаротен):

Для синтеза его кремнийорганического аналога используют цепочку превращений, в которой исходным соединением является доступный 1,2-бис(хлордиметилсилил)этан,реагирующий с этинилмагнийбромидом с образованием 1,2-бис(диметилэтинилсилил)этана (цепочку не вставил, просили лишь примеры, и так дохуя выходит)

Омыление сложноэфирной группы в полученном соединении гидроксидом калия приводит к образованию соли дисила-бексаротена, который оказался эффективным агонистом ретиноидных рецепторов, как и его прототип с атомами углерода вместо атомов кремния.
-В ряду ингибиторов обратного захвата серотонина и катехоламинных нейромедиаторов некоторые силановые производные оказались более избирательными в сравнении с углеродными аналогами. Так, например, силильный аналог антидепрессанта венлафаксина – силавенлафаксин блокирует преимущественно обратный захват норадреналина и дофамина:
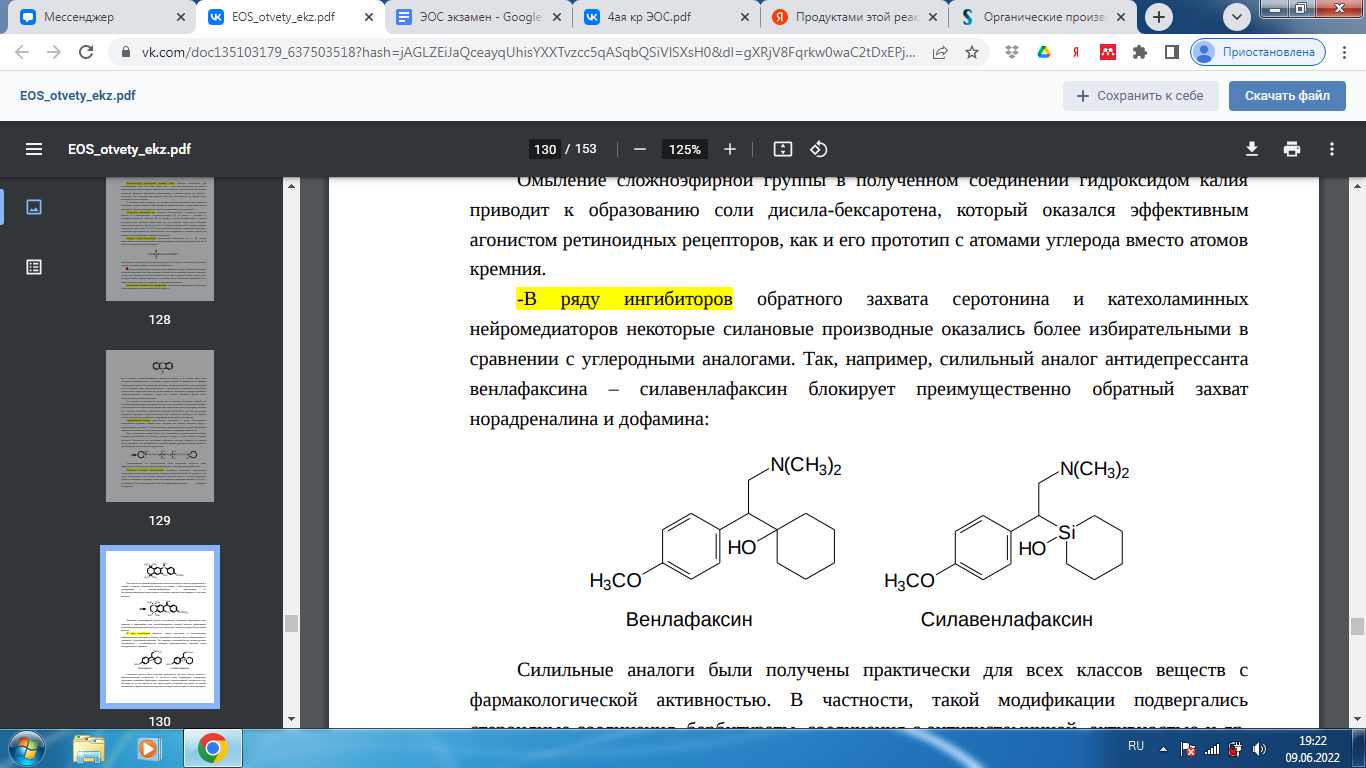
Силильные аналоги были получены практически для всех классов веществ с фармакологической активностью. В частности, такой модификации подвергались стероидные соединения, барбитураты, соединения с антигистаминной активностью и др. Несмотря на то что многие из них превосходили углеродные прототипы по многим показателям, в фармакологическую практику не введён пока ни один из таких препаратов. Это связано, очевидно, со сложностью их получения в требуемых для практического использования количествах
