
- •1. Стабильность Si-c-связей, влияние заместителей в связанном с атомом кремния остатке.
- •2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
- •3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений.
- •4. Способы получения и химические свойства литийорганических соединений.
- •5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта.
- •6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами.
- •7. Номенклатура фосфорорганических соединений и органических производных серы.
- •8. Роль растворителей при получении литий- и магнийорганических соединений.
- •9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса.
- •10. Способы получения, токсические характеристики и практическое использование органических производных свинца
- •11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
- •12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов.
- •13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
- •1) Получение:
- •2) Получение силамепробамата
- •3) Эффект замены
- •14. Метаболизм кремнийорганических соединений.
- •15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров
- •16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты.
- •17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки.
- •18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
- •19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных.
- •20. Получение кремнийорганических соединений
- •21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование.
- •22. Реакции Барта и Несмеянова.
- •23. Способы получения диэфиров фосфористой кислоты.
- •24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. Механизм выработки резистентности на примере карбофоса.
- •25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием.
- •27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений.
- •28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути.
- •29. Превращения функционализированных по β-положению кремнийорганических соединений.
- •30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера.
- •31. Способ получения и биологическая активность силатранов
- •32. Способы получения и биологическая активность органических производных германия, герматраны.
- •33. Получение триариловых и триалкиловых эфиров фосфористой кислоты.
- •34. Способы получения и практическое использование оловоорганических соединений.
- •35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция.
- •36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан
- •37. Механизм реакции Михаэлиса-Беккера, получение натриевой соли диалкилфосфористой кислоты, ее реакционная способность, побочные продукты в реакции Михаэлиса- Беккера.
- •38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза
- •39. Способы получения и свойства борорганических соединений.
- •40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности.
- •41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов.
- •43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим.
- •44.Синтез и свойства тиольных соединений алифатического ряда
- •46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата.
- •47. Синтез и свойства тиольных соединений ароматического ряда.
- •48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
- •49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера.
- •50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера.
- •51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности.
- •52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид.
- •53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение о-метил-о-этилового эфира хлорангидрида тиофосфорной кислоты.
- •54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило жмко в реакции их солей с органическими галогенидами
- •55. Получение трифенилфосфина, образование илидов трифенилфосфония, механизм реакции Виттига. Синтез сквалена по реакции Виттига.
- •56. Реакция Хорнера-Вадсворта-Эммонса, синтез фосфонацетатов по реакции Михаэлиса-Арбузова и по реакции Михаэлиса-Беккера.
- •57. Способы получения и свойства сульфокислот алифатического и ароматического ряда.
- •58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена.
- •59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента
- •60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина.
18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
Взаимодействие альфа-галогензамещённых кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова)
Ещё одна важная реакция триалкилфосфитов представлена их взаимодействием с α-галогензамещенными карбонильными соединениями. В этом случае основное направление реакции в значительной мере определяется природой атома галогена. Так, например, при взаимодействии триалкилфосфита с хлорацетоном основным продуктом реакции (с выходом около 90%) становится соответствующий изопропениловый эфир диалкилфосфорной кислоты (реакция Перкова, W.Perkow, 1952 г.):

В то же время реакция триалкилфосфита с бромацетоном приводит к смеси продукта реакции Перкова и продукта реакции Михаэлиса-Арбузова в примерно равных количествах, тогда как взаимодействие триалкилфосфита с иодацетоном протекает преимущественно по схеме реакции Михаэлиса-Арбузова с образованием соответствующего ацетонилфосфоната с выходом около 90%:

Механизм реакции Перкова может быть представлен двумя схемами. В соответствии с одной из них первичным продуктом взаимодействия является квазифосфониевое соединение, образующееся в результате атаки нуклеофильного атома фосфора по атому углерода карбонильной группы, которое далее претерпевает перегруппировку с образованием РО-связи и стабилизируется с отщеплением алкилбромида по схеме:

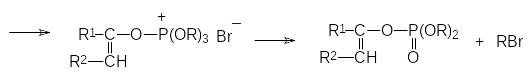
Если α-галогензамещенное карбонильное соединение может отщеплять галоген в виде положительно заряженного иона и превращаться в стабилизиро-ванный сопряжением анион енольной формы кетона, то механизм реакции Перкова представляется как атака образующегося при этом квазифосфониевого соединения непосредственно по атому кислорода:

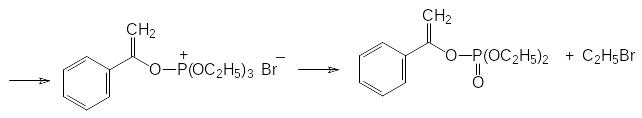
Винилфосфаты в качестве ингибиторов холинэстеразы
*По аналогии с представленной выше фосфонат-фосфатной перегруппировкой продуктов реакции Абрамова хлорофос при действии оснований превращается в более летучий и более токсичный жидкий 2,2‑дихлорвинилфосфат (дихлофос, ДДВФ), используемый для борьбы с летающими насекомыми:

*Другой механизм летального синтеза отвечает за антихолинэстеразную активность диметилового эфира 1-гидрокси-2,2,2-трихлорэтилфосфоновой кислоты с ЛД50 для крыс 560 мг/кг. Это соединение, известное под названием хлорофос, диптерекс и др., в присутствии даже слабых оснований претерпевает фосфонат-фосфатную перегруппировку с отщеплением молекулы хлористого водорода:

В результате дегидрохлорирования не соответствующий формуле Шрадера фосфонат превращается в фосфорилированный енол, который уже может выступать в качестве фосфорилирующего средства, поскольку в его составе появляется уходящая группа, соответствующая остатку слабой кислоты. В данном случае речь идет о енольной форме дихлоруксусного альдегида.
*По реакции Перкова были получены и многие другие винилфосфаты, например, на основе галогензамещенных производных ацетоуксусной кислоты или хлорированных ацетофенонов, но они оказались слишком токсичными. Так, например, при взаимодействии диметилхлорфосфата с натриевым производным ацетоуксусного эфира или триметилфосфита с хлорацетоуксусным эфиром образуется диметилфосфат енольной формы ацетоуксусного эфира (фосдрин, мевинфос, ЛД50 3,5 мг/кг, крысы), с хорошей инсектицидной активностью:

И всё же высокая острая токсичность этого соединения не позволила использовать его в широких масштабах. Интересно, что пространственное строение этого соединения решающим образом сказывается на его инсектицидной активности: цис-изомер этого соединения на два порядка более активен, чем транс-изомер.
Менее токсичен для теплокровных (для крыс ЛД50 22 мг/кг) дикротофос, образующийся по аналогичной схеме из диметилхлорфосфата и натриевого производного диметиламида ацетоуксусной кислоты:

**Согласно формуле Шрадера, фосфорорганическое соединение должно иметь уходящую группу, соответствующую остатку слабой кислоты. У дихлофоса У-фрагмент как раз является остатоком слабой кислоты, тк представляет собой спирт, у которого имеются электроноакцепторные заместители. Аналогично тому У-фрагмент у кротофоса.
