
- •1. Стабильность Si-c-связей, влияние заместителей в связанном с атомом кремния остатке.
- •2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
- •3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений.
- •4. Способы получения и химические свойства литийорганических соединений.
- •5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта.
- •6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами.
- •7. Номенклатура фосфорорганических соединений и органических производных серы.
- •8. Роль растворителей при получении литий- и магнийорганических соединений.
- •9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса.
- •10. Способы получения, токсические характеристики и практическое использование органических производных свинца
- •11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
- •12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов.
- •13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
- •1) Получение:
- •2) Получение силамепробамата
- •3) Эффект замены
- •14. Метаболизм кремнийорганических соединений.
- •15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров
- •16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты.
- •17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки.
- •18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
- •19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных.
- •20. Получение кремнийорганических соединений
- •21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование.
- •22. Реакции Барта и Несмеянова.
- •23. Способы получения диэфиров фосфористой кислоты.
- •24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. Механизм выработки резистентности на примере карбофоса.
- •25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием.
- •27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений.
- •28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути.
- •29. Превращения функционализированных по β-положению кремнийорганических соединений.
- •30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера.
- •31. Способ получения и биологическая активность силатранов
- •32. Способы получения и биологическая активность органических производных германия, герматраны.
- •33. Получение триариловых и триалкиловых эфиров фосфористой кислоты.
- •34. Способы получения и практическое использование оловоорганических соединений.
- •35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция.
- •36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан
- •37. Механизм реакции Михаэлиса-Беккера, получение натриевой соли диалкилфосфористой кислоты, ее реакционная способность, побочные продукты в реакции Михаэлиса- Беккера.
- •38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза
- •39. Способы получения и свойства борорганических соединений.
- •40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности.
- •41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов.
- •43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим.
- •44.Синтез и свойства тиольных соединений алифатического ряда
- •46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата.
- •47. Синтез и свойства тиольных соединений ароматического ряда.
- •48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
- •49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера.
- •50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера.
- •51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности.
- •52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид.
- •53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение о-метил-о-этилового эфира хлорангидрида тиофосфорной кислоты.
- •54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило жмко в реакции их солей с органическими галогенидами
- •55. Получение трифенилфосфина, образование илидов трифенилфосфония, механизм реакции Виттига. Синтез сквалена по реакции Виттига.
- •56. Реакция Хорнера-Вадсворта-Эммонса, синтез фосфонацетатов по реакции Михаэлиса-Арбузова и по реакции Михаэлиса-Беккера.
- •57. Способы получения и свойства сульфокислот алифатического и ароматического ряда.
- •58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена.
- •59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента
- •60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина.
13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
1) Получение:
Кремнийорганические соединения могут быть получены по реакции галогенидов кремния с металлорганическими соединениями

Действие дифенилртути на тетрахлорид кремния приводит к получению фенилтрихлорсилана:
![]()
В определённых случаях реакции хлорсиланов проводят с литийорганическими соединениями.
![]()
Дисиланы могут быть также получены действием таких металлов, как натрий, литий или магний, на хлорсиланы с тремя органическими остатками:

Образование Si–C-связи наблюдается также в реакции металлированных калием, натрием или литием силанов с арил- или алкилгалогенидами, например:

Металлированные силаны реагируют с эпоксидами с раскрытием оксиранового цикла:


Часто для получения элементоорганических соединений используют взаимодействие галогенидов соответствующих элементов с алкил- или арилгалогенидами и металлическим натрием.

![]()
В отдельных случаях можно проводить прямое силилирование углеводородов тетрахлоридом кремния

Хлорметилсиланы образуются в реакции хлорсиланов с диазометаном

И всё же наиболее интересны реализуемые в промышленном масштабе реакции алкил- и арилгалогенидов с элементным кремнием
![]()
2) Получение силамепробамата
В качестве исходного продукта берут триметилхлорсилан. Его хлорируют при облучении УФ-светом, затем действием пропилмагнийбромида переводят полученный бис(хлорметил)-метилхлорсилан в бис(хлорметил)метилпропилсилан:
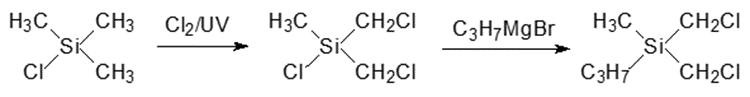
На следующей стадии действием ацетата калия в ледяной уксусной кислоте заменяют атомы хлора на ацетоксигруппы и в мягких условиях проводят гидрирование диацетатного производного в соответствующий диол алюмогидридом лития


Достаточно лабильны и кремнийорганические соединения с гидроксиметильными группами, поэтому для перевода их в карбаматные производные гидроксильные группы ацилируют фенилхлоркарбонатом в присутствии пиридина и после этого действием аммиака заменяют феноксигруппы на амидные:


3) Эффект замены
Рассчитанные значения для связей Si–Н, Si–S, Si–Si и для связей углерода с этими элементами хорошо согласуются с экспериментально определяемыми расстояниями между этими атомами. Однако для связей кремния с атомами азота, кислорода, хлора и фтора реальные расстояния оказываются значительно короче расчётных. Такое сокращение длин связей можно объяснить тем, что в соединениях тетракоординированного атома кремния с другим элементом с электроном на р-орбитали эта орбиталь может иметь область перекрывания с 3d‑орбиталью атома кремния по принципу (р→d)π связывания. В результате этого связь атома кремния с таким элементом (El) приобретает характер двойной связи, что можно представить резонансными структурами:

Доступностью свободных 3d‑орбиталей у атома кремния можно объяснить ещё одно различие между соединениями углерода и их аналогами с атомами кремния: трисилиламин N(SiН3)3 имеет плоскую (планарную) структуру, тогда как триметиламин N(СН3)3 имеет пирамидальное строение.
При изучении кислотности в парах R3СОН и R3SiOН, а также в парах (R3С)2NН и (R3Si)2NН получены дополнительные данные, подтверждающие возможность (р→р)π связывания.
В соответствии с существующими в органической химии представлениями о кислотности ОН-групп и NH-групп в соединениях такого типа она должна уменьшаться при переходе от атомов углерода к атомам кремния, поскольку атом углерода более электроотрицателен. Однако силанолы и вторичные силиламины представляют собой более сильные кислоты, чем соответствующие карбинолы и вторичные алкиламины
Связь атома кремния с фенильной группой с (р→р)π сопряжением влияет на распределение электронных плотностей в ароматической системе. В соответствии с этой моделью бензойная кислота с триметилсилильной группой в 4-положении показывает более высокую кислотность, чем можно было ожидать от индуктивного эффекта; п‑триметилсилилфенол также представляет собой более сильную кислоту, чем незамещённый фенол, а п-триметилсилиланилин демонстрирует пониженную основность в сравнении с незамещённым анилином.

Правда, влияние атома кремния на функциональные группы в органических соединениях можно охарактеризовать и без привлечения (р→р)π сопряжения. Так, например, в соединениях (СН3)3ССН2СООН и (СН3)3SiСН2СООН, а также (СН3)3ССН2NН2 и (СН3)3SiСН2NН2 кремнийорганические соединения представляют собой более слабую кислоту и соответственно более сильное основание. Эти эффекты можно объяснить и низкой электроотрицательностью атома кремния.
Введение изостерных углероду атомов кремния в известные биоактивные структуры позволяет оптимизировать фармакологическую активность, снижать токсичность и улучшать фармакокинетические показатели.
Увеличенный ковалентный радиус атома кремния примерно на 20 % увеличивает длину связей с другими атомами по сравнению с атомом углерода. Следствием этого становится изменение углов связей и конформаций в циклических структурных элементах. С введением триметилсилильных, диметилтретбутилсилильных и диметилфенилсилильных групп растёт липофильность молекул и связанная с этим способность модифицированных силильными группами молекул проходить через ткани и клеточные мембраны. Кроме того, у атома кремния другой характер связей из-за доступности для гиперконъюгации 3d орбиталей и низколежащих Si−C или Si−X разрыхляющих орбиталей. Выше отмечалась невозможность формирования кратных связей у атома кремния. Следствием этого становится образование структур, которые не имеют аналогов у молекул, построенных только из атомов углерода.
Электроположительный характер атома кремния (в сравнении с атомами углерода, азота, кислорода и водорода) объясняет обратную поляризацию его связей с другими атомами по сравнению с атомом углерода. В медицинской химии это приводит к упрочнению водородных связей и к повышению кислотности ОН-связи в силанолах.
