
- •1. Стабильность Si-c-связей, влияние заместителей в связанном с атомом кремния остатке.
- •2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
- •3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений.
- •4. Способы получения и химические свойства литийорганических соединений.
- •5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта.
- •6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами.
- •7. Номенклатура фосфорорганических соединений и органических производных серы.
- •8. Роль растворителей при получении литий- и магнийорганических соединений.
- •9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса.
- •10. Способы получения, токсические характеристики и практическое использование органических производных свинца
- •11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны.
- •12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов.
- •13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях.
- •1) Получение:
- •2) Получение силамепробамата
- •3) Эффект замены
- •14. Метаболизм кремнийорганических соединений.
- •15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров
- •16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты.
- •17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки.
- •18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы.
- •19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных.
- •20. Получение кремнийорганических соединений
- •21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование.
- •22. Реакции Барта и Несмеянова.
- •23. Способы получения диэфиров фосфористой кислоты.
- •24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. Механизм выработки резистентности на примере карбофоса.
- •25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием.
- •27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений.
- •28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути.
- •29. Превращения функционализированных по β-положению кремнийорганических соединений.
- •30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера.
- •31. Способ получения и биологическая активность силатранов
- •32. Способы получения и биологическая активность органических производных германия, герматраны.
- •33. Получение триариловых и триалкиловых эфиров фосфористой кислоты.
- •34. Способы получения и практическое использование оловоорганических соединений.
- •35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция.
- •36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан
- •37. Механизм реакции Михаэлиса-Беккера, получение натриевой соли диалкилфосфористой кислоты, ее реакционная способность, побочные продукты в реакции Михаэлиса- Беккера.
- •38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза
- •39. Способы получения и свойства борорганических соединений.
- •40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности.
- •41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов.
- •43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим.
- •44.Синтез и свойства тиольных соединений алифатического ряда
- •46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата.
- •47. Синтез и свойства тиольных соединений ароматического ряда.
- •48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры.
- •49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера.
- •50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера.
- •51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности.
- •52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид.
- •53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение о-метил-о-этилового эфира хлорангидрида тиофосфорной кислоты.
- •54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило жмко в реакции их солей с органическими галогенидами
- •55. Получение трифенилфосфина, образование илидов трифенилфосфония, механизм реакции Виттига. Синтез сквалена по реакции Виттига.
- •56. Реакция Хорнера-Вадсворта-Эммонса, синтез фосфонацетатов по реакции Михаэлиса-Арбузова и по реакции Михаэлиса-Беккера.
- •57. Способы получения и свойства сульфокислот алифатического и ароматического ряда.
- •58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена.
- •59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента
- •60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина.
Оглавление
1. Стабильность Si-C-связей, влияние заместителей в связанном с атомом кремния остатке. 4
2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа. 6
3. Реакционная способность и стабильность металлорганических соединений. Основные способы получения металлорганических соединений. 11
4. Способы получения и химические свойства литийорганических соединений. 16
5. Получение алкиларсиновых кислот по реакции Мейера, получение ариларсиновых кислот по реакции Барта. 27
6. Реакции литий- и магнийорганических соединений с альдегидами, кетонами, сложными эфирами, ортоэфирами и нитрилами. 29
7. Номенклатура фосфорорганических соединений и органических производных серы. 30
8. Роль растворителей при получении литий- и магнийорганических соединений. 35
9. Исходные продукты для получения тиофосфатов с инсектицидной активностью (хлортиофосфаты и дитиофосфаты), получение фоксима и карбофоса. 40
10. Способы получения, токсические характеристики и практическое использование органических производных свинца 45
11. Гидролиз и ацидолиз эфиров кислот фосфора. Получение триметилсилильных эфиров кислот фосфора, реакция МакКенны. 48
12. Реакции ацидолиза эфиров кислот фосфора, ацидолиз при получении диалкилфосфитов, условия перегонки реакционных масс. Окисление и галогенирование диалкилфосфитов. 55
13. Получение кремнийорганических аналогов биологически активных веществ, получение силамепробамата. Эффект замены атома углерода на атом кремния в биоактивных соединениях. 60
14. Метаболизм кремнийорганических соединений. 66
15. Способы получении и свойства алюминийорганических соединений. Применение в производстве полимеров 69
16. Жидкость Кадэ. Хлорвинилхлорарсины, получение, токсические характеристики, механизм действия, антидоты. 74
17. Получение эфиров арилбороновых кислот и использование их в реакции Сузуки. 77
18. Взаимодействие α-галогензамещеных кетонов с триалкилфосфитами (реакция Перкова и Михаэлиса-Арбузова). Винилфосфаты в качестве ингибиторов холинэстеразы. 81
19. Механизм гербицидной активности глюфосината (фосфинотрицина), способы его получения. Токсичность и побочные эффекты для теплокровных. 85
20. Получение кремнийорганических соединений 87
21. Получение силиконовых полимеров, регуляция молекулярной массы, вулканизация. Их практическое использование. 89
22. Реакции Барта и Несмеянова. 92
23. Способы получения диэфиров фосфористой кислоты. 94
24. Примеры фосфорорганических соединений с инсектицидной активностью, получение диалкилхлортиофосфатов. механизм выработки резистентности на примере карбофоса. 98
25.Реакция Вюрца-Фиттига, механизм избирательности в варианте Фиттига. Промежуточные продукты в реакциях арилхлоридов с хлоридами элементов и металлическим натрием. 105
26. Присоединение диалкилфосфитов к кратным связям (С=С, С=О, С=N), реакция Абрамова и Пудовика. 107
27. Способы получения и свойства цинкорганических соединений, использование их в реакции Реформатского и для получения карбонильных соединений. 110
28. Ртутьорганические соединения. Способы получения и химические свойства. Гранозан (этилмеркурхлорид), токсичность органических производных ртути. 113
29. Превращения функционализированных по β-положению кремнийорганических соединений. 115
30. Ингибирование холинэстеразы соединениями с ацилирующей способностью, особенности ингибирования производными кислот фосфора, формула Шрадера. 117
31. Способ получения и биологическая активность силатранов 121
32. Способы получения и биологическая активность органических производных германия, герматраны. 122
33. Получение триариловых и триалкиловых эфиров фосфористой кислоты. 126
34. Способы получения и практическое использование оловоорганических соединений. 129
35. Механизм реакции Михаэлиса-Арбузова, реакционная способность исходных соединений, побочная реакция. 132
36. Способы получения мышьякорганических соединений, Реакция Бешама. Сальварсан 135
37. Механизм реакции Михаэлиса-Беккера, получение натриевой соли диалкилфосфористой кислоты, ее реакционная способность, побочные продукты в реакции Михаэлиса- Беккера. 140
38. Биологическая активность бисфосфонатов. Примеры и способы получения бисфосфонатных средств для лечения остеопороза 144
39. Способы получения и свойства борорганических соединений. 147
40. Реакция диалкилфосфитов с изоцианатами, побочная реакция. Получение кренайта, механизм биологической активности. 152
41. Получение илидных соединений из диалкилсульфидов и диметилсульфоксида, синтез на их основе оксиранов и циклопропанов. 155
42. Антихолинэстеразная активность фосфорорганических соединений. Обратимое и необратимое ингибирование холинэстеразы. Примеры обратимого и необратимого ингибирования в ряду фосфорорганических инсектицидов. 158
43. Реактивация ацилированной фосфорорганическими соединениями холинэстеразы производными гидроксиламина, оксимы в качестве антидотов и фоксим. 162
44.Синтез и свойства тиольных соединений алифатического ряда 165
45. 2-Хлорэтильные производные в ряду кремний- и фосфорорганических соединений. Синтез хлорэтилфосфоновой кислоты, механизм дефолиантного действия. 169
46. Гербицидная активность фосфонометилглицина (глифосата). Способы его получения. Экологические последствия использования глифосата. 171
47. Синтез и свойства тиольных соединений ароматического ряда. 175
48. Три возможных направления использования кремнийорганических соединений в химии биологически активных соединений, привести примеры. 179
49. Получение арсоновых и арсиновых кислот по реакциям Барта и Мейера. 188
50. Зависимость токсичности от строения для фосфорорганических соединений, эмпирическая формула Шрадера. 190
51. Фосфорорганические соединения с противовирусной активностью. Получение фосфонуксусной кислоты и тринатриевой соли фосфонкарбоновой кислоты. Механизм противовирусной активности. 195
52.Взаимодействие трихлорида мышьяка с ароматическими соединениями и с ацетиленом, токсичность α-, β- и γ-льюизита, дифенилхлорарсин и фенарсазинхлорид. 199
53. Зависимость токсичности от строения в ряду нитрофениловых эфиров фосфорной и тиофосфорной кислоты. Получение О-метил-О-этилового эфира хлорангидрида тиофосфорной кислоты. 201
54. Способы получения и свойства тиофосфорных и тиофосфористых кислот. Правило ЖМКО в реакции их солей с органическими галогенидами 205
58.Биологическая активность синтетических селенорганических соединений. Получение и антиоксидантная активность эбселена. 220
59.Получение и химические свойства диметилсульфоксида в качестве растворителя и реагента 225
60.Роль серосодержащих аминокислот в составе белков и в метаболизме. Биосинтез цистеина. 228
1. Стабильность Si-c-связей, влияние заместителей в связанном с атомом кремния остатке.
Наименьшие различия в химических свойствах показывают связи между атомами кремния и углерода в сравнении со свойствами связи между двумя атомами углерода. Стабильность этих связей в реакциях гомолитического разрыва практически одинакова, как и следовало ожидать при небольшом различии в энергии этих связей (соответственно 85 и 72 ккал/моль). В то же время гетеролитическое расщепление Si–С-связи протекает легче, чем гетеролитическое расщепление С–С-связи, вследствие более ионного характера Si–С-связи. Расщепление может протекать в результате нуклеофильной атаки по атому кремния или электрофильной атаки по атому углерода или же в результате более или менее согласованных атак двух этих типов. Однако в нормальных условиях связи атомов кремния с атомами углерода сравнительно устойчивы в химических превращениях. Только в особых случаях наблюдается значительное увеличение реакционной способности Si–С-связи. Так, например, легко разрывается Si–С-связь в β-галогензамещённых алкилсиланах R3SiСН2СН2Х, где Х означает атом галогена. Эти соединения гораздо менее устойчивы в условиях термического воздействия, действия оснований и трихлорида алюминия, чем соответствующие α- и γ-галогензамещённые аналоги. Основное направление реакции при этом представлено образованием олефина и галогенсилана, например:
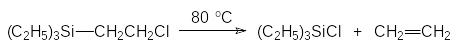
Кремнийорганические соединения с 2‑хлорэтильными группами могут найти применение в качестве регуляторов роста растений, действие которых основано на генерировании этилена, представляющего собой один из растительных гормонов. Так, например, эффективным продуцентом этилена является этасиласил – трис(2-метоксиэтокси)-2-хлорэтилсилан:
![]()
Необычную реакционную способность демонстрируют и другие кремнийорганические соединения с функциональными группами в β‑положении. Далее приводятся некоторые из таких превращений:
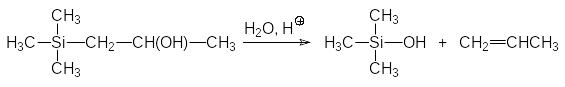
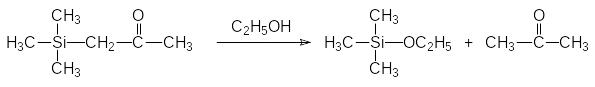
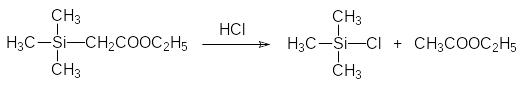
Важно, что Si–С-связь устойчива к действию воды. Только в особых случаях (например, в соединениях с функциональными группами в β‑положении к атому кремния, связанному с арильной группой) появляется возможность гидролиза связи атома кремния с арильной группой в присутствии сильных кислот.
В отличие от
С–С-связи и Si–С-связи, связь между
атомами кремния показывает невысокую
термическую стабильность, что согласуется
с низкой энергией этой связи (54 ккал/моль).
Связь Si-C как и связь С-С, показывает
высокую термическую устойчивость.
2. Реакция Пудовика. Исходные соединения, связь с реакцией Кабачника—Филдса в варианте с основаниями Шиффа.
Реакция присоединения гидрофосфорильных соединений к активированным этиленовым связям, катализируемая сильными основаниями, называется реакцией Пудовика (А.Н.Пудовик, 1954 г.). В качестве непредельных соединений в этой реакции могут участвовать α,β-ненасыщенные кислоты, их эфиры и нитрилы, различные винилкетоны, нитроалкены и другие винильные соединения с электроноакцепторными группами, например:
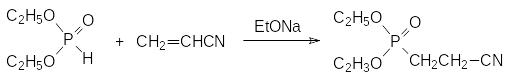
При добавлении этилата натрия к смеси диалкилфосфита и акрилонитрила реакция достаточно быстро останавливается с невысокой степенью превращения реагентов. При добавлении новой порции катализатора она возобновляется и для её завершения добавление катализатора надо повторять несколько раз или непрерывно добавлять его к реакционной массе небольшими порциями. Предполагается, что в основе этого явления лежит алкилирование этилата натрия как исходным фосфитом, так и образующимся фосфонатом. Однако высказывались предположения и о том, что реакция Пудовика представляет собой цепной процесс, в котором этилат натрия является не катализатором, а инициатором.
При взаимодействии диалкилфосфитов с винилкетонами реакция может идти по двум направлениям в соответствии с реакцией Абрамова или реакцией Пудовика:

Реакция Пудовика
Реакция Абрамова

Превращение по реакции Пудовика конкурирует с присоединением гидрофосфорильного соединения по карбонильной группе по реакции Абрамова. Понятно, что кетофосфонат, образовавшийся в результате присоединения диалкилфосфита по этиленовой двойной связи винилкетона, может присоединять еще одну молекулу фосфита по карбонильной группе по реакции Абрамова с образованием гидроксизамещенного бисфосфоната.
В случаях, когда этиленовая двойная связь активирована несколькими электроноакцепторными заместителями, реакция присоединения фосфитов может протекать и без катализатора.
Присоединение гидрофосфорильных соединений по этиленовым связям ненасыщенных углеводородов можно проводить в присутствии катализаторов радикальных реакций или при облучении через образование фосфорцентри-рованных радикалов. В соответствии с этим такая реакция присоединения не подчиняется правилу Марковникова:

Выход в этой реакции увеличивается при добавлении таких кислот, как уксусная или щавелевая кислота.
Присоединение диалкилфосфитов к олефинам может протекать при катализе кислотами, если олефин образует стабильный карбокатион:
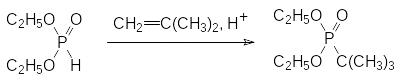
При катализе основаниями идёт присоединение диалкилфосфитов к ацетилену, при этом конечным продуктом реакции может стать этилен-бис-фосфонат:
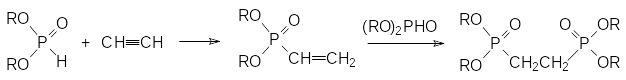
Важный класс фосфорорганических соединений представлен аминофосфонатами и аминофосфоновыми кислотами, один из способов получения которых основан на конденсации гидрофосфорильных соединений с аминами и карбонильными соединениями. Эта трёхкомпонентная реакция, приводящая к образованию α‑аминофосфонатов, была описана в 1952 году М.И.Кабачником и Е.К.Филдсом, проводившими исследования независимо друг от друга. Реакция протекает по схеме:
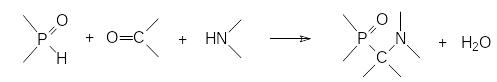
Продуктом реакции становятся соединения, представляющие собой структурные аналоги эфиров α-аминокислот, кроме того, присутствие в их структуре аминной и фосфорильной групп, позволяло рассчитывать на получение на их основе соединений с комплексообразующей способностью. В соответствии с этим были синтезированы соединения с двумя и с несколькими аминофосфонатными группами, которые могли быть использованы, например, в качестве бидентатных лигандов для ионов металлов:
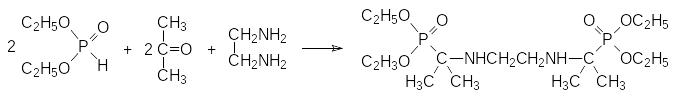
Понятно, что комплексообразующая способность этих соединений по отношению к ионам металлов может быть повышена путём перевода их в соответствующие кислоты гидролитическим отщеплением эфирных групп. В частности, так были получены кислые бис(аминофосфонаты), которые могут быть использованы в качестве антидотов при хронических отравлениях такими токсичными металлами, как бериллий.
Ещё один комплексообразователь - нитрило-трис(метилфосфоновая кислота) - образуется из фосфористой кислоты, формальдегида и хлорида аммония в присутствии соляной кислоты:
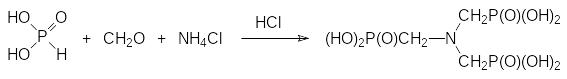
Эта кислота, образующая прочные соли с ионами кальция, магния и других металлов, может найти применение в производстве стиральных порошков в качестве заменителя экологически небезопасных полифосфатов и нитрилотриуксусной кислоты для снижения жесткости воды.
Так, например, были синтезированы фосфонатные аналоги всех белковых аминокислот и пептидные соединения на их основе, блокировавшие такие гидролазы, как ренин. Получаемые по реакции Кабачника-Филдса α‑аминофосфонаты проявляют фунгицидную, гербицидную, рострегуляторную, фармакологическую активность.
Уже в первой публикации по трёхкомпонентному синтезу аминофосфонатов Е.К.Филдс предположил, что её механизм аналогичен механизму реакции Манниха, в соответствии с которым в реакции карбонильного соединения с вторичным амином образуется α-аминоспирт, который легко генерирует карбокатион, атакующий атом фосфора:
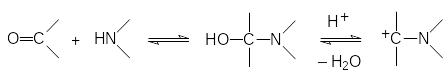
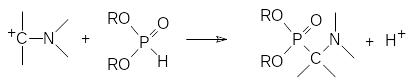
В соответствии с этим механизмом аминоалкилирование фосфитов может также протекать при действии аминоацеталей карбонильных соединений и геминальных диаминов:
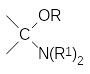 и
и
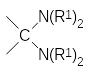
Реакция диалкилфосфитов с этими соединениями протекает с выделением, соответственно, спирта или амина. В этой же статье было показано, что первичные амины и карбонильные соединения могут реагировать с фосфитами через образующиеся в качестве промежуточных продуктов имины. В частности, именно этот механизм считается наиболее вероятным для реакции диалкилфосфитов с бензальдегидом и анилином:
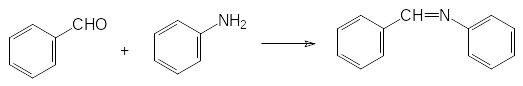
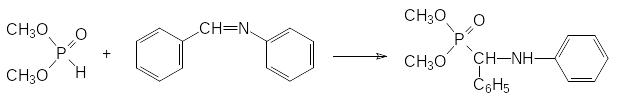
Основные тезисы:
Реакция Пудовика – присоединение диалкилфосфитов по активированной двойной связи (по ацетилену в случае катализа оснваниями), катализируемая сильными основаниями, а также катализаторами радикальных реакций и при облучении. Кроме того, имеет место катализ сильными кислотами в случае образования олефином устойчивого карбокатиона.
Реакция карбонильного соединения со вторичным амином протекает аналогично реакции Манниха – через образование устойчивого карбокатиона. Соответственно, в реакцию могут вступать ацетали и геминальные диамины.
Реакция карбонильного соединения с первичными амином протекает через образование промежуточного имина – основание Шиффа.
