
- •Часть 1
- •Введение
- •Методические указания
- •Контрольная работа по физике №1
- •Студента группы рк-001
- •Шифр 257320
- •Иванова Петра Ивановича
- •1. Механика
- •Кинематика материальной точки и поступательного движения абсолютно твёрдого тела
- •1.2. Динамика материальной точки и поступательного движения абсолютно твердого тела
- •1.3.Кинематика вращательного движения абсолютно твёрдого тела
- •1.4. Динамика вращательного движения
- •1.4.1. Момент инерции и момент импульса
- •1.4.2. Момент силы. Основной закон динамики вращательного движения
- •1.5.Механическая энергия, работа и мощность
- •1.5.1 Механическая работа при поступательном движении
- •1.5.2. Кинетическая и потенциальная энергия
- •1.5.3. Работа и мощность при вращательном движении
- •1.6. Законы сохранения
- •1.6.1. Закон сохранения импульса
- •1.6.2. Закон сохранения момента импульса
- •1.6.3. Закон сохранения механической энергии
- •1.7. Механика жидкостей и газов
- •1.7.1. Идеальная жидкость. Уравнение неразрывности. Уравнение Бернулли
- •1.7.2. Вязкость. Ламинарный и турбулентный режимы течения жидкостей
- •1.8. Механика деформируемых тел
- •1.8.1. Идеально упругое тело. Упругие напряжения
- •1.8.2 Одноосное растяжение и сжатие
- •1.8.3. Сдвиг
- •1.8.4. Кручение
- •1.9. Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Задача № 6
- •Решение.
- •Решение
- •Решение
- •Решение
- •1.10. Задачи для контрольных заданий
- •2. Основы молекулярно - кинетической теории
- •2.1. Идеальный газ. Уравнение состояния. Основное уравнение молекулярно - кинетической теории
- •2.2. Распределение молекул по скоростям
- •2.3. Идеальный газ в поле сил тяжести. Распределение Больцмана
- •2.4. Эффективный диаметр и средняя длина свободного пробега молекул
- •2.5. Внутренняя энергия идеального газа. Теплота и работа. Первое начало термодинамики
- •2.6. Изопроцессы. Применение первого начала термодинамики к различным процессам. Адиабатный процесс
- •2.7. Круговые процессы. Цикл Карно. Второе начало
- •2.8. Энтропия
- •2.9. Примеры решения задач
- •Решение
- •Решение.
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Р ешение
- •Решение
- •2.10 Задачи для контрольных заданий
- •2.16. Азот находится при нормальных условиях. Найти:
- •3. Электростатика
- •3.1. Электрический заряд. Закон сохранения электрического заряда. Закон Кулона
- •Электростатическое поле. Напряженность электростатического поля. Принцип суперпозиции полей
- •3.3. Линии напряжённости. Поток вектора напряжённости. Теорема Гаусса
- •3.4. Работа сил электрического поля. Потенциал
- •3.5. Эквипотенциальные поверхности. Связь между напряженностью и потенциалом
- •3.6. Проводники в электрическом поле
- •3.7. Диэлектрики в электрическом поле
- •3.8. Электроемкость уединенного проводника.
- •3.9. Энергия электрического поля
- •3.10. Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •3.11. Задачи для контрольных заданий
- •4. Законы постоянного тока
- •4.1. Сила и плотность тока. Сторонние силы, эдс и напряжение
- •4.2 Обобщённый закон Ома. Дифференциальная форма закона Ома
- •4.3. Работа тока. Закон Джоуля - Ленца
- •4.4. Правила Кирхгофа и их применение к расчёту электрических цепей
- •4.5. Примеры решения задач.
- •Решение
- •Подставляя это выражение в (1), получим
- •Решение Из условия равномерности возрастания тока следует
- •Решение
- •4.6. Задачи для контрольных заданий
- •5. Варианты контрольных заданий
- •П. 1. Скалярное произведение двух векторов
- •П. 1. Векторное произведение двух векторов
- •Приложение 2
- •П. 2. Таблица простейших производных.
- •Приложение 3 Элементы интегрального исчисления Интегрирование– действие обратное дифференцированию
- •Неопределенный интеграл
- •Приложение 4
- •Приложение 5 Некоторые астрономические величины
- •Приложение 6 Основные физические постоянные
- •Приложение 7 Плотности ρ твёрдых тел, жидкостей и газов
- •Приложение 8 Диэлектрическая проницаемость ε
- •Удельное сопротивление ρ и температурный коэффициент α проводимости
- •Заключение
- •Библиографический список
- •Оглавление Введение…………………………………………………………..3
- •Кинематика материальной точки и поступательного движения абсолютно твёрдого тела……………….….5
- •1.2. Динамика материальной точки и поступательного
- •2.5. Внутренняя энергия идеального газа. Теплота и работа.
- •Часть 1 механика, молекулярная физика, термодинамика и электродинамика
- •394026 Воронеж, Московский просп.,14
- •Часть 1
2.6. Изопроцессы. Применение первого начала термодинамики к различным процессам. Адиабатный процесс
Изохорный процесс (V = const; dV = 0). Так как dV = 0, то работа при изохорном процессе А = О. Из первого закона термодинамики следует, что
![]() ,
(2.26)
,
(2.26)
то есть
при изохорном процессе поступающая
извне теплота
![]() идёт только на приращение внутренней
энергии dU
системы.
Учитывая, что
идёт только на приращение внутренней
энергии dU
системы.
Учитывая, что
![]() ,
получаем
,
получаем
![]() , (2.27)
, (2.27)
CV – молярная теплоёмкость при постоянном объеме.
Сопоставляя (2.23) и (2.27), найдем СV
![]()
![]()
. (2.28)
Изобарный процесс (P = const, dP = 0). Передаваемое газу количество теплоты идёт на изменение его внутренней энергии и на совершение им работы при постоянном давлении:
Q = dU + A . (2.29)
Пользуясь уравнением состояния, получим
A = pdV = vRdT
Тогда,
учитывая соотношение (2.27) и что
![]() ,
перепишем
уравнение (2.29)
в виде:
,
перепишем
уравнение (2.29)
в виде:
vCp dT = vСv dT + vRdT,
откуда
![]() ,
(2.30)
,
(2.30)
Это выражение называют уравнением Майера.
Из
уравнения (2.30) следует, что Cp>Cv
![]() .
.
При одном и том же Q, изменение температуры dT при изобарном процессе меньше, чем при изохорном, и, следовательно, теплоемкость больше.
Изотермический процесс (T = const, dT = 0).
Так как dT
= 0, то
внутренняя энергия системы при
изотермическом
процессе не изменяется, и вся поступающая
извне теплота идёт на совершение системой
работы:
![]() .
(2.31)
.
(2.31)
Учитывая, что согласно уравнению состояния идеального газа,
![]()
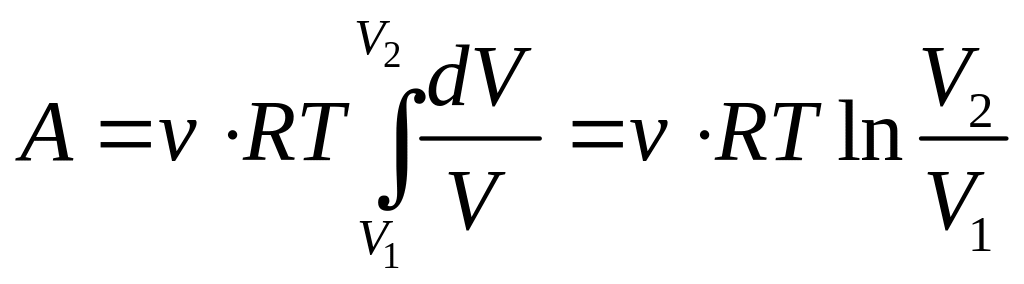 получим
получим
. (2.32)
Адиабатный процесс - процесс без теплообмена с окружающей средой ( Q = 0). При Q = 0 из (2.29) следует A = - dU, то есть
PdV = -νCvdT. (2.33)
Это означает, что система совершает работу за счёт убыли своей внутренней энергии. При А > 0 (газ расширяется) dT < 0 (он охлаждается). При А < 0 (газ сжимается) dT > 0 (он нагревается).
Зависимость какого-либо параметра адиабатного процесса от другого называется уравнением адиабаты. В выражение (2.33) входят все три параметра состояния, причём два из них в дифференциальной форме. Чтобы получить уравнение адиабаты, нужно один параметр, например P, исключить, используя уравнение состояния идеального газа. В результате получим:
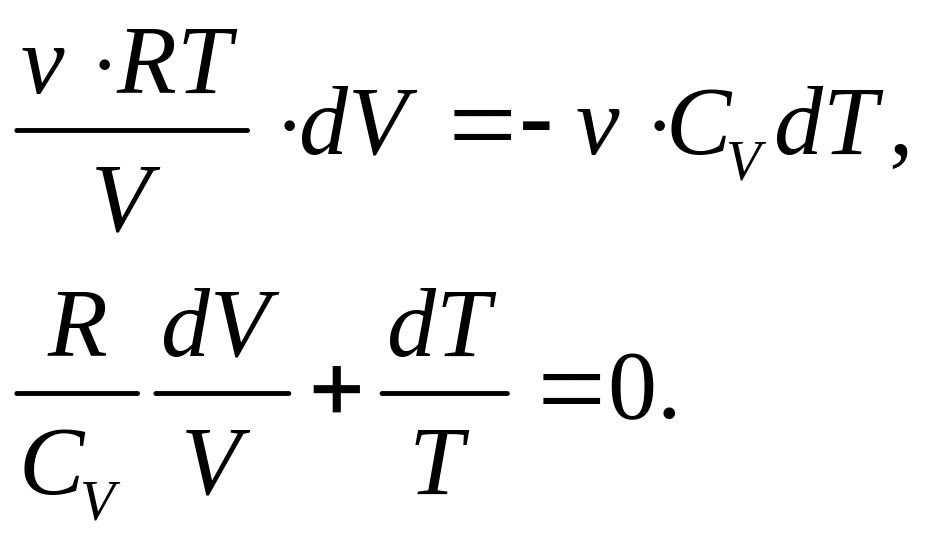
Или на основании (2.30)
![]()
где
![]() - отношение теплоём- костей при постоянном
давлении и объеме.
- отношение теплоём- костей при постоянном
давлении и объеме.
Так как γ = сonst, то
![]() .
(2.34)
.
(2.34)
Пользуясь уравнением состояния идеального газа, это выражение можно представить в других переменных:
![]() .
(2.35)
.
(2.35)
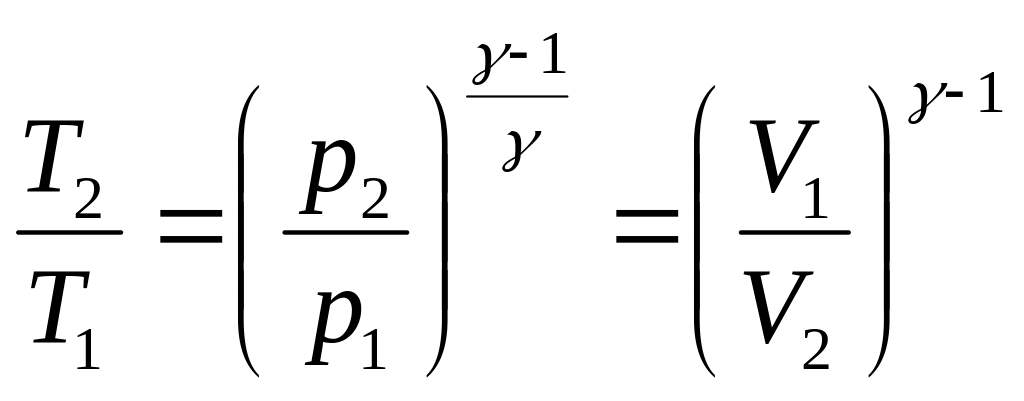 Из
уравнений (2.34)
и (2.35)
следуют
полезные соотношения между параметрами
двух разных точек адиабаты:
Из
уравнений (2.34)
и (2.35)
следуют
полезные соотношения между параметрами
двух разных точек адиабаты:
Уравнения (2.34) (2.35)
- это
различные формы уравнения адиабаты,
в которых
![]() называют показателем адиабаты. Так
как γ>1,
то на диаграмме РV
(риc.2.7)
адиабата 1 круче,
чем изотерма
2.
Выражение
для работы при адиабатном
процессе
следует из
уравнения (2.33):
называют показателем адиабаты. Так
как γ>1,
то на диаграмме РV
(риc.2.7)
адиабата 1 круче,
чем изотерма
2.
Выражение
для работы при адиабатном
процессе
следует из
уравнения (2.33):
![]() . (2.36)
. (2.36)
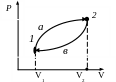
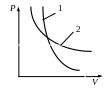
Рис.2.7 Рис.2.8
