
- •Терминологический словарь
- •Моносахариды- простые углеводы, содержащие гидроксильные и альдегидную (альдозы) или кетонную (кетозы) группы. По числу атомов углерода различают триозы, тетрозы, пентозы и т.Д.
- •Глава 1. Паращитовидные железы
- •Функции кальция.
- •Регуляция поддержания нормального уровня
- •Кальция, магния и фосфата в сыворотке крови
- •Метаболизм фосфата
- •Регуляторы экспрессии птг
- •Рецепторы птг — трансмембранные гликопротеины, связанные с g‑белком — в значительном количестве содержатся в костной ткани (остеобласты) и корковой части почек (эпителий извитых канальцев нефрона).
- •Функции. Птг поддерживает гомеостаз кальция и фосфатов.
- •Минерализация остеоида
- •Особенности коррекция обмена кальция методами прикладной кинезиологии.
- •Пищевые факторы стимулирующие: Лосось
- •Глава 2. Мужские половые железы — яички (тестис)
- •Анатомия яичек и половой системы
- •Эмбриогенез
- •Гормоны мужских половых желез - яичек
- •Эффекты мужских половых гормонов
- •Транспорт мужских половых гормонов
- •Механизм действия андрогенов
- •Регуляция функции мужских половых желез
- •Болезни мужских половых желез гипогонадизм
- •Первичный гипергонадотропный гипогонадизм
- •Причины первичного гипогонадизма:
- •Недостаточность семинифорных трубочек у взрослых.
- •Аутоиммунный гипогонадизм.
- •Вторичный и третичный гипогонадотропный гипогонадизм
- •Третичный гипогонадизм
- •Гиперпролактинемия как причина гипогонадизма
- •Мужской климакс, или андропауза
- •Примеры токсических эффектов факторов внешней среды на мужскую репродуктивную систему
- •Доброкачественная гиперплазия простаты (дгп)
- •Гормональная регуляция предстательной железы
- •Фитотерапия
- •Женские половые железы — яичники. Анатомия, функция, гормоны яичников. Менструальный цикл
- •Гормоны яичников
- •Физиологические эффекты стероидных гормонов яичников
- •Метаболизм стероидных гормонов яичников
- •Пути метаболизма эстрогенов
- •Рост и развитие фолликула в яичниках
- •Гипоталамически-гипофизарный цикл
- •Цикл яичников
- •Половой гормон, связывающий глобулин
- •Механизм регуляции функции яичников
- •Клиника и патогенез нарушений метаболизма эстрогенов
- •Предменструальный синдром
- •При ановуляторных циклах предменструальный синдром не возникает.
- •Наблюдаются:
- •Диагностический критерий:
- •Лечение дисменореи
- •Симптомы
- •Эстрогены при поликистозе:
- •Диагностика
- •Возможные этиологии
- •Лечение
- •Предменопауза
- •Менопауза
- •Урогенитальные изменения
- •Лечение
- •Прутняк/Ягоды чистоты
- •Клопогон кистевидный (Black Cohosh)
- •Индол-3-карбинол
- •Глава 3. Эндокринная часть поджелудочной железы (островки лангерганса, гормоны, их функция, эффекты, механизм действия)
- •Механизм действия инсулина
- •Транспортные белки для глюкозы
- •Соматостатин
- •Панкреатический полипептид (рр)
- •Гомеостаз глюкозы в норме Функции углеводов
- •Расщепление углеводов
- •Транспорт глюкозы в клетки
- •Катаболизм глюкозы
- •Значение анаэробного гликолиза
- •Особенности метаболизма гликогена в печени и мышцах
- •Биосинтез глюкозы - глюконеогенез
- •Пентозофосфатный путь в метаболизме глюкозы
- •Регуляция метаболизма углеводов (некоторые аспекты)
- •Сахарный диабет
- •3. Другие специфические типы сахарного диабета.
- •4. Гестационный диабет.
- •Сахарный диабет тип 2
- •Гиперинсулинизм.
- •Интерпретация результатов пробы
- •Аллопатическое лечение сахарного диабета
- •3. Препараты сулъфонилмочевины (см).
- •1 Тип сахарного диабета.
- •2Тип сахарного диабета.
- •Глубокоуважаемые коллеги!
- •Программа семинаров
Регуляторы экспрессии птг
[Са2+] сыворотки — главный регулятор секреции ПТГ. Ионы Са2+ взаимодействуют с рецепторами Са2+ (Са2+-сенсор) главных клеток паращитовидных желёз.
Гипокальциемия ([Са2+] в крови) усиливает секрецию ПТГ.
Гиперкальциемия ([Са2+] в крови) уменьшает секрецию ПТГ.
Са2+-сенсор — трансмембранный гликопротеин, обнаруженный в главных клетках околощитовидных желёз, а также в эпителии почечных канальцев. Связывание Са2+ с рецептором стимулирует фосфолипазу C, что приводит к освобождению инозитолтрифосфата и диацилглицерола с последующим выбросом Са2+ из его внутриклеточных депо. Увеличение внутриклеточного [Са2+] активирует протеинкиназу C. Конечный результат — подавление секреции ПТГ.
Витамин D — вспомогательный регулятор экспрессии гена ПТГ. Рецепторы витамина D (кальцитриола) относятся к ядерным факторам транскрипции. Связывание комплекса «кальцитриол–рецептор кальцитриола» с ДНК угнетает транскрипцию гена ПТГ.
Ионы магния. Пониженное содержание Mg2+ стимулирует секрецию ПТГ, избыток Mg2+ оказывает на неё тормозящий эффект.
Секреция ПТГ увеличивается под влиянием активации β–адренергических рецепторов и цАМФ.
Рецепторы птг — трансмембранные гликопротеины, связанные с g‑белком — в значительном количестве содержатся в костной ткани (остеобласты) и корковой части почек (эпителий извитых канальцев нефрона).
Известно 2 типа рецепторов ПТГ: тип I связывает ПТГ и относящийся к ПТГ белок, тип II — только ПТГ. При связывании лигандов с рецептором в клетках–мишенях происходит не только увеличение внутриклеточного содержания цАМФ, но и активация фосфолипазы C (освобождение инозитолтрифосфата и диацилглицерола, выброс Са2+ из его внутриклеточных депо, активация Са2+–зависимых протеинкиназ).
Мутации генов ПТГ–рецепторов, а также мутации генов отдельных субъединиц G‑белка приводят к развитию разных форм остеодистрофий.
Функции. Птг поддерживает гомеостаз кальция и фосфатов.
ПТГ увеличивает содержание кальция в крови, усиливая резорбцию кости и вымывание кальция из костей, а также усиливая канальцевую реабсорбцию кальция в почках.

Рис. 9. Механизмы действия паратгормона. Адаптировано из Rose BD (1994).
ПТГ стимулирует образование кальцитриола в почках, кальцитриол же усиливает всасывание кальция и фосфатов в кишечнике.
ПТГ уменьшает реабсорбцию фосфатов в канальцах почки и усиливает их вымывание из костей.
Вторичная гиперфункция паращитовидных желез может возникать при хронических заболеваниях почек и рахите, для которых характерен хронически низкий уровень Ca2+ в плазме. Это обстоятельство по типу обратной связи вызывает стимуляцию паращитовидных желез и приводит к их компенсаторной гипертрофии.
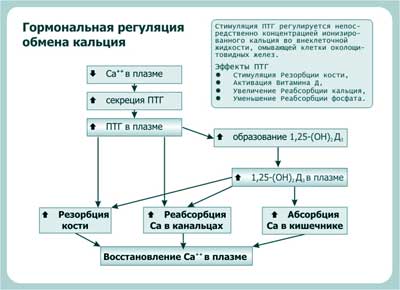
Рис. 10. Гормональная регуляция обмена кальция (для упрощения здесь не показано влияние ПТГ и витамина Д на фосфат - см. рисунок 6). Адаптировано из Вандер А., 2000.
2 основных механизма действия паратгормона: активация системы аденилатциклаза - циклический АМФ (аденозинмонофосфат) - протеинкиназа А и системы фосфатидилинозитол - протеинкиназа С
ПТГ-СВЯЗЫВАЮЩИЙ ПРОТЕИН
ПТГ-связывающий протеин (ПТГсП) —полипептид, состоящий из 141 аминокислотного остатка — имеет частичную структурную гомологию с ПТГ. Рецепторы этого гормона — рецепторы ПТГ типа I. Оказывает те же физиологические эффекты, что и ПТГ. Может синтезироваться в злокачественных опухолях и вызывает значительную гиперкальциемию, так как его действие и эффекты подобны ПТГ. В норме ПТГсП синтезируется в нормальных тканях, не вызывая гиперкальциемию, и его эффекты совершенно отличаются от ПТГ. В пренатальной жизни он необходим для пролиферации и минерализации хондроцитов и как регулятор транспорта кальция через плаценту. В постнатальной жизни ПТГсП регулирует эпителиально-мезенхимальные связи, которые имеют основное значение в развитии молочных желез, зубов, эпидермиса и волосяных фолликулов. Считают, что ПТГсП оказывает свои эффекты локально, не поступая в кровоток. Концентрация ПТГсП в сыворотке крови < 1,3 ммоль/л
ВИТАМИН D3
Активный витамин D3 — l,25(OH)2D образуется в почках из его предшественника эргокальциферола, который поступает с пищей, или из предшественников, которые образуются в коже из холестерина под воздействием ультрафиолетовых лучей (рис.9).
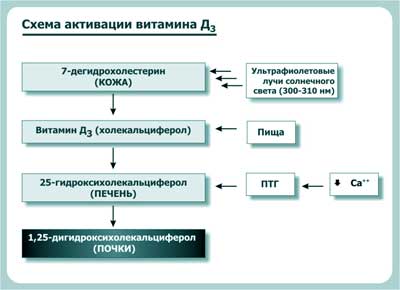
Рис.11. Схема активации витамина Д. Адаптировано из Lancaster L.E., 1995 [2].
В сыворотке крови витамин D3 (l,25(OH)2D) связан с белком - витамин D связывающим протеином. Свободный биологически активный витамин D3 циркулирует в крови в очень малых количествах и составляет 0,03—0,4% от общего количества.
Механизм действия витамина Ds подобен всем стероидным гормонам. Он свободно проходит в цитоплазму клетки, где встречается со своим рецептором и вместе с ним поступает в ядро. В ядре витамин D3 активирует гены, кодирующие его эффекты, и тРНК переносит информацию в рибосомы цитоплазмы клеток, завиимых от витамина D3 тканей и органов.

Рисунок 12. Механизм действия витамина Д. Адаптировано из Brown A.J., 1999 .
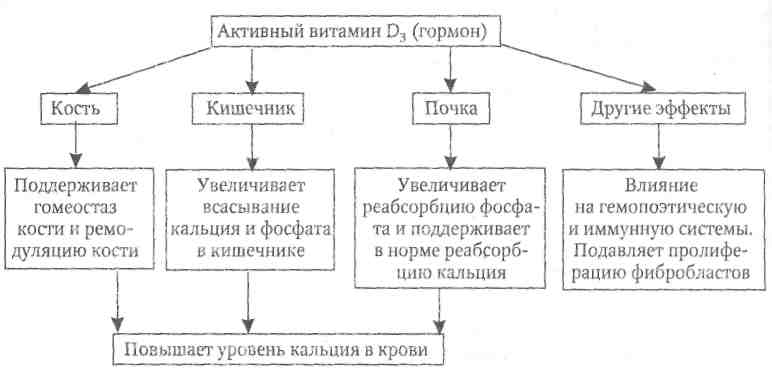
Рис. 13. Эффекты витамина D3
Кроме классического действия на кость, почки, кишечник, витамин D3 имеет много других эффектов. Он оказывает влияние на гемопоэтическую и иммунную системы. Витамин D3 регулирует синтез и секрецию инсулина В-клетками островков поджелудочной железы, пролактина лактотрофами гипофиза и ПТГ клетками паращитовидных желез. Он регулирует синтез цитокинов и секрецию интерлейкина-2 из лимфоцитов и фактора некроза опухолей из моноцитов. Витамин D, уменьшает пролиферацию фибробластов, лимфоцитов, тимоцитов. Кроме того, витамин D3 оказывает подавляющее действие на атипичные клетки в молочных железах, в кишечнике и на клетки миелоидного ряда. Поэтому витамин D3 используют в лечении псориаза, аллопеции и идут исследования возможности лечения им рака различных локализаций.
В норме концентрация витамина D3 — l,25(OH)2D в сыворотке крови у взрослых 15—60 нг/дл (31—144 пмоль/л).
КАЛЬЦИТОНИН
Кальцитонин образуется в парафолликулярных клетках (С-клетки) щитовидной железы. Кальцитонин — полипептидный гормон, состоящий из 32 аминокислот в виде одной цепи.
Основная функция кальцитонина состоит в торможении резорбции кости через остеокласты. На остеокластах имеются рецепторы к кальцитонину, занимая их, кальцитонин, в течение минут, приводит к уменьшению размеров остеокластов, втягиванию в них органелл и уменьшению костной резорбции. В конечном итоге, под влиянием кальцитонина приостанавливается резорбция кости и увеличивается поступление кальция в кость.
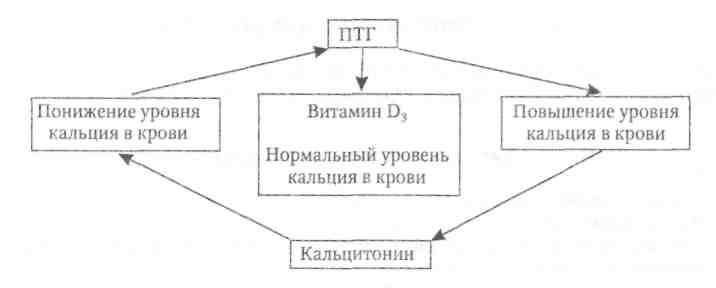
Рис. 14. Регуляция уровня кальция в крови
Таблица 4 Нормальные концентрации гормонов, регулирующих уровень кальция и фосфата в сыворотке крови
Гормон |
Концентрация |
|
Паратиреоидный гормон |
10—60 пг/мл (1—6 пмоль/л) |
|
Кальцитонин: |
|
|
мужчины |
3-24 пг/л (0,88-7,6 пмоль/л) |
|
женщины |
2-17 пг/л (0,58-5,0 пмоль/л) |
|
Витамин D3 - l,25(OH)D |
20—60 пг/мл (5—150 пмоль/л) |
|
Витамин D, - 1,25(ОН)2 D |
10-50 пг/мл (25-125 пмоль/л) |
|
Стимулом для синтеза и секреции кальцитонина является повышение уровня кальция в сыворотке крови. Тормозит его секрецию снижение уровня кальция в крови.
На мембранах парафолликулярных клеток в щитовидной железе имеются рецепторы к кальцию и связанный с ним белок 120 кДа. Этот белок является «цензором», чутко улавливающим повышение уровня кальция в сыворотке крови, и в ответ стимулирует секрецию кальцитонина. Кальцитонин оказывает действие и на почки. Клетки проксимального канальца имеют рецепторы к кальцитонину. Последний умеренно тормозит реабсорбцию фосфата и кальция и увеличивает натрийурез. Болезни, вызванные избытком кальцитонина, не известны. Медуллярный рак щитовидной железы в избытке секретирует кальцитонин. Повышение его в крови является одним из маркеров медуллярного рака щитовидной железы.
ГИПЕРКАЛЬЦИЕМИЯ
Гиперкалъциемия - превышение уровня кальция в сыворотке крови выше нормальных колебаний 2,1—2,6 ммоль/л (8,5—10,5 мг/дл).
ПРИЧИНЫ
1. Первичный гиперпаратиреоз:
а) спорадический;
б) гиперпаратиреоз, как одно из проявлений МЭН 1 и МЭН 2а (синдром мно- жественной эндокринной неоплазмы).
2. Злокачественные опухоли:
а) злокачественные опухоли, которые синтезируют паратиреоидный гормон связывающий протеин (ПТГсП);
б) гиперкальциемия, вызванная остеолизисом: множественная миелома, лей- кемия, лимфома (некоторые лимфомы секретируют ПТГсП);
в) гиперкальциемия, как следствие секреции опухолью ПТГ, — эктопическая секреция паратиреоидного гормона (встречается очень редко).
3. Гранулематозные заболевания:
Саркоидоз. В макрофагах саркоидозных гранулем имеется энзим 25-гидрокси-витамин D 1-ос-гидроксилаза, который превращает неактивный предшественник витамин D3 — l,25(OH)D в активный витамин D3 — l,25(OH)2D. Избыток витамина l,25(OH)2D стимулирует остеокласты, резорбцию кости и выход кальция из кости в кровоток. ПТГ подавлен избытком кальция.
4. Эндокринопатии:
а) Тиреотоксикоз. Тиреоидные гормоны, особенно при их избытке, оказывают прямое резорбтивное действие на кость.
б) Феохромоцитома. Может синтезировать паратиреоидный гормон связы- вающий протеин (ПТГсП).
в) Острая недостаточность коры надпочечников.
5. Вызванная лекарствами:
а) Литий. Литий стимулирует секрецию ПТГ и увеличивает реабсорбцию каль- ция в почках.
б) Тиазидовые диуретики.
в) Гипервитаминоз D. В сыворотке высокая концентрация витамина D, низкий уровень ПТГ.
г) Гипервитаминоз А. Характерны гиперкальциемия, остеопороз, переломы костей, гингивиты, кожная эритема, выпадение волос.
6.Абсорбтивная гиперкальциемия (молочно-щелочной синдром) может развиться при употреблении больших количеств молока, антацидов, содержащих кальций.
Другие причины:
а) Иммобилизация. При длительной иммобилизации увеличивается реабсорб- ция кости.
б) Острая почечная недостаточность при синдроме раздавливания. В процессе рабдомиолиза освобождается кальций.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ГИПЕРКАЛЬЦИЕМИИ
. При легкой гиперкальциемии обычно симптомы отсутствуют. При умеренной и особенно выраженной гиперкальциемии беспокоят слабость, сонливость, депрессия, атаксия, в тяжелых случаях сопор и кома. Снижен аппетит, вплоть до анорексии, тошнота, рвота. Мышечная слабость, брадикардия вплоть до возникновения асистолии. Характерно образование камней в почках, почечная колика, может развиться нефрокальциноз и ХПН. Характерна полиурия и полидипсия, как следствие нефрогенного несахарного диабета, так как гиперкальциемии снижает чувствительность рецепторов вазопрессина в собирательных трубочках почек к вазопрессину. Укорочен интервал QT на ЭКГ.
БОЛЕЗНИ ПАРАЩИТОВИДНЫХ ЖЕЛЕЗ
ГИПЕРПАРАТИРЕОЗ
Первичный является следствием первичной патологии паращитовидных желез (ПЩЖ) (аденома, гиперплазия). Для него характерны избыточная продукция ПТГ и гиперкальциемия.
Вторичный является ответом паращитовидных желез на гипокальциемию, возникающую при недостатке витамина D (рахит), хронической почечной недостаточности (уменьшается реабсорбция кальция в почках). В ответ на гипокальциемию увеличиваются секреция ПТГ и резорбция кости. В результате уровень кальция в сыворотке нормализуется. Это ведет к уменьшению минеральной плотности кости, остеомаляции и почечной остеодистрофии. Длительная стимуляция паращитовидных желез может привести к развитию аденомы паращитовидных желез или их гиперплазии.
ПЕРВИЧНЫЙ ГИПЕРПАРАТИРЕОЗ
У женщин встречается в 2—3 раза чаще, чему мужчин.
Этиология. Причины: 80% случаев - автономно функционирующая аденома одной из паращитовидных желез. 15% случаев - гиперплазия всех четырех паращитовидных желез. в 5% случаев - множественная эндокринная неоплазма (МЭН 1, МЭН 2а).
Патогенез. Избыток ПТГ увеличивает резорбцию кости, мобилизацию кальция из кости, увеличивает реаосорбцию кальция в почках, и в результате развивается гиперкальциемия. Под влиянием избытка ПТГ в почках уменьшается реабсорбция фосфата и уровень его в сыворотке крови снижается. Гиперкальциемия снижает чувствительность рецепторов собирательных трубочек почек к вазопрессину с развитием полиурии и полидипсии (почечный несахарный диабет).
Основные нарушения, вызванные избытком ПТГ и гиперкальциемией.
Клинические проявления. В классических случаях гиперпаратиреоз проявляется: генерализованным поражением костей; фиброкистозным остеитом; поражением почек: нефролитиаз, нефрокальциноз, хроническая почечная недостаточность (ХГШ); гиперкальциемия и ее последействия (нарушение психического статуса); нарушения со стороны пищеварительной и нейромышечной систем.
85% больных гиперпаратиреозом не имеют классических проявлений, заболевание протекает асимптоматично, без поражения костей с умеренной гиперкальциемией и выявляется случайно.
Рис.15. Клинические проявления первичного гиперпаратиреоза
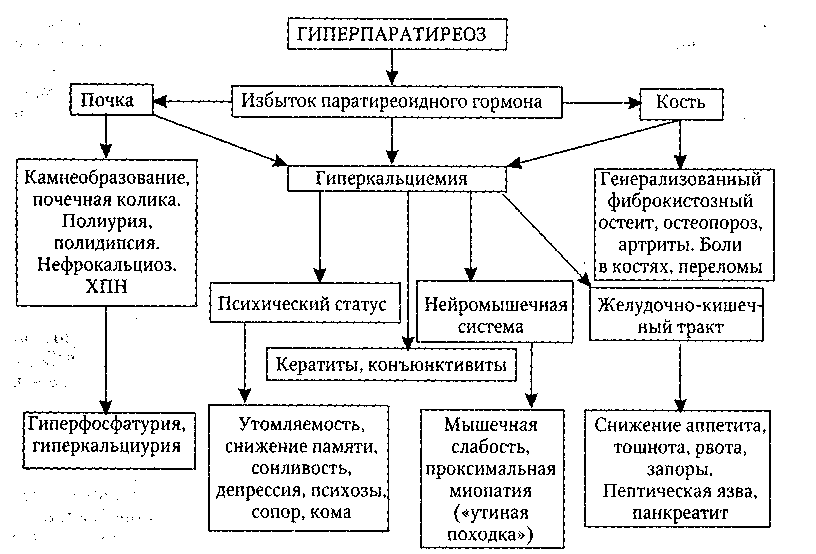
У 5% больных развиваются тяжелые поражения суставов в результате кальциноза суставных хрящей.
Асимптоматическое течение гиперпаратиреоза. Гиперпаратиреоз нередко выявляется случайно, по наличию гиперкальциемии. В этих случаях необходимо исключить гиперкальциемию другого происхождения, в частности при злокачественных опухолях, которые вырабатывают ПТГсП, гранулематозные заболевания (саркоидоз), передозировку витамина D или витамина А, лечение литием.
Лечение первичного гиперпаратиреоза. Хирургическое удаление паращи-товидной железы, в которой находится аденома. При наличии гиперплазии паращитовидных желез удаляются три железы и половина четвертой. Однако, особенно при МЭН, оставшаяся половина одной железы гиперплазируется и гиперпаратиреоз персистирует.
Медикаментозное (консервативное) лечение гиперпаратиреоза. Пост-менопаузальным женщинам проводится заместительная терапия эстрогенами — 1,25 мг конъюгированных эстрогенов или 30 мкг этинилэстрадиола в день будут снижать уровень кальция в сыворотке крови в среднем на 0,5—1,0 мг/дл и увеличивать минеральную плотность кости. Концентрация ПТГ не снижается.
Кальцитонин — синтетический кальцитонин лосося. Назначается подкожно по 50—100 ЕД ежедневно или через день в течение 1—4 недель.
Пища, богатая фосфатом, и фосфосодержащие антациды уменьшают всасывание кальция.
СЕМЕЙНАЯ ГИПОКАЛЬЦИУРИЧЕСКАЯ ГИПЕРКАЛЬЦИЕМИЯ
Этот вид гиперкальциемии является следствием уменьшения экскреции кальция с мочой, менее чем 50 мг/сут. В основе лежит нарушение внутрипочечного механизма, участвующего в экскреции кальция. Предполагают, что имеет место дефект в рецепторах ПТГ в почках. Заболевание наследуется по аутосомно-доминантному типу. Гиперкальциемия обычно умеренно выражена, общий кальций — 2,7—3,0 ммоль/л (10,5—12,0 мг/дл), и часто сочетается с гиперфосфатемией. ПТГ в сыворотке крови нормальный или умеренно повышен.
Заболевание протекает доброкачественно, асимптоматично.
ГИПОКАЛЬЦИЕМИЯ
Гипокальциемия — это снижение уровня общего кальция в сыворотке крови < 2 ммоль/л (< 8 мг/дл).
Причины гипокальциемии
1. Гипопаратиреоз:
а) хирургический;
б) идиопатический (аутоиммунный);
в) пострадиационный;
г) инфильтративный (отложение железа, меди);
д) функциональный (при гипомагнеземии);
е) семейный;
ж) неонатальный (гипоплазия паращитовидных желез).
Резистентность к действию паращитовидного гормона — псевдогипопаратиреоз.
Препараты, блокирующие остеокласты и резорбцию кости (пликомицин, кальцитонин, бифосфонаты).
Недостаток синтеза витамина D3 — l,25(OH)2D в почках из-за врожденной недостаточности витамина D3 или недостаточности энзима — почечной 25-ОН-угШ-1-ос-гидроксилазы, превращающей l,25(OH)D в активный витамин D3 (гормон) — l,25(OH)2D (рахит тип 1 или тип 2).
Острый панкреатит.
Переливание цитратной крови.
Остеобластные метастазы.
Гипомагнеземия. Подавляет секрецию ПТГ (при уровне магнезии < 0,4 ммоль/л (< 1 мг/дл) следует немедленно вводить магнезию).
ГИПОПАРАТИРЕОЗ
Гипопаратиреоз — клинико-биохимический синдром недостатка паратиреоидного гормона (ПТГ), характеризующийся гипокальциемией и ее клиническими проявлениями.
Причины:
Постхирургический.
Радиационный гипопаратиреоз.
Идиопатический или аутоиммунный гипопаратиреоз. Аутоантитела направлены к рецепторам кальция на мембранах клеток паращитовидных желез.
Аутоиммунный гипопаратиреоз может быть изолированным или быть частью синдрома множественной аутоиммунной эндокринопатии, в который входят недостаточность коры надпочечников, сахарный диабет тип I и кожно-слизистый кандидоз.
Семейный, или генетически обусловленный, гипопаратиреоз. В основе болезни мутация генов рецепторов кальция на мембранах клеток паращитовидных желез — снижение чувствительности рецепторов к уровню кальция в крови и недостаток секреции ПТГ.
Функциональный гипопаратиреоз, вызванный недостатком магния. Гипомагниемия тормозит секрецию ПТГ.
Врожденная гипоплазия паращитовидных желез.
Патогенез.
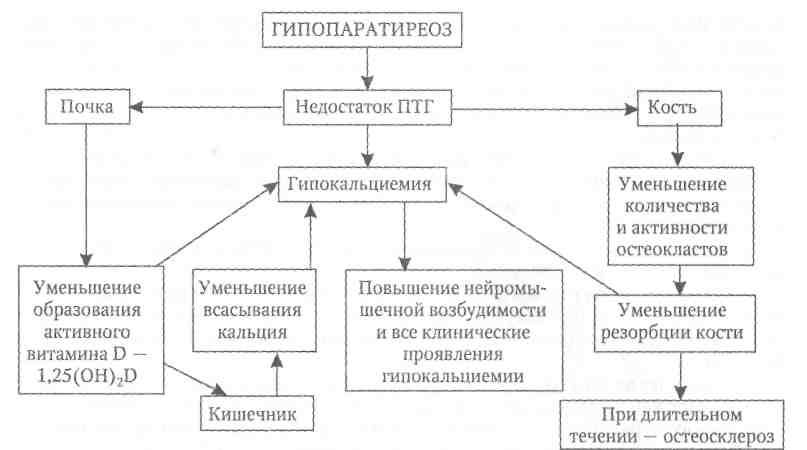
Рис.16. Патогенез гипопаратиреоза
Клинические проявления
Симптомы повышенной нервно-мышечной возбудимости: а) парестезии в основном вокруг рта, в пальцах; б) тетания в виде спазма отдельных групп мышц, чаще всего мимических («рыбий рот») и метакарпальных («рука акушера»); в) судороги. Две формы судорог — простую или генерализованную тетанию, характеризующуюся продолжительным тоническим спазмом мышц, и эпилептиформный судорожный синдром, который подобен эпилепсии, с соответствующими изменениями электроэнцефалограммы (ЭЭГ), нередко отеком соска зрительного нерва, но в отличие от эпилепсии сознание сохранено. Судороги могут быть болезненными.
Повышение активности симпатоадреналовой системы: тахикардия, потливость, бледность кожи.
Проявления со стороны сердца. Замедляется период реполяризации, удлиняется интервал QT на ЭКГ.
Проявления со стороны ЦНС. Отложение кальция в базальных ганглиях проявляется как истинный паркинсонизм. Неврологическая симптоматика и отек зрительного нерва могут симулировать опухоль мозга.
Проявления со стороны кожи и зубов. Кожа сухая, шелушащаяся. Ломкие ногти. У детей нарушается образование зубной эмали, плохой рост зубов, дефекты в корнях зубов.
Проявления со стороны глаз. Характерна лентикуляриая катаракта.
При длительно текущем гипопаратиреозе и недостаточном лечении может развиться синдром мальабсорбции.
ЛАТЕНТНО ПРОТЕКАЮЩАЯ ГИПОКАЛЬЦИЕМИЯ
Латентно протекающая гипокальциемия — уровень кальция в сыворотке крови 7—8 мг/дл.
Диагностические тесты латентно протекающей гипокальциемии:
1. Положительные симптомы Хвостека и Труссо.
Симптом Хвостека: поколачивание по области выхода лицевого нерва — на 1 см кпереди и несколько ниже бугорка ушной раковины. Положительный симптом — от слабого подергивания уголка рта на стороне поколачивания до ярко выраженного сокращения всех лицевых мышц.
Симптом Труссо: в манжетку тонометра, надетую на руку пациента, нагнетается воздух до достижения отметки на 20 мм рт. ст. выше уровня систолического давления. Положительный симптом — появление карпального спазма («рука акушера») (рис. 78).
Экстрапирамидальные симптомы (из-за кальцификации базальных ганглиев).
Сердце — удлинение интервала QT, кардиомегалия. Сердечная недостаточность, резистентная к лечению.
ПСЕВДОГИПОПАРАТИРЕОЗ
В основе лежит врожденный дефект — нечувствительность периферических тканей к действию ПТГ.
Клинически протекает как гипопаратиреоз, но уровень ПТГ в сыворотке крови нормальный или слегка выше нормы. Характерны низкий рост, короткая шея, короткие IV и V пальцы, подкожные кальцификаты и нарушение половой функции: у женщин аменорея или олигоменорея, у мужчин — импотенция. Клинические проявления гипокальциемии.
ГИПОКАЛЬЦИЕМИЯ ВСЛЕДСТВИЕ НЕДОСТАТКА ВИТАМИНА D
Протекает с повышением секреции ПТГ. Причины:
недостаток ультрафиолетовых лучей;
недостаток витамина D в пище;
синдром мальабсорбции;
лекарства, которые увеличивают метаболизм витамина D и могут вызвать его дефицит (фенобарбитал, фенитион).
Уменьшается всасывание кальция и фосфата в кишечнике. Увеличивается секреция ПТГ.

Рис.17. Проявления недостатка витамина D (рахит, остеомаляция у взрослых)
Лечение хронической гипокальциемии проводится препаратами кальция в сочетании с витамином D.
Назначается элементарный кальций в дозе 1,0—1,5 г/сут.
|
Препараты кальция
|
|
|
|
Препарат |
Содержание элементарного кальция в 1 табл. (мг) |
|
|
Карбонат кальция Карбонат кальция-500 Фосфат кальция Цитрат кальция Ацетат кальция |
250 500
600 200 169 |
|
АНАТОМИЯ, ФИЗИОЛОГИЯ И РЕМОДУЛИРОВАНИЕ КОСТНОЙ ТКАНИ
Кости формируют скелет организма, защищают и поддерживают жизненно важные органы, выполняют функцию депо кальция для нужд всего организма. Две линии клеток кости — созидающая (остеогенные клетки , остеобласты , остеоциты) и разрушающая (многоядерные остеокласты). Клетки костной ткани окружает костный матрикс. Различают незрелый (не минерализованный) костный матрикс — остеоид и зрелый (обызвествлённый, или кальцифицированный) костный матрикс.
Костный матрикс
Зрелый костный матрикс составляет 50% сухого веса кости и состоит из неорганической (50%) и органической (25%) частей и воды (25%).
Органическая часть. Органические вещества костного матрикса синтезируют остеобласты. Макромолекулы - коллагены (коллаген типа I — 90–95% и коллаген типа V) и неколлагеновые белки (остеонектин, остеокальцин, протеогликаны, сиалопротеины, морфогенетические белки, протеолипиды, фосфопротеины), а также гликозаминогликаны (хондроитинсульфат, кератансульфат).
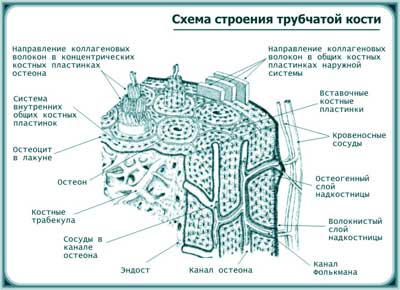
Рис. 18. Анатомия кости.
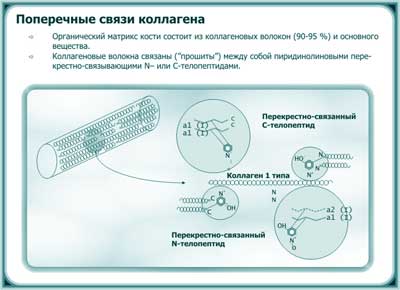
Рис. 20. Схема коллагеновых поперечных связей в кости. Адаптировано из Eyre D.R., 1996.
Остеонектин, относящийся к Ca2+-связывающим белкам, поддерживает в присутствии коллагена осаждение Ca2+ и PO43– и соединён одним своим концом с кристаллом гидроксиапатита, а другим с молекулой коллагена типа I.
Остеокальцин участвует в процессе кальцификации, связываясь с кристаллами гидроксиапатита ‑карбоксиглутаминовой кислоты.при помощи остатков
Морфогенетические белки кости (семейство трансформирующих факторов роста ) — регуляторные (в частности, они индуцируют развитие кости на месте хряща (энхондральный остеогенез).
Неорганическая часть в значительном количестве содержит два химических элемента — кальций (35%) и фосфор (50%), образующие кристаллы гидроксиапатита — [Ca10(PO4)6(OH)2H2O]. В состав неорганической части кости также входят бикарбонаты, цитраты, фториды, соли Mg2+, K+, Na+.
Кристаллы гидроксиапатита соединяются с молекулами коллагена через остеонектин. Такая связка делает кости исключительно устойчивыми к растяжению и сжатию.
В организме взрослого человека содержится около 1000 г кальция. 99% всего кальция находится в костях. Около 99% кальция костей входит в состав кристаллов гидроксиапатита. Лишь 1% кальция костей находится в виде фосфатных солей, именно эти соли легко обмениваются между костью и кровью и играют роль буфера («обменный кальций») при изменениях концентрации кальция в плазме крови.
