
- •Методичні вказівки
- •Зміст модуля I
- •1. Основні хімічні поняття і стехіометричні закони
- •1.1. Предмет хімії і основні хімічні поняття
- •1.2. Основні закони хімічної взаємодії
- •1.3. Запитання для самоконтролю
- •1.4. Задачі для самоконтролю
- •2. Основні класи неорганічних сполук
- •2.1. Оксиди
- •2.2. Гідрати оксидів
- •2.2.1. Основи
- •2.2.2. Амфотерні гідроксиди
- •2.2.3. Кислоти
- •2.4. Запитання для самоконтролю
- •2.4. Задачі для самоконтролю
- •3. Будова атома. Періодичний закон д.І.Менделєєва
- •3.1. Загальні уявлення про будову атома, природа електрона і характеристики його стану в атомі
- •3.2. Квантові числа
- •3.3. Розподіл електронів в атомі, електронні й електронно-графічні формули елементів
- •3.4. Періодичний закон та періодична система елементів д.І.Менделєєва
- •3.5. Радіуси атомів та йонів елементів
- •3.6. Закономірності зміни енергетичних характеристик елементів.
- •Енергія йонізації
- •Енергія спорідненості до електрона
- •Електронегативність атомів
- •3.7. Запитання для самоконтролю
- •3.8. Задачі для самоконтролю
- •4. Хімічний зв’язок. Кристалічний стан речовин
- •4.1. Основні типи хімічного зв’язку. Ковалентний зв’язок
- •4.2. Іонний зв'язок
- •4.3. Металічний зв'язок
- •4.4. Водневий зв'язок
- •4.5. Міжмолекулярна взаємодія
- •4.6. Тверді тіла. Типи кристалічних граток
- •4.7. Запитання та задачі для самоконтролю
- •5. Основи хімічної термодинаміки
- •5.1. Основні термодинамічні поняття
- •5.2. Термохімія.
- •5.3. Напрям перебігу хімічних процесів.
- •5.4. Питання для самоконтролю
- •5.5. Задачі і вправи для самостійної роботи
- •6.Хімічна кінетика і рівновага
- •6.1. Загальні уявлення про швидкість хімічних реакцій
- •6.3. Закон діючих мас
- •6.4. Енергія активації
- •6.5. Вплив температури на швидкість реакції
- •6.6. Каталіз
- •6.7. Хімічна рівновага
- •6.8. Вплив зовнішніх факторів на хімічну рівновагу. Принцип ле Шательє
- •6.9. Запитання та задачі для самоконтролю
- •Список рекомендованої літератури
3.2. Квантові числа
Головне квантове число визначає повний запас енергії електрона (рівень енергії електронного шару), тобто ступінь віддалення його від ядра або розмір електронної хмари (орбіталі) і приймає значення 1, 2, 3, 4, 5, 6, 7 ..., які збігаються з нумерацією періодів у періодичній системі елементів Д. І. Менделєєва. Стан електрона, що характеризується певним значенням головного квантового числа, називають енергетичним рівнем електрона в атомі. Для енергетичних рівнів електрона в атомі, що відповідають різним значенням n прийняті позначення великими латинськими буквами.
Головне квантове число - 1, 2, 3, 4, 5, 6, 7...
Енергетичні рівні – K, L, M, N, O, P, Q...
Максимальна кількість енергетичних рівнів, яку може мати атом в основному стані, відповідає номеру періоду, в якому розміщений певний хімічний елемент.
Орбітальне квантове число l описує форму АО і уточнює енергетичну характеристику стану електрона – його підрівень, що позначається арабськими цифрами 0, 1, 2, 3,... або латинськими буквами s, p, d, f. Орбітальне квантове число може приймати значення від 0 до n-1. Для s-підрівня l=0, для p-підрівня l=1,для d-підрівня l=2, для f-підрівня l=3.
Можлива кількість підрівнів для кожного енергетичного рівня дорівнює номеру цього рівня, тобто головному квантовому числу. Так, на першому енергетичному рівні (n=1) може бути лише один підрівень з орбітальним квантом числом l=0. На другому енергетичному рівні (n=2) можуть бути два підрівні, яким відповідають орбітальні квантові числа l=0; 1. Третій енергетичний рівень (n=3) має три підрівні з відповідними орбітальними квантовими числами: l=0; 1; 2. На четвертому енергетичному рівні (n=4) можуть бути чотири підрівні, кожен з яких має своє значення орбітального квантового числа: l=0; 1; 2; 3.
Відповідно до квантово-механічних розрахунків s-орбіталі мають форму кулі (сферичну симетрію), р-орбіталі – форму гантелі, d – і f-орбіталі – складні форми.
Форми атомних орбіталей (АО), що відповідають різним значенням l наведено на рис. 1.1-1.3. Отже, енергетичний підрівень визначає стан електрона в атомі, що характеризується певним набором квантових чисел n і l, наприклад підрівень 4p: n=4, l=1; підрівень 5d: n=5, l=2 тощо.
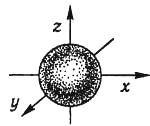
ns-AO, nsl і ns2; n = 1,2,3,4, 5, 6,7; l = 0, тl = 0. Куля (кульова симетрія), всенапрямленність у просторі атома; позначається у графічних формулах як
|
; |
↑ |
; |
↑↓ |
Рис. 3.1.Електронна s-орбіталь і s-електрони
Магнітне квантове число ml, визначає орієнтацію АО в просторі і змінюється від -l до +l, включаючи нульове значення. Магнітне квантове число визначає кількість АО на кожному підрівні: так s-підрівень характеризується однією кулястою атомною орбіталлю (l=0, ml=0); р-підрівень має три АО (l=1, ml=-1, 0, +1); d-підрівень має
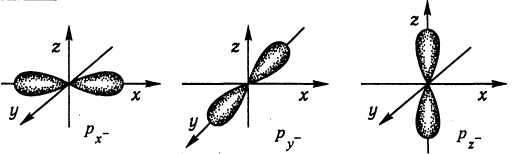
пр-АО, пр1 -пр6, п = 2, 3, 4, 5, 6, 7; l = 1, тl = -1, 0, +1. Гантелеподібні об'ємні фігури, напрямлені за осями координат, позначаються у графічних формулах як
-
↑
↑
↑
↑
↑
↑↓
↑↓
↑↓
тощо
Рис. 3.2. Електронні p-орбіталі і p-електрони

(n-l) d -AO; (n-1)dl - (n-1)d10, n = 4, 5, 6, 7; l = 2; ml = -2, -1, 0, +1, +2. Одна АО — фігура типу труби, замкненої в кільце (тор) з об'ємною гантеллю на осі z. Чотири АО — чотирилопатеві об'ємні фігури, лопаті яких лежать: однієї — на осях x і у (х2-y2), трьох інших — у квадрантах трьох координатних площин (ху, xz, yz) та ще одна фігура на осі z – dz2 . Позначаються у графічних формулах як
|
|
|
|
|
|
↑ |
↑ |
↑ |
↑ |
↑ |
|
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
тощо.
Рис.3.3. Електронні d-орбіталі і d -електрони.
п’ять АО (l=2, ml=-2, -1, 0, +1, +2); f-підрівень має сім АО (l=3, ml=-3, -2, -1, 0, +1, +2, +3).
Слід зазначити, що кожну атомну орбіталь спрощено зображають як енергетичну комірку (квантову комірку) у вигляді □. Для s-електронів може бути лише одна енергетична комірка □; для р-електронів – три □□□ ; для d-електронів – п’ять □□□□□ ; для f-електронів – сім □□□□□□□ . Число енергетичних комірок визначається значенням магнітного квантового числа.
Спінове квантове число ms, характеризує власний момент кількості руху електрона і приймає значення +1/2 або -1/2. Спрощено спін (від англійського spin – крутіння, обертання) можна уявити як рух електрона навколо своєї осі. Спін зображають протилежно напрямленими стрілками: ↑;↓. Спіни електронів, напрямлені в один бік, називаються паралельними, у протилежні – антипаралельними.
