
- •Методичні вказівки
- •Зміст модуля I
- •1. Основні хімічні поняття і стехіометричні закони
- •1.1. Предмет хімії і основні хімічні поняття
- •1.2. Основні закони хімічної взаємодії
- •1.3. Запитання для самоконтролю
- •1.4. Задачі для самоконтролю
- •2. Основні класи неорганічних сполук
- •2.1. Оксиди
- •2.2. Гідрати оксидів
- •2.2.1. Основи
- •2.2.2. Амфотерні гідроксиди
- •2.2.3. Кислоти
- •2.4. Запитання для самоконтролю
- •2.4. Задачі для самоконтролю
- •3. Будова атома. Періодичний закон д.І.Менделєєва
- •3.1. Загальні уявлення про будову атома, природа електрона і характеристики його стану в атомі
- •3.2. Квантові числа
- •3.3. Розподіл електронів в атомі, електронні й електронно-графічні формули елементів
- •3.4. Періодичний закон та періодична система елементів д.І.Менделєєва
- •3.5. Радіуси атомів та йонів елементів
- •3.6. Закономірності зміни енергетичних характеристик елементів.
- •Енергія йонізації
- •Енергія спорідненості до електрона
- •Електронегативність атомів
- •3.7. Запитання для самоконтролю
- •3.8. Задачі для самоконтролю
- •4. Хімічний зв’язок. Кристалічний стан речовин
- •4.1. Основні типи хімічного зв’язку. Ковалентний зв’язок
- •4.2. Іонний зв'язок
- •4.3. Металічний зв'язок
- •4.4. Водневий зв'язок
- •4.5. Міжмолекулярна взаємодія
- •4.6. Тверді тіла. Типи кристалічних граток
- •4.7. Запитання та задачі для самоконтролю
- •5. Основи хімічної термодинаміки
- •5.1. Основні термодинамічні поняття
- •5.2. Термохімія.
- •5.3. Напрям перебігу хімічних процесів.
- •5.4. Питання для самоконтролю
- •5.5. Задачі і вправи для самостійної роботи
- •6.Хімічна кінетика і рівновага
- •6.1. Загальні уявлення про швидкість хімічних реакцій
- •6.3. Закон діючих мас
- •6.4. Енергія активації
- •6.5. Вплив температури на швидкість реакції
- •6.6. Каталіз
- •6.7. Хімічна рівновага
- •6.8. Вплив зовнішніх факторів на хімічну рівновагу. Принцип ле Шательє
- •6.9. Запитання та задачі для самоконтролю
- •Список рекомендованої літератури
3.5. Радіуси атомів та йонів елементів
У визначенні радіуса атома не спостерігається однозначності тому, що ізольований атом або йон не має чітко визначених зовнішніх меж. Тому залежно від типу хімічного зв'язку, структури речовини і ступеня окиснення елемента слід відрізняти такі види радіусів атомів: 1) ефективний радіус атома — радіус, розрахований на основі експериментальних даних між'ядерних відстаней у молекулах і кристалах; 2) ковалентний (атомний) радіус — половина між'ядерної відстані в молекулах або кристалах відповідних простих речовин; 3) металічний (атомний) радіус також дорівнює половині відстані між центрами двох сусідніх атомів у кристалічній гратці металу; 4) йонний радіус — ефективний радіус, розрахований для кристалів з переважно йонним типом зв'язку (аніонний — більший за атомний радіус, катіонний — менший від нього); 5) орбітальний радіус — теоретично розрахована відстань від ядра до головного максимуму електронної густини зовнішньої орбіталі; він є характеристикою ізольованого атома або йона, що не залежить від природи хімічного зв'язку.
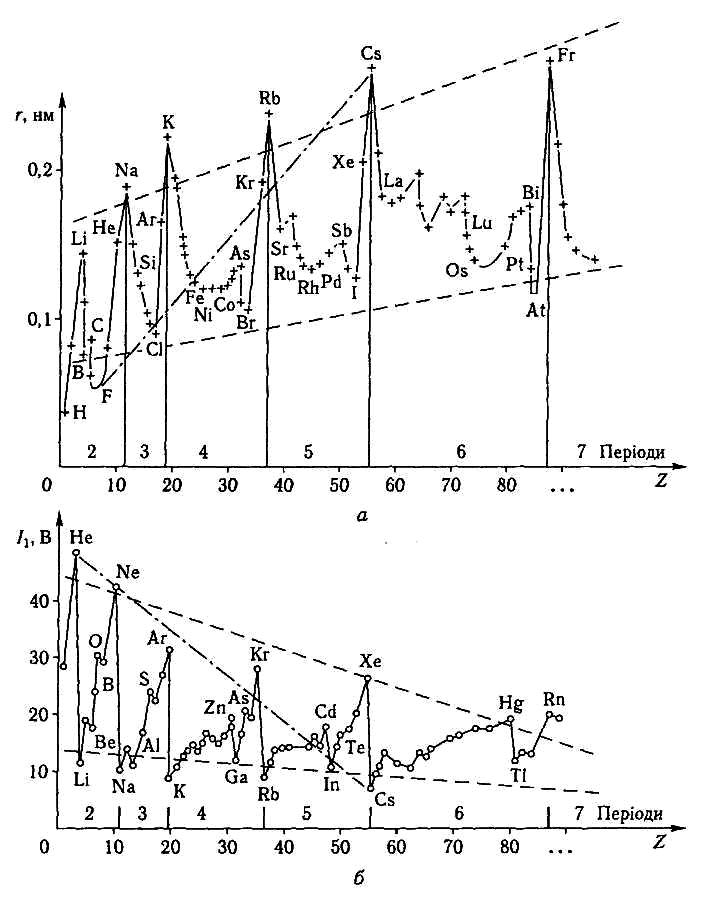
Зміна радіусів атомів елементів у періодичній системі має періодичний характер (див. рис. 3.4, а):
у періодах зліва направо |—»| у міру збільшення зарядів ядер (тобто порядкових номерів) і чисел валентних електронів елементів радіуси зменшуються;
у групах зверху донизу |↓| заряди ядер атомів зростають стрибкоподібно, але одночасно збільшується і число електронних енергетичних рівнів, що призводить до збільшення радіусів атомів. При цьому в групах А таке збільшення відбувається більш різко, ніж у групах В.
3.6. Закономірності зміни енергетичних характеристик елементів.
Хімічна активність елемента визначається здатністю його атомів відщеплювати чи приєднувати електрони. Кількісно ця здатність атомів елементів оцінюється за допомогою двох енергетичних характеристик: 1) енергії (потенціалу) йонізації; 2) енергії спорідненості до електрона.
Енергія йонізації
Енергія йонізації (І, кДж/моль; еВ) — мінімальна енергія, потрібна для відщеплення найслабкіше зв'язаного електрона від незбудженого атома: R0 —> R+ +e, I1> 0, де R0 — символ будь-якого елемента, R+ — символ його йона. Потенціал (і енергія) йонізації є складною функцією деяких характеристик атома: заряду ядра, радіуса атома, конфігурації валентних електронних оболонок. Періодичність зміни величини I1 елементів залежно від їх порядкових номерів подано на рис. 3.4, б.
Аналізуючи данні рис.3.4,б, можна зробити відповідні висновки.
У групах елементів зверху вниз зі зростанням радіусів атомів зменшується сила утримування валентних електронів. Отже, значення енергії йонізації знижується, тобто в цьому напрямі здатність віддавати електрони (окиснюватися) стає енергетично все легшою.
У періодах елементів зліва направо |—»| у міру зменшення радіусів атомів і водночас зростання ступеня заповнення електронами (зокрема, парами електронів) валентних рівнів значення I1 зростають відповідно. Тобто в цьому напрямі відщеплення електронів атомами енергетично утруднюється.
• Враховуючи характер зміни величин I1 у групах і періодах, треба за значити, що зліва в системі елементів, і особливо в її нижній частині,знаходяться найактивніші метали-відновники, здатні енергетично легко окиснюватися. Тобто, енергія іонізації може бути кількісною мірою відновлювальної здатності елемента, його “металічності”.
