
- •Тема 6. Соединения со смешанными функциями
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Гидрокси – и оксоальдегиды и кетоны
- •Оксокислоты
- •Химические свойства
- •2. Кето-енольная таутомерия-оксокислот.
- •Оксокислоты
- •Стереоизомерия
- •(Оптические,
- •Энантиомеры
- •Глоссарий
- •Тема 6. Аминокислоты. Первичная структура белков и пептидов
- •I. Аминокислоты с неполярными (гидрофобными) r-группами (8):
- •II. Аминокислоты с полярными (гидрофильными) незаряженными
- •III. Аминокислоты с полярными (гидрофильными) положительно заряженными радикалами (3):
- •IV. Аминокислоты с полярными (гидрофильными) отрицательно заряженными радикалами (2):
- •III. Биологически важные реакции - аминокислот
- •2. Реакция декарбоксилирования:
- •IV. Аналитические, качественные реакции аминокислот и пептидов.
- •3. Взаимодействие с 2,4-динитрофторбензолом – днфб (реактивом Сенджера):
- •Тема 8. Углеводы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Тема 8-1. Углеводы. Моносахариды Теория
- •Важнейшие природные моносахариды Альдопентозы
- •Альдогексозы Кетогексоза
- •Перспективные формулы Хеуорса
- •Цикло-цепная таутомерия моносахаридов – это существование в водном растворе смеси таутомерных форм, способных превращаться друг в друга через открытую таутомерную форму:
- •3. Мутаротация сахаров При растворении кристаллической таутомерной формы углевода в воде наблюдается явление мутаротации.
- •4. Конформации моносахаридов
- •5. Эпимеризация
- •6. Химические свойства моносахаридов
- •1. Окисление
- •Галактаровая и др.) кислоты
- •Тема 8-2. Ди – и полисахариды
- •Дисахариды
- •Цикло-цепная таутомерия дисахаридов
- •Химические свойства дисахаридов
- •Реакция «серебряного зеркала»:
- •Полисахариды
- •Тема 9. Гетероциклические соединения
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятий и контроль усвоения знаний
- •Содержание этапов занятия
- •Электронное строение «пиррольного» атома азота
- •Шестичленные гетероциклические системы с одним гетероатомом
- •Электронное строение «пиридинового» атома азота
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Химические свойства
- •Шестичленные гетероциклические соединения с двумя гетероатомами Пиримидин
- •Производные пиримидина
- •Полициклические гетероциклы
- •Триптофан
- •Хинолин и изохинолин
- •Нуклеиновые кислоты
- •Общая схема построения нуклеиновых кислот
- •Нуклеиновые кислоты
- •Нуклеотиды
- •Названия нуклеозидов и нуклеотидов
Гидрокси – и оксоальдегиды и кетоны
|
Формула |
Тривиальное название |
ИЮПАК – номенклатура |
Местонахождение в природе и биологическая роль |
|
|
Гликолевый, или гидроксиуксусный альдегид |
2– гидроксиэтаналь |
Предшественник гликолевой кислоты |
|
|
Глицериновый альдегид |
2,3–дигидрокси-пропаналь |
Стандарт конфигурации всех «хиральных» соединений: гидрокси- и аминокислот, углеводов и др. |
|
|
Дигидроксиацетон |
1,3 – дигидрокси-2-пропанон
|
В виде фосфорно-кислого эфира встречается как промежуточный продукт при окислении глюкозы в организме |

П родолжение
таблицы 2
родолжение
таблицы 2
|
Формула |
Тривиальное Название кислот (их солей и эфиров) |
ИЮПАК-номенклатура |
Атомность
|
Основность |
Местонахождение в природе и биологическая роль |
|
|
Винная (виноградная), или ,-дигидрокси янтарная кислота (тартраты) |
2,3-дигидрокси бутандиовая кислота |
4-х атомная |
2х основная |
Содержится в виноградном соке. Является продуктом жизнедеятельности бактерий. Применяется как консервант в пищевой промышленности, в красильном деле. Соли (тартраты) применяются в радиотехнике (пьезокристаллы) и в биохимическом анализе в виде Фелинговой жидкости для обнаружения альдегидов. Существует в трех стереоизомерных формах (L-, D-и мезо-) |
|
|
Лимонная , или -гидрокси--карбокси-глутаровая (цитраты) |
3-гидрокси-3-карбоксипентан диовая |
4-х атомная |
3-х основная |
Содержится в лимонах, апельсинах, винограде, в листьях махорки. Играет важную роль в ЦТК. Соли (цитраты) применяются для консервирования донорской крови, соли железа – при малокровии. |
Оксокислоты
Наиболее важные природные оксокислоты представлены в Таблице 3
Химические свойства
I. Они проявляютобщие свойства, присущие альдегидам или кетонам и кислотам, но как кислоты они сильнее соответствующих карбоновых кислот (сказывается –Iэффект карбонильной группы)
П Специфические свойства, обусловленные взаимным влиянием
>C=Oи -COOHгрупп:
1. Расщепление - и- оксокислот при нагревании – декарбоксилирование:
 ˉ
ˉ
![]() +
+
t°, H2SO4разб.
+
+
t°, H2SO4разб.
 а)
+ CO2
а)
+ CO2
ˉ
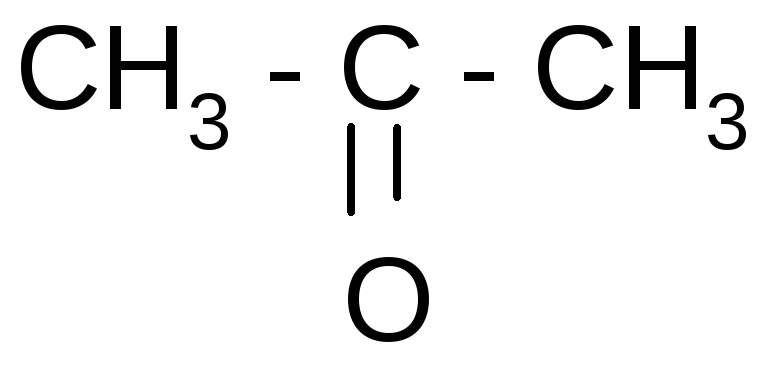 t° комн.
t° комн.

 б)
+ CO2
б)
+ CO2
2. Кето-енольная таутомерия-оксокислот.
 +
+


:
–
кето-форма
енольная форма
ацетоуксусная
кислота (АУК)
Обе формы известны в свободном состоянии и могут быть при определенных условиях выделены. Однако они обе неустойчивы – легко превращаются в равновесную смесь с содержанием кето-формы (93%) и енольной (17%). Стойкость енола по сравнению с другими енольными формами возрастает из-за сопряжения.
Для доказательства существования обеих форм пользуются соответствующими реакциями. Например, как кетон АУК восстанавливается до вторичного спирта, реагирует с HCN, фенилгидразином и т.д. Как енол АУК или ее этиловый эфир (ацетоуксусный эфир) дает окрашивание при действии разбавленного водного раствораFeCl3вследствие образования комплексной железной соли (хелата):

Таблица 3




