
- •Тема 6. Соединения со смешанными функциями
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Гидрокси – и оксоальдегиды и кетоны
- •Оксокислоты
- •Химические свойства
- •2. Кето-енольная таутомерия-оксокислот.
- •Оксокислоты
- •Стереоизомерия
- •(Оптические,
- •Энантиомеры
- •Глоссарий
- •Тема 6. Аминокислоты. Первичная структура белков и пептидов
- •I. Аминокислоты с неполярными (гидрофобными) r-группами (8):
- •II. Аминокислоты с полярными (гидрофильными) незаряженными
- •III. Аминокислоты с полярными (гидрофильными) положительно заряженными радикалами (3):
- •IV. Аминокислоты с полярными (гидрофильными) отрицательно заряженными радикалами (2):
- •III. Биологически важные реакции - аминокислот
- •2. Реакция декарбоксилирования:
- •IV. Аналитические, качественные реакции аминокислот и пептидов.
- •3. Взаимодействие с 2,4-динитрофторбензолом – днфб (реактивом Сенджера):
- •Тема 8. Углеводы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Тема 8-1. Углеводы. Моносахариды Теория
- •Важнейшие природные моносахариды Альдопентозы
- •Альдогексозы Кетогексоза
- •Перспективные формулы Хеуорса
- •Цикло-цепная таутомерия моносахаридов – это существование в водном растворе смеси таутомерных форм, способных превращаться друг в друга через открытую таутомерную форму:
- •3. Мутаротация сахаров При растворении кристаллической таутомерной формы углевода в воде наблюдается явление мутаротации.
- •4. Конформации моносахаридов
- •5. Эпимеризация
- •6. Химические свойства моносахаридов
- •1. Окисление
- •Галактаровая и др.) кислоты
- •Тема 8-2. Ди – и полисахариды
- •Дисахариды
- •Цикло-цепная таутомерия дисахаридов
- •Химические свойства дисахаридов
- •Реакция «серебряного зеркала»:
- •Полисахариды
- •Тема 9. Гетероциклические соединения
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятий и контроль усвоения знаний
- •Содержание этапов занятия
- •Электронное строение «пиррольного» атома азота
- •Шестичленные гетероциклические системы с одним гетероатомом
- •Электронное строение «пиридинового» атома азота
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Химические свойства
- •Шестичленные гетероциклические соединения с двумя гетероатомами Пиримидин
- •Производные пиримидина
- •Полициклические гетероциклы
- •Триптофан
- •Хинолин и изохинолин
- •Нуклеиновые кислоты
- •Общая схема построения нуклеиновых кислот
- •Нуклеиновые кислоты
- •Нуклеотиды
- •Названия нуклеозидов и нуклеотидов
Тема 9. Гетероциклические соединения
Цель занятия:сформировать знания электронного строения и химических свойств гетероциклических соединений, играющих важную роль в биологической химии и медицине, составляющих основу метаболитов и лекарственных веществ.
Конкретные задачи
1. Студент должен знать: строение гетероциклических соединений – пиррола, фурана, тиофена, имидазола, пиразола, пиридина, пиримидина и пурина; электронное строение пиррольного и пиридинового атома азота; ароматичность и критерии ароматичности; реакции электрофильного замещения в гетероциклических ароматических системах; проявление кислотности и основности гетероциклических соединений.
2. Студент должен уметь: писать формулы пяти- и шестичленных гетероциклических соединений с одним или двумя гетероатомами, доказывать их ароматичность; писать уравнения реакций, показывающих их основные, кислотные и ароматические свойства; писать формулы пиримидиновых и пуриновых оснований в лактимной и лактамной формах; составлять структуры нуклеозидов, нуклеотидов, фрагментов первичной структуры нуклеиновых кислот.
Мотивация. Гетероциклические соединения широко распространены в природе и играют важную биологическую роль. Они входят в состав нуклеиновых кислот (пурин, пиримидин), пигментов растений и животных (пиррол), гормонов (индол), витаминов (пиррол, тиофен, пиридин), аминокислот (индол, имидазол, пирролидин), алкалоидов (пиридин, пиперидин); лекарственных препаратов (имидазол, хинолин, индол, пиразолон, пиридин), красителей (-оксииндол).
Вопросы для самоподготовки
1. Напишите структурные формулы 2.5-диметилфурана, 2-аминопиридина,
3-оксииндола, 2,6-диоксипиримидина; 2,6,8-триоксипурина.
2. Получите из пиридина никотиновую кислоту. Напишите уравнение реакции ее с
NH3.
3. Почему мочевая кислота проявляет кислотные свойства?
4. Напишите формулы пиримидиновых и пуриновых оснований, входящих в состав
нуклеиновых кислот.
Этапы занятий и контроль усвоения знаний
|
Этапы занятия |
Формы проведения этапа |
Время, мин |
|
1. Проверка выполнения домашнего задания. |
Проверка преподавателем выполнения домашнего задания в рабочей тетради. |
15 |
|
2. Контроль самоподготовки. |
Тест-контроль по теме занятия и оценка его результатов (0, 5, 10 баллов) |
15 |
|
3. Разбор теоретического материала. |
Устный опрос студентов у доски, объяснение наиболее трудных вопросов преподавателем. |
150 |
Содержание этапов занятия
1-й этап.Преподаватель проверяет наличие выполненного домашнего задания в рабочих тетрадях и оценивает его по пятибалльной системе.
2-й этап. Студент письменно отвечает на билет программированного контроля. Ответ оценивается по принятой балльной системе (0, 5, 10 баллов).
3-й этап.На 1 занятии по теме «Гетероциклические соединения» студенты учатся писать формулы пяти- и шестичленных гетероциклов с одним гетероатомом. Разбирают электронное строение «пиррольного» и «пиридинового» атомов азота, рассматривают свойства, характерные для этих соединений: ароматичность, кислотно-основные, нуклеофильные.
На 2 занятии рассматриваются пяти- и шестичленные гетероциклические соединения с двумя гетероатомами: имидазол, пиразол, пиримидин, окси- и аминопрозводные пиримидина – урацил, тимин, цитозин в лактимной и лактамной формах; конденсированные гетероциклические соединения: индол, пурин, окси- и аминопроизводные пурина – аденин, гуанин, мочевая кислота в лактимной и лактамной форме; разбирается строение нуклеозидов, нуклеотидов, фрагментов полинуклеотидной цепи.
Теория
Пятичленные гетероциклические соединения с одним гетероатомом
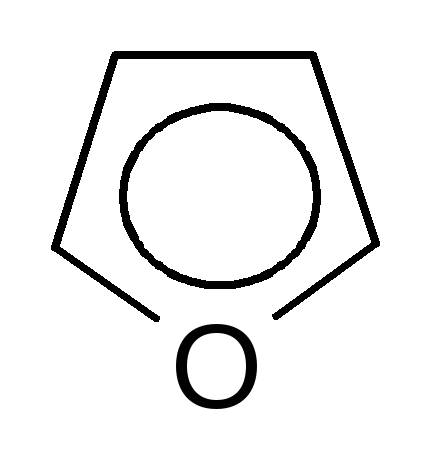

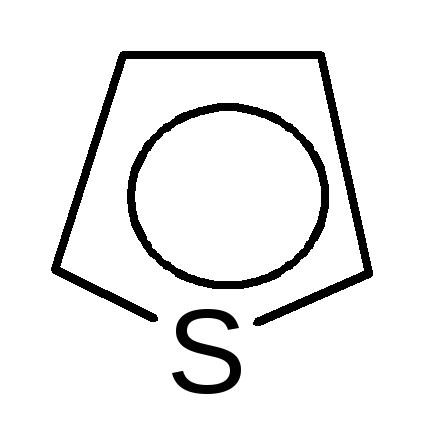
фуран пиррол тиофен
Все эти соединения являются ароматическими, так как отвечают критериям
ароматичности:
S2 – гибридизованные атомы пиррола, фурана, тиофена образуют плоский
- скелет;
количество р- электронов удовлетворяет формуле Хюккеля 4n+2=N, гдеn-целое
натуральное число.
4р Электрона поставляют атомы углерода и 2р- электрона – гетероатомы N,OилиS. Образуется- электронный секстет;
6р- электронов образуют единое сопряженное облако, делокализованное по всему кольцу.
Общей чертой ароматических гетероциклов и производных бензола является
высокая термодинамическая устойчивость.
Отличиеот бензола.
6р Электронов распределяются по пятицентровой системе, поэтому такие системы называются суперароматическими, или -избыточными; их реакции электрофильного замещения идут легче, чем в бензоле.
Из-за влияния гетероатома электронная плотность увеличена в -положениях кольца (2 и 5), поэтому атака электрофильного реагента происходит предпочтительно в эти положения.
Энергия сопряжения у пятичленных гетероциклических соединений меньше, чем у бензола (22-28 ккал/моль, а у бензола– 36 ккал/моль).
Поэтому легче идут реакции с раскрытием кольца. Например, реакции восстановления.
