
- •Тема 6. Соединения со смешанными функциями
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Гидрокси – и оксоальдегиды и кетоны
- •Оксокислоты
- •Химические свойства
- •2. Кето-енольная таутомерия-оксокислот.
- •Оксокислоты
- •Стереоизомерия
- •(Оптические,
- •Энантиомеры
- •Глоссарий
- •Тема 6. Аминокислоты. Первичная структура белков и пептидов
- •I. Аминокислоты с неполярными (гидрофобными) r-группами (8):
- •II. Аминокислоты с полярными (гидрофильными) незаряженными
- •III. Аминокислоты с полярными (гидрофильными) положительно заряженными радикалами (3):
- •IV. Аминокислоты с полярными (гидрофильными) отрицательно заряженными радикалами (2):
- •III. Биологически важные реакции - аминокислот
- •2. Реакция декарбоксилирования:
- •IV. Аналитические, качественные реакции аминокислот и пептидов.
- •3. Взаимодействие с 2,4-динитрофторбензолом – днфб (реактивом Сенджера):
- •Тема 8. Углеводы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Тема 8-1. Углеводы. Моносахариды Теория
- •Важнейшие природные моносахариды Альдопентозы
- •Альдогексозы Кетогексоза
- •Перспективные формулы Хеуорса
- •Цикло-цепная таутомерия моносахаридов – это существование в водном растворе смеси таутомерных форм, способных превращаться друг в друга через открытую таутомерную форму:
- •3. Мутаротация сахаров При растворении кристаллической таутомерной формы углевода в воде наблюдается явление мутаротации.
- •4. Конформации моносахаридов
- •5. Эпимеризация
- •6. Химические свойства моносахаридов
- •1. Окисление
- •Галактаровая и др.) кислоты
- •Тема 8-2. Ди – и полисахариды
- •Дисахариды
- •Цикло-цепная таутомерия дисахаридов
- •Химические свойства дисахаридов
- •Реакция «серебряного зеркала»:
- •Полисахариды
- •Тема 9. Гетероциклические соединения
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятий и контроль усвоения знаний
- •Содержание этапов занятия
- •Электронное строение «пиррольного» атома азота
- •Шестичленные гетероциклические системы с одним гетероатомом
- •Электронное строение «пиридинового» атома азота
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Химические свойства
- •Шестичленные гетероциклические соединения с двумя гетероатомами Пиримидин
- •Производные пиримидина
- •Полициклические гетероциклы
- •Триптофан
- •Хинолин и изохинолин
- •Нуклеиновые кислоты
- •Общая схема построения нуклеиновых кислот
- •Нуклеиновые кислоты
- •Нуклеотиды
- •Названия нуклеозидов и нуклеотидов
Этапы занятия и контроль усвоения знаний
Продолжительность занятия – 4 часа.
|
Этапы занятия |
Формы проведения |
Время |
|
1. Контроль выполнения домашнего задания. |
Проверка преподавателем выполнения домашнего задания в рабочих тетрадях. |
15 мин. |
|
2. Контроль самоподготовки. |
Написание тест – контроля и его оценка. |
15 мин |
|
3. Разбор теоретического материала. |
Опрос студентов у доски, объяснение преподавателем наиболее трудных и важных вопросов, демонстрация моделей, плакатов. |
90 мин |
|
4. Приобретение практических навыков. |
Выполнение лабораторных работ по теме занятия. |
30 мин |
|
5. Оформление протоколов лабораторных работ.
|
Заполнение графы «Визуальные наблюдения» в протоколах лабораторных работ. Самостоятельный анализ полученных данных и формулировка выводов. |
15 мин |
|
6. Проверка и защита протоколов. |
Собеседование и оценка практических навыков преподавателем. |
15 мин |
Содержание этапов занятия
1-й этап.Преподаватель проверяет и оценивает по пятибалльной системе выполнение домашнего задания по заданной теме и отвечает на вопросы студентов.
2-й этап.Студенты письменно отвечают на билет тест – контроля. Ответ оценивается по десятибалльной системе (0, 5, 10 баллов).
3-й этап.При обсуждении теоретического материала необходимо вспомнить свойства карбоновых кислот, спиртов, альдегидов и кетонов как соединений, определяющих общие химические свойства гидрокси- и оксокислот. Разобрать специфические свойства: отношение к нагреванию-,-,-гидроксикислот на примере молочной,
-гидроксимасляной, -гидроксимасляной кислот; способность- гидроксикислот разлагаться при нагревании в присутствии серной кислоты на примере молочной кислоты; реакции декарбоксилирования пировиноградной и ацетоуксусной кислот; кето-енольную таутомерию на примере ацетоуксусного эфира; оптическую изомерию на примере винной и молочной кислот.
4-й этап.Студенты по 2 человека выполняют лабораторные работы по теме занятия.
5-й этап.Студенты оформляют в рабочей тетради протокол лабораторной работы в виде таблицы. Заполняют графы «Наблюдения и выводы»
6-й этап.Студенты предоставляют оформленный протокол и объясняют полученные результаты. Преподаватель оценивает приобретенные практические навыки.
Теория
Органические соединения, содержащие ОН- и >С=О группы, называются гидроксиальдегидами и гидроксикетонами. Важнейшие представители приведены в таблице 1.
Соединения, содержащие -ОН и -СООН группы, называются гидроксикислотами (таблица 2).
Гидроксикислоты
Классификация
Г идроксикислоты
идроксикислоты
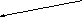

по атомности по основности по взаимному расположению
двух функциональных групп
-
по количеству -ОН групп, включая и входящую в -СООН, бывают двух- и многоатомными
по количеству -СООН групп бывают одно- и многоосновными
бывают -,.-,- и т.д. гидроксикислотами
Виды изомерии: структурная– по положению 2-й функциональной ОН – группы относительно – СООН;стереоизомерия(энантиомерия, диастереомерия)
Химические свойства
IГидроксикислоты проявляютобщие свойстваспиртов и кислот. В зависимости от реагентов и условий проведения реакций взаимодействует ОН или -СООН группа или обе одновременно. Как кислоты они более сильны, чем соответствующие карбоновые кислоты (сказывается –Iэффект ОН- группы).
П. Гидроксикислоты проявляют специфические свойства, которые обусловлены взаимным влиянием ОН- и СООН- групп.
Например, своеобразная реакция отщепления воды при нагревании.
Она позволяет отличить -,-,- и другие гидроксикислоты.
а
 )
)
t°


гидролиз + 2H2O
+ H+илиOH-
лактиды
(циклические
 сложные эфиры)
сложные эфиры)
б) t°

-H2O
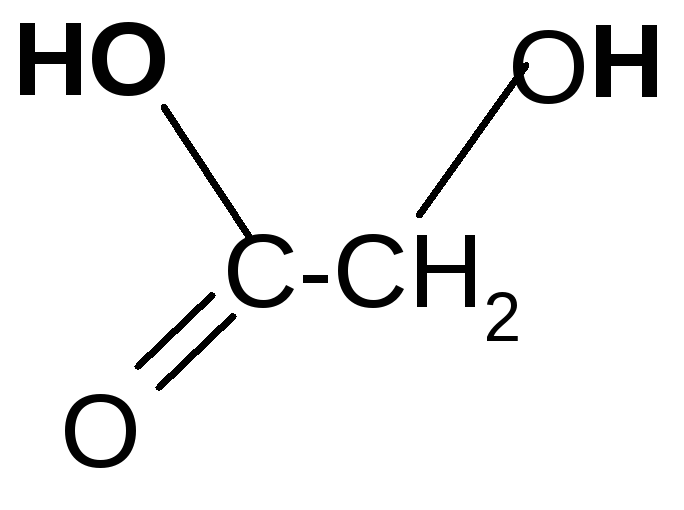
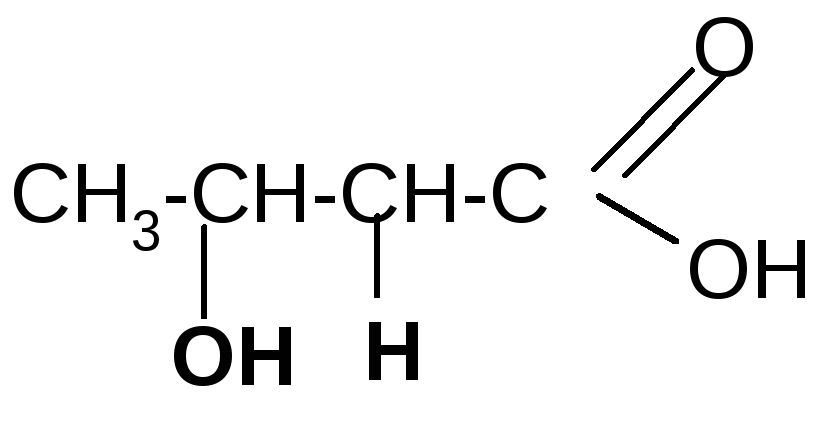
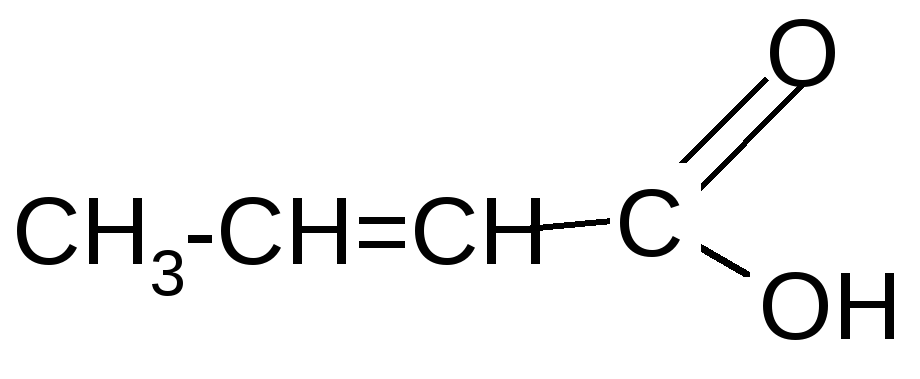
-оксимасляная кротоновая кислота
кислота
в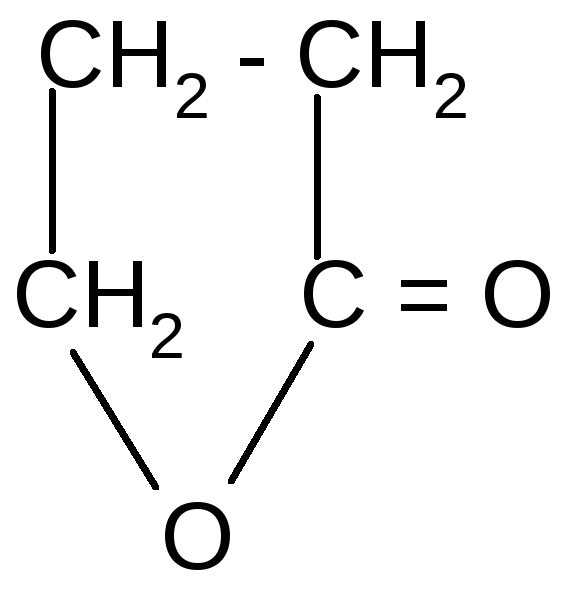 )t°
)t°


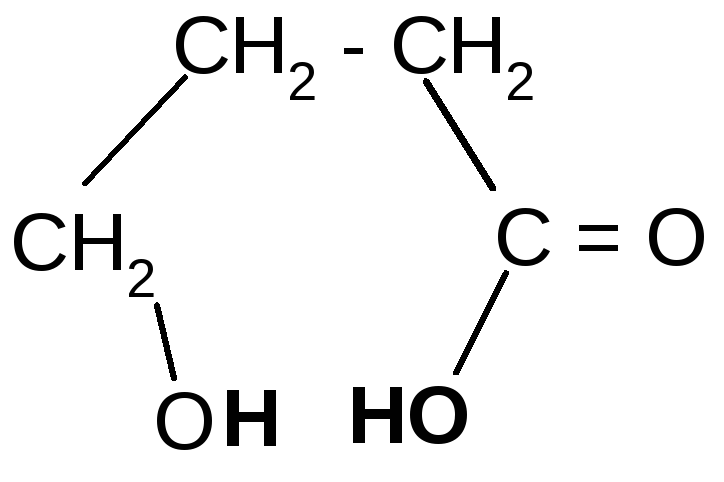 +H2O
+H2O
гидролиз
H+
-гидроксимасляная - бутиролактон
кислота (ГОМК)
ГОМК обладает наркотическим действием, нетоксична, применяется в виде натриевой соли как снотворное средство и при неингаляционном наркозе при операциях.
г)

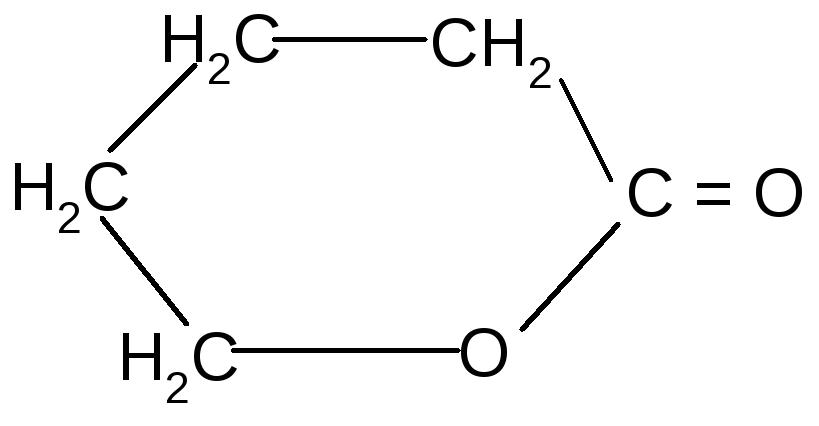
t°

 +
H2O
+
H2O
гидролиз
H+
-гидроксивалериановая - валеролактон
лактон
Лактиды и лактоны могут гидролизоваться в кислой среде с образованием исходных гидроксикислот.
2. Разложение -гидроксикислот при нагревании в присутствииH2SO4:
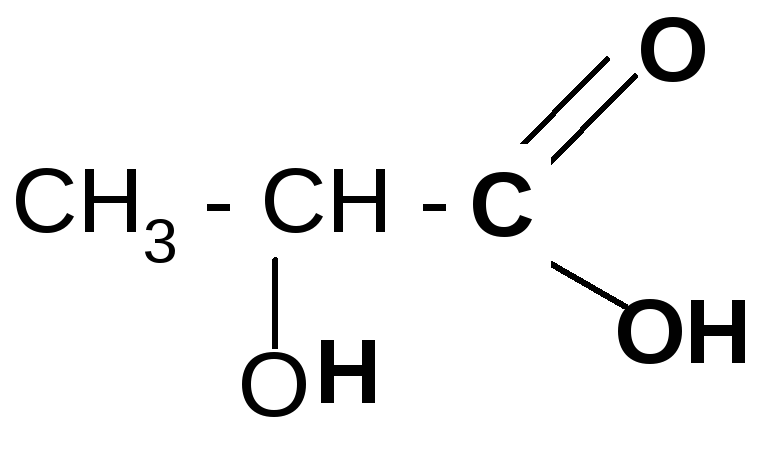
t°, H2SO4
 CH3–CHO
+ HCOOH
CH3–CHO
+ HCOOH
Многоосновные кислоты ведут себя так же. Например,
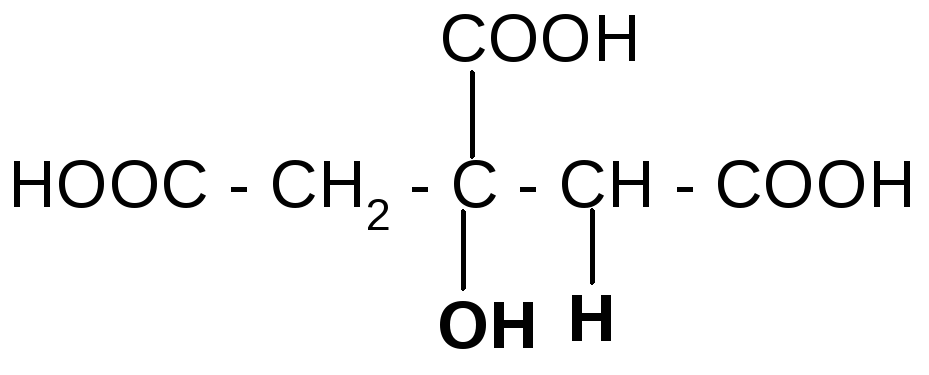
а) при нагревании лимонная кислота будет вести себя как -гидроксикислоты:
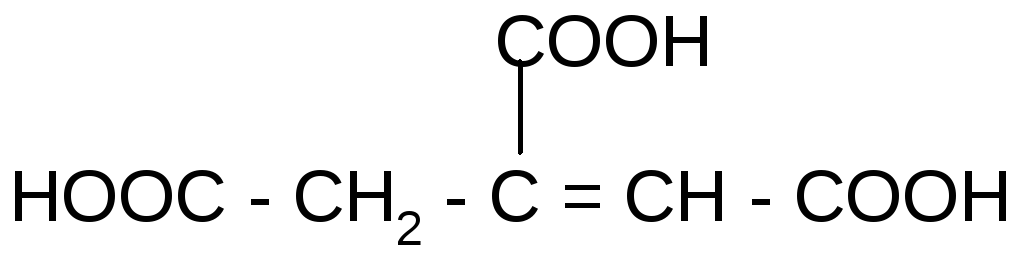
t°


-Н2О
 лимонная кислота
цис-аконитовая к-та
лимонная кислота
цис-аконитовая к-та
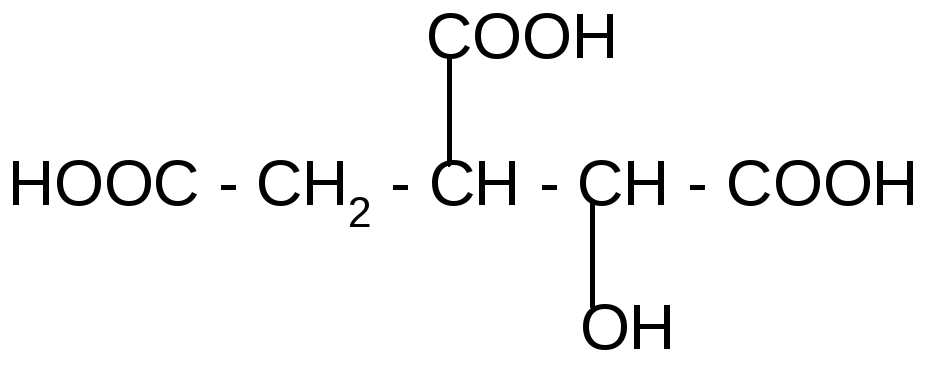
+ Н2О

против правила
Марковникова
изолимонная кислота
б) при действии H2SO4и нагревании она ведет себя как-гидроксикислота, т.е. разлагается с выделением муравьиной кислоты:

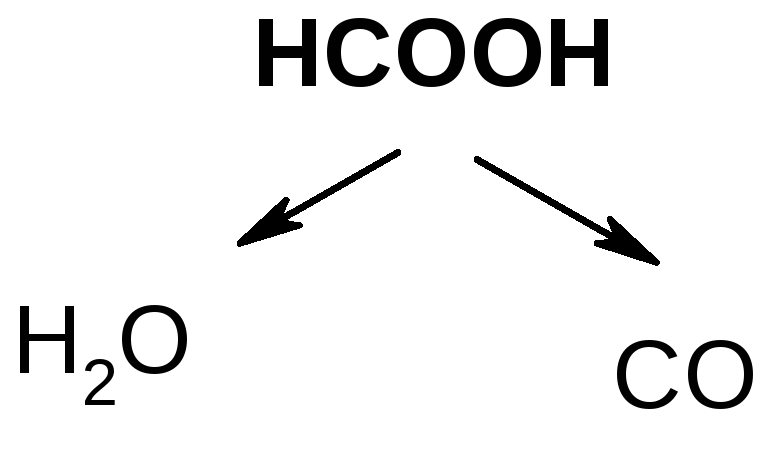
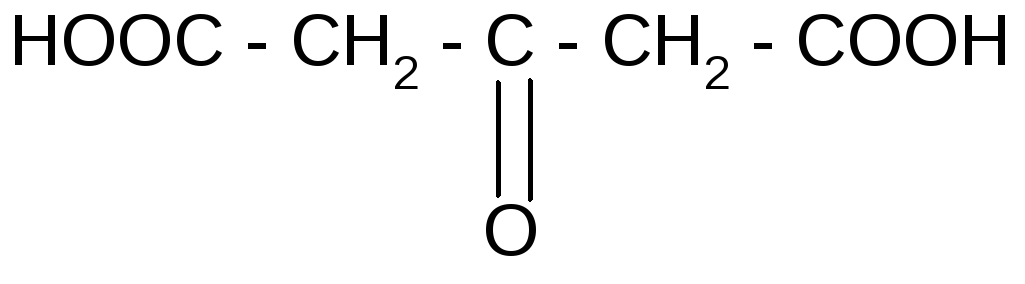 t°,H2SO4
t°,H2SO4
 +
+
ацетондикарбоновая


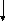
 кислота
кислота
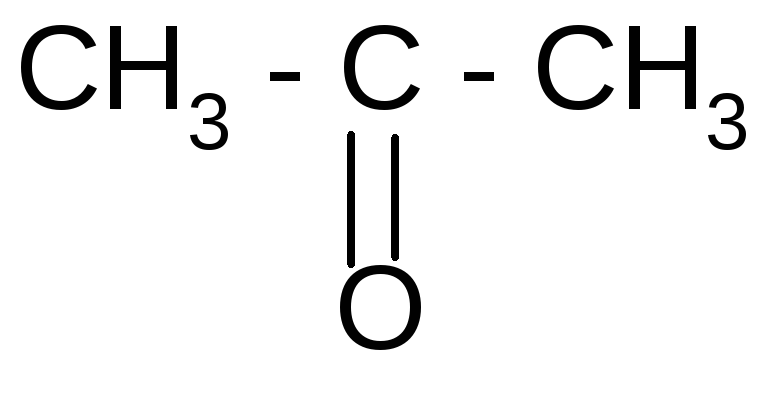 2СO2+
2СO2+
Таблица 1
