
- •Итоговые контрольные задания по общей химии Учебно-методическое пособие
- •Репетитор и эталоны
- •Выполнения типовых заданий
- •По общей химии
- •Введение
- •1. Основные понятия химии
- •2. Химический эквивалент
- •3. Строение атомов. Периодический закон д.И. Менделеева
- •Периодичность изменения общих химических свойств элементов
- •4. Химическая термодинамика
- •Первое следствие.Энтальпия реакции равна разности алгебраических сумм энтальпий образования конечных и исходных веществ:
- •Второе следствие. Энтальпия прямой реакции численно равна энтальпии обратной реакции, но с противоположным знаком:
- •5. Скорость химической реакций
- •6. Химическое равновесие
- •7. Растворы
- •Способы выражения состава раствора (концентрации).
- •Электролитическая диссоциация и ионное произведение воды. Водородный и гидроксильный показатели (рН и рОн).
- •8. Гидролиз солей
- •9. Окислительно-восстановительные реакции
- •Важнейшие окислители и восстановители
- •Влияние различный факторов на овр
- •4. Влияние кислотности среды – pH
- •10. Электродные потенциалы. Гальванические элементы.
- •11. Электролиз
- •2. Растворимость кислот, оснований и солей в воде
- •3. Относительные электроотрицательности атомов элементов
- •4. Константы ионизации некоторых слабых электролитов в водных растворах при 25 0с
- •5. Стандартные энтальпии , энтропии и энергии гиббса образования некоторых веществ при 298 к (25 оС)
- •6. Стандартные электродные (окислительно-восстановительные) потенциалы
- •Литература
- •Содержание
2. Растворимость кислот, оснований и солей в воде
(при комнатной температуре)
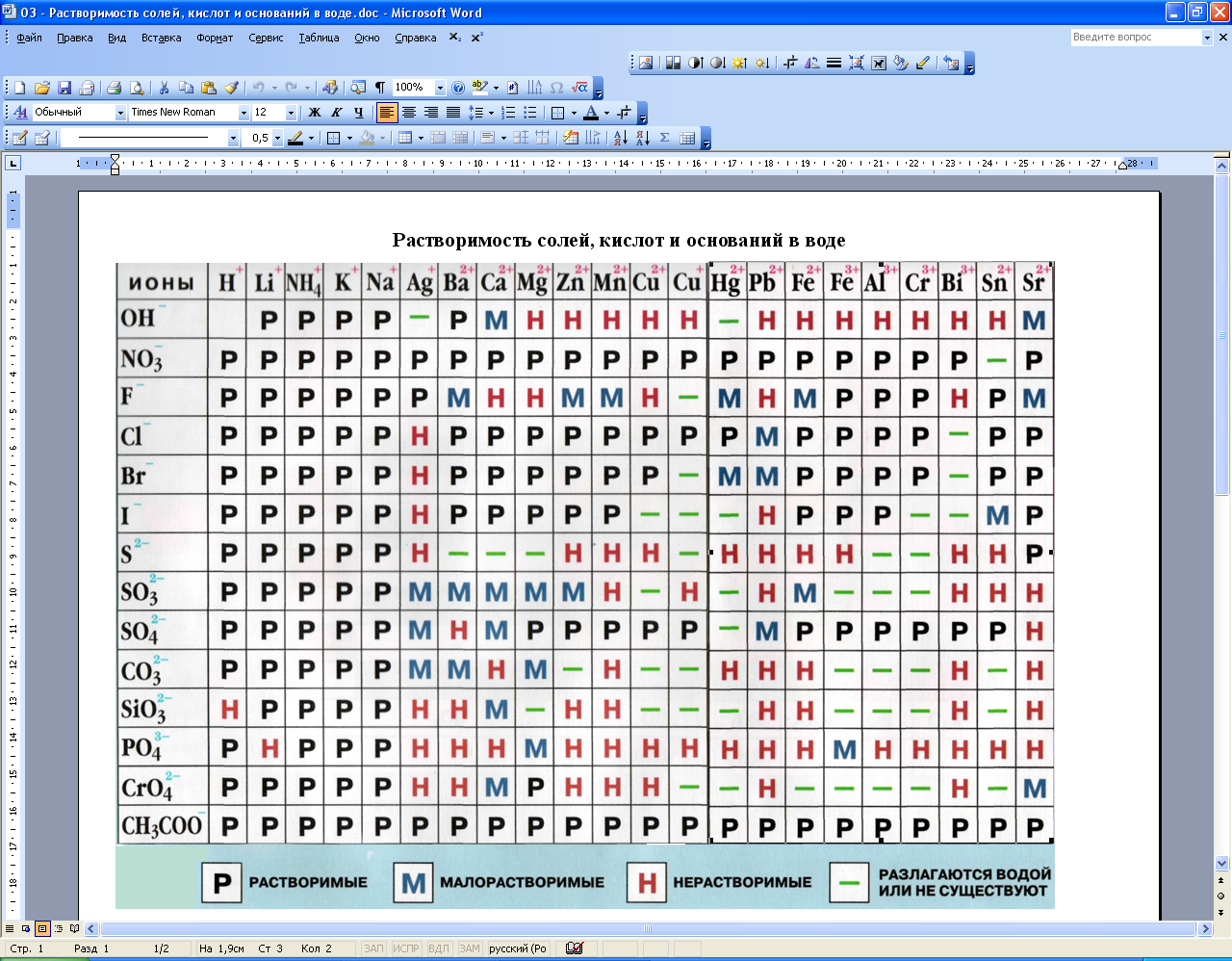
Р – хорошо растворимое вещество (растворяется > 1 г в 100 г воды, или > 0,1 моль/л)
М – малорастворимое вещество (растворяется от 0,1 до 1 г в 100 г воды, или 0,1-0,001 моль/л)
Н – практически нерастворимое вещество (растворяется < 0,1 в 100 г воды, или < 0,001 моль/л)
3. Относительные электроотрицательности атомов элементов
|
I |
II |
III |
IV |
V |
VI |
VII |
VIII | ||
|
Н 2,2 |
|
|
|
|
|
|
|
|
Не – |
|
Li 1,0 |
Ве 1,6 |
В 2,0 |
С 2,6 |
N 3,0 |
О 3,5 |
F 4,0 |
|
|
Nе – |
|
Nа 0,9 |
Мg 1,2 |
Аl 1,6 |
Si 1,9 |
Р 2,2 |
S 2,6 |
Сl 3,1 |
|
|
Аr – |
|
К 0,8 |
Са 1,0 |
Sс 1,3 |
Тi 1,5 |
V 1,6 |
Сr 1,6 |
Мn 1,6 |
Fе 1,8 |
Со 1,9 |
Ni 1,9 |
|
Сu 1,8 |
Zn 1,6 |
Gа 1,7 |
Gе 2,0 |
Аs 2,1 |
Sе 2,5 |
Вr 2,9 |
|
|
Кr – |
|
Rb 0,8 |
Sr 1,0 |
Y 1,2 |
Zr 1,4 |
Nb 1,6 |
Мо 1,8 |
Тс 1,9 |
Ru 2,0 |
Rh 2,0 |
Рd 2,1 |
|
Аg 1,9 |
Сd 1,7 |
In 1,8 |
Sn 1,8 |
Sb 1,9 |
Те 2,3 |
I 2,6 |
|
|
Хе – |
|
Сs 0,7 |
Ва 0,9 |
Lа* 1,2 |
Нf 1,3 |
Та 1,5 |
W 1,8 |
Rе 1,9 |
Оs 2,0 |
Ir 2,1 |
Рt 2,1 |
|
Аu 2,0 |
Нg 1,8 |
Тl 1,4 |
Рb 1,9 |
Вi 2,0 |
Ро 2,2 |
Аt 2,3 |
|
|
Rn – |
|
Fr 0,7 |
Rа 0,9 |
Ас** 1,1 |
* - Лантаниды 1,08 – 1,14 ** - Актиниды 1,00 – 1,20 |
| |||||
|
|
s–элементы |
|
р–элементы |
|
d–элементы |
4. Константы ионизации некоторых слабых электролитов в водных растворах при 25 0с
|
Электролит |
|
Кд |
рК = – lg К
|
|
Азотистая кислота HNO2 |
|
4,0 ∙ 10-4 |
3,40 |
|
Гидрат аммиака NH3 ∙ Н2О |
|
1,8 ∙ 10-5 |
4,75 |
|
Кремниевая кислота Н2SiO3 |
К1 |
2,2 ∙ 10-10 |
9,66 |
|
|
K2 |
1,6 ∙ 10-12 |
11,80 |
|
Сернистая кислота Н2SO3 |
К1 |
1,6 ∙ 10-2 |
1,80 |
|
|
K2 |
6,3 ∙ 10-8 |
7,21 |
|
Сероводородная кислота Н2S |
К1 |
6,0 ∙ 10-8 |
7,22 |
|
|
K2 |
1,0 ∙ 10-14 |
14,00 |
|
Угольная кислота Н2СО3 |
К1 |
4,5 ∙ 10-7 |
6,35 |
|
|
K2 |
4,7 ∙ 10-11 |
10,33 |
|
Уксусная кислота СН3СООН |
|
1,8 ∙ 10-5 |
4,75 |
|
Фосфорная (ортофосфорная) кислота Н3РО4 |
К1 K2 |
7,5 ∙ 10-3 6,3 ∙ 10-8 |
2,12 7,20 |
|
|
К3 |
1,3 ∙ 10-12 |
11,89 |
|
Фтороводородная кислота НF |
|
6,6 ∙ 10-4 |
3,18 |
|
Хлорноватистая кислота НОСl |
|
5,0 ∙ 10-8 |
7,30 |
|
Циановодородная кислота НСN |
|
7,9 ∙ 10-10 |
9,10 |
