
- •Министерство сельского хозяйства и продовольствия республики беларусь
- •Введение
- •Раздел 1. Физиология и биохимия растительной клетки
- •Работа 1. Проницаемость живой и мертвой протоплазмы
- •Работа 2. Влияние ионов калия и кальция на состояние протоплазмы
- •Работа 3. Определение редуцирующих сахаров
- •Работа 4. Определение кислотного числа жиров
- •Работа 5. Определение изоэлектрической точки белка
- •Работа 6. Обнаружение дегидрогеназ в растительных тканях
- •Работа 7. Газометрическое определение активности каталазы растительных тканей
- •Работа 8. Влияние кислотности среды на активность каталазы
- •Работа 9. Влияние температуры на скорость гидролиза крахмала амилазами
- •Раздел 2. Водный обмен растений
- •Работа 10. Определение содержания воды и сухого вещества в растительном материале
- •Работа 11. Получение полупроницаемой перепонки и наблюдение явлений осмоса
- •Работа 12. Явления плазмолиза и деплазмолиза в растительной клетке
- •Работа 13. Определение водного потенциала растительных тканей с помощью рефрактометра (по н. А. Максимову и н. С. Петинову)
- •Работа 14. Определение осмотического потенциала клеточного сока методом плазмолиза
- •Работа 15. Влияние света и влажности воздуха на транспирацию
- •Работа 16. Определение интенсивности транспирации по методу л.А.Иванова (при помощи торсионных весов)
- •Работа 17. Определение относительной транспирации
- •Работа 18. Определение интенсивности транспирации объёмным методом (в модификации в. П. Моисеева)
- •Работа 19. Определение водного дефицита растений
- •Раздел 3. Фотосинтез
- •Работа 20. Изучение химических свойств пигментов зеленого листа
- •Работа 21. Оптические свойства пигментов
- •Работа 22. Определение содержания хлорофилла в листьях
- •Работа 23. Определение интенсивности истинного фотосинтеза по количеству накопленного сухого вещества
- •Работа 24. Определение чистой продуктивности фотосинтеза
- •Раздел 7. Дыхание растений
- •Работа 25. Расходование органических веществ на дыхание
- •Работа 26. Влияние температуры на интенсивность дыхания
- •Работа 27. Определение величины дыхательного коэффициента
- •Раздел 8. Минеральное питание растений
- •Работа 28. Влияние отдельных элементов минерального питания на рост и развитие растений
- •156,36 Г MgSо42н2о содержит 32,06 г s,
- •Работа 29. Определение общей и рабочей адсорбирующей поверхности корней методом д. А. Сабинина и и. И. Колосова
- •Работа 30. Влияние концентрации раствора аммиачной селитры (нитрата аммония) на прорастание семян
- •Работа 31. Антагонизм ионов
- •Раздел 9. Рост и развитие растений
- •Работа 32. Влияние света на рост растений
- •Работа 33. Влияние температуры на рост растений
- •Работа 34. Влияние гетероауксина на рост корней
- •Работа 35. Влияние гетероауксина на укоренение черенков
- •Работа 36. Обнаружение углеводов при прорастании семян масличных культур
- •Раздел 10. Приспособление и устойчивость растений
- •Работа 37. Влияние температуры на прорастание семян
- •Работа 38. Защитное действие сахара на протоплазму при замораживании
- •Работа 39. Определение солеустойчивости растений
- •Раздел 11. Физиология и биохимия формирования качества урожая сельскохозяйственных культур
- •Работа 40. Определение белка в семенах по биуретовой реакции
- •Работа 41. Определение содержания клейковины в зерне
- •Работа 42. Определение индекса деформации клейковины
- •Работа 43. Колориметрический метод определения сахаров
- •Работа 44. Определение содержания крахмала поляриметрическим методом
- •Работа 45. Определение содержания масла в семенах при помощи рефрактометра (по а.И. Ермакову)
- •Работа 46. Быстрый рефрактометрический метод определения йодного числа жиров
- •Работа 47. Определение общей кислотности растительных тканей
- •Работа 48. Обнаружение алкалоидов в растениях
- •Работа 49. Обнаружение дубильных веществ в растениях
- •Работа 50. Определение аскорбиновой кислоты (витамина с)
- •Работа 51. Количественное определение каротина
- •Список литературы
- •Раздел 1. Физиология и биохимия растительной клетки 4
- •Раздел 2. Водный обмен растений 22
- •Раздел 3. Фотосинтез 45
- •Виктор Потапович Моисеев, Николай Петрович Решецкий
- •213407 Г. Горки Могилевской обл., ул. Мичурина, 5
Работа 5. Определение изоэлектрической точки белка
Белки – сложные органические азотсодержащие полимерные соединения, состоящие из аминокислот. Аминокислоты в белках соединяются ковалентными пептидными связями, возникающими при взаимодействии аминогруппы одной аминокислоты с карбоксильной группы другой аминокислоты. Свободные амино- и карбоксильные группы диаминомонокарбоновых и моноаминодикарбоновых аминокислот и другие боковые радикалы белков определяют их кислотно-основные свойства (амфотерность) и заряд. Проявление этих свойств зависит от кислотности среды.
В кислой среде, в результате подавления диссоциации свободных карбоксильных групп, белки заряжаются положительно, т.е. становятся катионами:
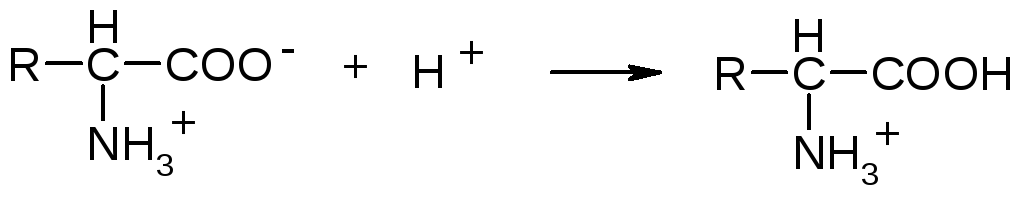
В щелочной среде подавляется диссоциация свободных амино-групп, молекулы белков заряжаются отрицательно и ведут себя как анионы:
![]()
Кислотность среды, при которой устанавливается равенство положительных и отрицательных зарядов и белок становится электронейтральным, называется изоэлектрической точкой (ИЭТ). Белки, у которых ИЭТ находится в кислой среде, называются кислыми. Белки, у которых значение ИЭТ находится в щелочной среде, называются основными. У большинства растительных белков ИЭТ находится в слабокислой среде.
В изоэлектрической точке белок обладает наименьшей растворимостью и легко выпадает в осадок при воздействиях, снижающих гидратацию его молекул (добавлении органических растворителей или солей). При этом молекулы белка слипаются, образуя более крупные частицы, и выпадают из раствора в виде осадка.
Цель работы. Определить значения ИЭТ белков различных фракций (альбуминов, глобулинов, глютелинов, проламинов).
Ход работы. В 8 пронумерованных пробирок приливают воду, 0,01 н. или 0,1 н. раствор уксусной кислоты в количествах, указанных в табл. 5 и тщательно перемешивают, получая растворы с различными значениями рН. В каждую пробирку приливают по 1 мл раствора белка и содержимое пробирок перемешивают. Затем в пробирки добавляют по 2 мл ацетона или спирта, снова перемешивают содержимое и оставляют на 30…40 мин при комнатной температуре. При значении рН, равном или близком к ИЭТ белка, раствор мутнеет или из него выпадает осадок. В таблице 5 отмечают интенсивность помутнения раствора (+), выпадение осадка (++) или его отсутствие (–). ИЭТ белка устанавливают по кислотности среды в пробирке, в которой выпадает больше осадка, либо в которой интенсивность помутнения раствора наибольшая.
Т а б л и ц а 5. Схема приготовления растворов с различными значениями рН и результаты опыта
|
Номер пробирки |
Внесено в пробирки, мл |
рН |
Помутнение (+), образование (++) или отсутствие (–) осадка | ||
|
воды |
0,01 н. СН3СООН |
0,1 н. СН3СООН | |||
|
1. |
8,40 |
0,60 |
- |
5,9 |
|
|
2. |
7,75 |
1,25 |
- |
5,6 |
|
|
3. |
8,75 |
- |
0,25 |
5,3 |
|
|
4. |
8,5 |
- |
0,50 |
5,0 |
|
|
5. |
8,0 |
- |
1,0 |
4,7 |
|
|
6. |
7,0 |
- |
2,0 |
4,4 |
|
|
7. |
5,0 |
- |
4,0 |
4,1 |
|
|
8. |
1,0 |
- |
8,0 |
3,8 |
|
После выполнения работы сравнивают значения изоэлектрической точки анализируемых белков и делают выводы об их аминокислотном составе и свойствах.
Вопросы:
Как классифицируют белки (по строению и составу)?
Назовите свойства и функции белков.
Что понимают под изоэлектрической точкой белка? Значение этого показателя?
Материалы и оборудование: растворы белков или белковых фракций семян зерновых и зернобобовых культур (1,0 г белковых препаратов растворяют в 20 мл 0,5 н. раствора СН3СООNа при нагревании на водяной бане, объем доводят водой до 100 мл), белок куриного яйца (разводят в 10 раз водой и фильтруют через два слоя марли), 0,1 н. раствор СН3СООН (6 мл ледяной уксусной кислоты разбавляют водой до литра), 0,01 н. раствор СН3СООН (0,1 н. раствор СН3СООН разбавляют в 10 раз), этиловый спирт или ацетон, пробирки, штативы.
