- •Министерство сельского хозяйства и продовольствия республики беларусь
- •Введение
- •Раздел 1. Физиология и биохимия растительной клетки
- •Работа 1. Проницаемость живой и мертвой протоплазмы
- •Работа 2. Влияние ионов калия и кальция на состояние протоплазмы
- •Работа 3. Определение редуцирующих сахаров
- •Работа 4. Определение кислотного числа жиров
- •Работа 5. Определение изоэлектрической точки белка
- •Работа 6. Обнаружение дегидрогеназ в растительных тканях
- •Работа 7. Газометрическое определение активности каталазы растительных тканей
- •Работа 8. Влияние кислотности среды на активность каталазы
- •Работа 9. Влияние температуры на скорость гидролиза крахмала амилазами
- •Раздел 2. Водный обмен растений
- •Работа 10. Определение содержания воды и сухого вещества в растительном материале
- •Работа 11. Получение полупроницаемой перепонки и наблюдение явлений осмоса
- •Работа 12. Явления плазмолиза и деплазмолиза в растительной клетке
- •Работа 13. Определение водного потенциала растительных тканей с помощью рефрактометра (по н. А. Максимову и н. С. Петинову)
- •Работа 14. Определение осмотического потенциала клеточного сока методом плазмолиза
- •Работа 15. Влияние света и влажности воздуха на транспирацию
- •Работа 16. Определение интенсивности транспирации по методу л.А.Иванова (при помощи торсионных весов)
- •Работа 17. Определение относительной транспирации
- •Работа 18. Определение интенсивности транспирации объёмным методом (в модификации в. П. Моисеева)
- •Работа 19. Определение водного дефицита растений
- •Раздел 3. Фотосинтез
- •Работа 20. Изучение химических свойств пигментов зеленого листа
- •Работа 21. Оптические свойства пигментов
- •Работа 22. Определение содержания хлорофилла в листьях
- •Работа 23. Определение интенсивности истинного фотосинтеза по количеству накопленного сухого вещества
- •Работа 24. Определение чистой продуктивности фотосинтеза
- •Раздел 7. Дыхание растений
- •Работа 25. Расходование органических веществ на дыхание
- •Работа 26. Влияние температуры на интенсивность дыхания
- •Работа 27. Определение величины дыхательного коэффициента
- •Раздел 8. Минеральное питание растений
- •Работа 28. Влияние отдельных элементов минерального питания на рост и развитие растений
- •156,36 Г MgSо42н2о содержит 32,06 г s,
- •Работа 29. Определение общей и рабочей адсорбирующей поверхности корней методом д. А. Сабинина и и. И. Колосова
- •Работа 30. Влияние концентрации раствора аммиачной селитры (нитрата аммония) на прорастание семян
- •Работа 31. Антагонизм ионов
- •Раздел 9. Рост и развитие растений
- •Работа 32. Влияние света на рост растений
- •Работа 33. Влияние температуры на рост растений
- •Работа 34. Влияние гетероауксина на рост корней
- •Работа 35. Влияние гетероауксина на укоренение черенков
- •Работа 36. Обнаружение углеводов при прорастании семян масличных культур
- •Раздел 10. Приспособление и устойчивость растений
- •Работа 37. Влияние температуры на прорастание семян
- •Работа 38. Защитное действие сахара на протоплазму при замораживании
- •Работа 39. Определение солеустойчивости растений
- •Раздел 11. Физиология и биохимия формирования качества урожая сельскохозяйственных культур
- •Работа 40. Определение белка в семенах по биуретовой реакции
- •Работа 41. Определение содержания клейковины в зерне
- •Работа 42. Определение индекса деформации клейковины
- •Работа 43. Колориметрический метод определения сахаров
- •Работа 44. Определение содержания крахмала поляриметрическим методом
- •Работа 45. Определение содержания масла в семенах при помощи рефрактометра (по а.И. Ермакову)
- •Работа 46. Быстрый рефрактометрический метод определения йодного числа жиров
- •Работа 47. Определение общей кислотности растительных тканей
- •Работа 48. Обнаружение алкалоидов в растениях
- •Работа 49. Обнаружение дубильных веществ в растениях
- •Работа 50. Определение аскорбиновой кислоты (витамина с)
- •Работа 51. Количественное определение каротина
- •Список литературы
- •Раздел 1. Физиология и биохимия растительной клетки 4
- •Раздел 2. Водный обмен растений 22
- •Раздел 3. Фотосинтез 45
- •Виктор Потапович Моисеев, Николай Петрович Решецкий
- •213407 Г. Горки Могилевской обл., ул. Мичурина, 5
Работа 43. Колориметрический метод определения сахаров
Сахара (моно- и олигосахариды) – углеводы, хорошо растворимые в воде и имеющие сладкий вкус. Они широко распространены в растениях, выполняют различные функции и могут накапливаться в корнеплодах, плодах, фруктах и ягодах в значительных количествах.
Колорометрический метод определения сахаров основан на изменении интенсивности окраски раствора глицерата меди при кипячении его с вытяжками сахаров.
Цель работы. Определить содержание сахаров в разных частях корнеплодов репы, сахарной и кормовой свеклы.
Ход работы. Отвешивают из средней пробы 5…10 ± 0,01 г материала, помещают в сосуды микро- или макроразмельчителя (или ступки), приливают 10-кратный объём нагретой до 70 °С воды и извлекают сахара, размельчая навеску в течение 3…5 мин.
Для определения общего количества моно- и дисахаридов, после охлаждения отбирают пипеткой 0,5 мл прозрачной вытяжки в сухую пробирку и добавляют в нее 0,5 мл 1 %-го раствора соляной кислоты. После перемешивания смесь помещают на кипящую водяную баню на 15 мин, затем добавляют 15 мл глицерата меди и нагревают еще ровно 6 мин. После этого пробирки снимают с водяной бани и охлаждают в холодной воде.
Смесь отстаивают, прозрачную жидкость переносят в пробирки и определяют оптическую плотность растворов на фотоэлектроколориметре КФК-2 (рис. 6, стр. 97) при длине волны 582 нм (ручку 1 устанавливают в положение 7).
Для определения редуцирующих сахаров отбирают по 1 мл вытяжки, и прилив 15 мл глицерата меди, нагревают на кипящей водяной бане и далее поступают, как указано выше.
Концентрацию сахаров определяют по калибровочной кривой, построенной по растворам глюкозы известной концентрации (от 0,5 до 10 мг глюкозы в 1 мл раствора).
Количество сахаров вычисляют по формуле:
Х
=![]() %,
%,
где а – концентрация сахаров в пробе, найденная по калибровочной кривой, мг/мл;
V – объем вытяжки, полученной из навески, мл;
m – масса навески, г;
100 – коэффициент перевода в проценты;
1000 – коэффициент перевода грамм в миллиграммы.
Результаты записывают в табл. 52.
Т а б л и ц а 52. Содержание сахаров в корнеплодах различных растений
|
Культура |
Части корнеплода |
Содержание сахаров, % |
|
|
|
|
Вопросы.
Перечислите методы качественного и количественного определения сахаров.
Укажите содержание сахаров в плодах, ягодах, корнеплодах, фруктах.
Материалы и оборудование: сахарная или кормовая свекла, репа, раствор глицерата меди (смешивают объемы реактивов № 1 и № 2 в соотношении 2 : 1; реактив № 1 готовят растворением 8 ± 0,01 г CuSO4 . 5Н2О в 1 дм3 дистиллированной воды, реактив № 2 готовят растворением в воде 150 г едкого натра в мерной колбе на 1 дм3 и объем доводят до метки, перед анализом на 40 мл реактива № 2 добавляют 1 мл чистого глицерина), весы, 1 %-я соляная кислота, измельчители или ступки, пробирки, пипетки на 1 мл, мерные цилиндры на 50…100 мл, КФК-2.
Работа 44. Определение содержания крахмала поляриметрическим методом
Крахмал – полисахарид растений, который запасается в виде крахмальных зерен различной формы и размеров в зерне, клубнях, корнеплодах и плодах. У разных растений в крахмале содержится 10…30 % амилозы и 70..90 % амилопектина (работа 9). У восковидных сортов ячменя, кукурузы, риса крахмал состоит только из амилопектина, а у некоторых гибридов кукурузы и мозговом горохе содержание амилозы может достигать 50…80 %.
Содержание крахмала зависит от вида и сорта растений, а также почвенно-климатических условий, удобрений, орошения и других. Знание этих зависимостей позволяет управлять процессом накопления крахмала в урожае.
Многие углеводы обладают оптической активностью, то есть способностью вращать плоскость поляризации. При определенных условиях опыта величина отношения угла вращения α к плоскости поляризации [α]D, есть величина постоянная и характерная для каждого оптически активного вещества. Для количественного определения крахмала широко применяют поляриметрические методы с использованием поляриметров различных конструкций. Крахмал сначала гидролизуют, а затем в гидролизате определяют угол вращения с помощью поляриметра.
Цель работы. Определить содержание крахмала в зерне злаковых и бобовых культур, клубнях картофеля.
Ход работы. Гидролиз крахмала. Семена злаков или бобовых культур тщательно измельчают на мельнице. Берут навеску 5 ±0,001 г, переносят ее в мерную колбу на 100 мл, приливают 12,5 мл 1 %-ной соляной кислоты. Хорошо размешивают, затем приливают еще 12,5 мл этого же раствора. Колбу нагревают на кипящей водяной бане в течение 15 мин. Во время кипячения содержимое систематически перемешивают. Сначала содержимое колбы загустевает за счет клейстеризации крахмала, а затем разжижается. После гидролиза крахмала приливают 30 мл воды и колбе дают остыть. Затем приливают 5 мл фосфорновольфрамовой кислоты и после взбалтывания доводят объем водой до метки. До определения на поляриметре колбу с гидролизатом можно хранить в холодильнике. Условия гидролиза должно быть одинаковым для всех проб.
При определении крахмала в клубнях картофеля предварительно извлекают из них сахара концентрированным спиртом. Для этого к средней пробе клубней, измельченной на размельчителе, ткани добавляют концентрированный этиловый спирт, перемешивают и отфильтровывают на бумажном фильтре. Фильтрат выбрасывают, а из оставшейся массы берут навеску 15 ±0,001 г и растирают дополнительно в ступке в 5 мл 5 %-ной соляной кислоты до однородной массы. Затем, полученную смесь, переносят в мерную колбу на 100 мл и добавляют 25 мл 1 %-ной соляной кислоты, одновременно ополаскивая ступку. Колбу нагревают на кипящей водяной бане в течение 15 мин. В дальнейшем поступают так, как указано выше, при определении крахмала в муке семян. Перед определением угла вращения, полученный экстракт фильтруют в сухую колбу. Исследуемые растворы должны быть прозрачными (бесцветны или слабо окрашены). Фильтрат наливают в поляризационную трубку поляриметра и определяют угол вращения.
Подготовка прибора. Поляриметр (рис. 8) состоит из поляризатора (1) и анализатора (2), разделенных промежутком для помещения поляриметрической трубки (3) с раствором изучаемого вещества, источника света (4) и блока питания (5).
|
1
3
2
4
5
5 |
6
8
9
10
7 |
Рис. 8. Поляриметр СМ-1 с круговой шкалой: 1– поляризатор; 2 – анализатор; 3 – поляриметрическая трубка с анализируемым раствором; 4 – источник света; 5 – блок питания; 6 – окуляр анализатора; 7 – муфта окуляра; 8 – винт анализатора; 9 – круг; 10 – нониус.
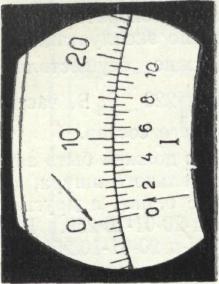
Шкала на лимбе поляриметра разделена на градусы от 0 до 360 ºС. Измерения проводят с помощью нониусов, которые имеют по 10 делений (цена одного деления 0,05º). При измерении следует пользоваться двумя нониусами, расположенными на противоположных концах, для учета эксцентриситета круга при больших углах вращения.
Перед определением угла вращения нужно проверить нулевую точку прибора. Для этого производят наблюдения с поляриметрической трубкой, наполненной водой. Включают блок питания (5) источника света (4). Окуляр (6) анализатора устанавливают на резкость по глазу перемещением муфты (7). Затем вращают винт (8), приводящий анализатор в движение вправо или влево, добиваясь равномерности освещения и однородности поля зрения (рис. 9, б). Нулевые деления круга и нониуса должны совпадать (рис. 9, а). При несовпадении нулевого деления и круга нониуса делают несколько отсчетов и устанавливают среднюю поправку (+) или (-). Отсчеты производят до сотых долей градуса.
Определение угла вращения. Поляриметрическую трубку наполняют испытуемым раствором до краев так, чтобы образовался выпуклый мениск, затем прикрывают круглым стеклышком, надвигая его с края трубки до необходимого положения, и наблюдают, чтобы под стеклышком не осталось пузырьков воздуха. После этого навинчивают шайбу с резиновой прокладкой. В трубках с расширением пузырьки воздуха можно загнать в расширение, чтобы они не мешали определению. Поляриметрическую трубку с анализируемым раствором вкладывают в промежуток между поляризатором и анализатором и закрывают шторку. Отсчет угла вращения производят по шкале, соединенной с анализатором, который вращают вокруг оси прибора с помощью винта (8). Если плоскость поляризации анализатора будет установлена под правильным углом, то лучи от призм поляризатора будут проходить одинаково через анализатор и обе половины поля зрения, и будут освещены одинаково, но слабо (рис. 9, б). Измерения проводят по двум нониусам. Угол вращения устанавливают с учетом поправки, установленной ранее.
|
|
|
|
|
а |
б |
в |
Рис. 9. Нониус поляриметра с круговой шкалой и виды полей зрения у поляриметра: а – начальное положение нониуса после установки анализатора на равную яркость (б) частей поля зрения при введенной кювете с водой; в – вид поля зрения после ввода наполненной анализируемым раствором кюветы.
Содержание крахмала для зерновых вычисляют по формуле:
х = ka·100/0,3468·(100 – b),
где х – количество крахмала, % на сухое вещество;
k – переводной коэффициент равный для пшеницы 1,898; кукурузы – 1,879; ржи – 1,885; ячменя – 1,912; овса – 1,914; риса – 1,866; просо – 1,818; гречихи – 1,876;
a – угол вращения, град;
b – влажность размолотого зерна в %.
Содержание крахмала в клубнях картофеля вычисляют по формуле:
х = V·a·100·0,3468/195,4·g·n,
где х – количество крахмала, % на сырое вещество;
V – объем гидролизата, мл;
а – угол вращения, град;
g – длина трубки, дм;
n – масса навески, г;
195,4 – фактор для крахмала картофеля соответствующий [α]D;
0,3468 – коэффициент переводы в градусы круговой шкалы.
Полученные данные заносят в табл. 53 и делают выводы.
Т а б л и ц а 53. Результаты определения крахмала в __________
|
Объект |
Масса навески, г |
Угол вращения, град. |
Содержание крахмала, % |
|
|
|
|
|
Вопросы:
Из каких компонентов состоит крахмал? Строение, соотношение и свойства компонентов крахмала.
Сколько крахмала содержится в клубнях, корнеплодах, зерне, плодах?
Материалы и оборудование: поляриметр СМ-1, колбочки на 50 и 100 мл, фарфоровые чашки, водяная баня, фильтры, 1 %-ный и 5 %-ный растворы соляной кислоты, 5 %-ный раствор фосфорновольфрамовой кислоты.