
Яцюк, Зубкова _Основы биоорганической химии
.pdf
сложноэфирная |
NH2 |
||
связь |
N |
N |
|
OH OH OH |
|||
|
|
||
HO-P- O-P-O- P-O-CH |
N |
N |
|
2 |
N-гликозидная |
||
O O O |
O |
связь |
|
|
|||
ангидридные OH OH связи
АТФ (аденозинтрифосфат)
Ангидридные связи между остатками фосфорной кислоты обладают большим запасом энергии (~32 кДж/моль), поэтому их называют макроэргическими. При гидролизе АТФ до АДФ и АМФ эта энергия выделяется. Важнейшая роль АТФ – поставщик энергии во всех живых клетках.
С участием АТФ и АДФ в организме осуществляется важнейший биохимический процесс – перенос фосфатных групп. Образование фосфатов – типичная реакция в метаболизме углеводов:
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|||
|
|
|
CH2OH |
|
|
|
O=P-O-CH 2 |
O |
OH |
|||||||||
|
|
|
||||||||||||||||
|
|
|
|
|
O |
|
OH |
|
HO |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
OH |
|
+ АТФ |
|
|
|
|
OH |
|
|
|
+ АДФ |
||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
OH |
|
|
|
HO |
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
глюкоза |
|
|
|
глюкозо-6-фосфат |
||||||||||||
АТФ активирует α-аминокислоты в биосинтезе белков:
NH2
N 
 N
N
OH OH OH
N N
CH3-CH-COOH + HO-P- O-P-O- P-O-CH 2
NH2 |
O O O |
O |
|
||
аланин |
АТФ |
|
OH OH
211
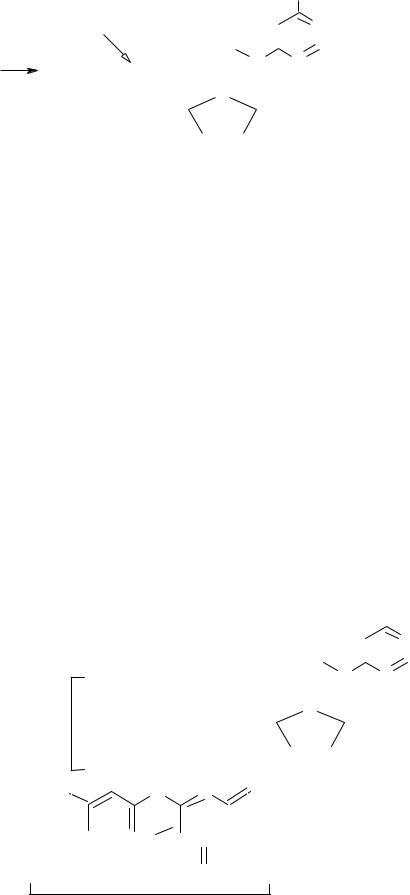
ангидридная |
|
|
|
|
N |
|
|
|
|
|
NH2 |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|||||||||
связь |
OH |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
N |
N |
|
OH |
OH |
|||||||
CH -CH-C-O- P-O-CH |
2 |
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ HO-P-O-P-OH |
||||||||
NH2 O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|||||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пирофосфорная кислота |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
OH OH |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
аминоациладенилат |
|
|
|
|
|
|
|
|
|
|||||||||||
При взаимодействии α-аминокислоты с молекулой АТФ образуется смешанный ангидрид аминокислоты и АМФ – аминоа- циладенилат. Ангидриды кислот являются более активными ацилирующими средствами, чем сами кислоты. Активированная аминокислота затем взаимодействует с аминогруппой следующей аминокислоты в синтезе пептидов.
Нуклеотидную природу имеет никотинамидадениндинуклеотид (НАД+) – кофермент дегидрогеназ, который является участником окислительно-восстановительных реакций (см. стр. 148). С участием НАД+ протекают реакции окисления спиртов в альдегиды (ретинол – ретиналь и др.).
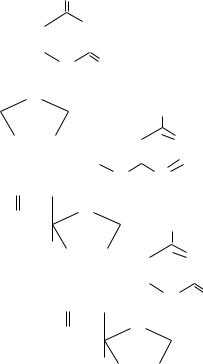
Флавинадениндинуклеотид (ФАД) является метаболически активной формой рибофлавина (витамина B2).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нуклеотидный фрагмент |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
NH2 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
N |
||||||
|
|
|
|
|
|
|
CH |
2- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
O-P-O- |
P-O-CH2 |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
фрагмент |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
HO |
|
|
|
|
|
H |
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
рибитола |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
HO |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
HO |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
H3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C
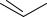
 N
N
 NH
NH
O
фрагмент изоаллоксазина
212

O
|
|
|
|
|
|
5 4 |
3 |
|
NH |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
6 |
1 |
2 |
|
O У |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
-O-CH |
2 |
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|||||||||
|
|
|
3' |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
O OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
A |
||||||||
|
|
|
5' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
N |
|
N |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
HO-P-O-CH 2 |
O |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
O |
|
|
|
|
|
|
|
|
NH2 |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
3' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
|
|
OH |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
5' |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
HO-P-O-CH 2 |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
Ц |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
OH |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
HO-P-O- |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
||||
Вторичная структура нуклеиновых кислот – пространст-
венная организация полинуклеотидных цепей, т.е. определенное расположение полинуклеотидной цепи в пространстве.
В1953 г. Уотсон и Крик описали вторичную структуру ДНК
ввиде двойной спирали (рис. 7). Согласно этой модели молекула ДНК состоит из двух полинуклеотидных цепей, правозакрученных вокруг общей оси. Диаметр спирали 1,8-2,0 нм. Две полинуклеотидные цепи антипараллельны, т.е. направления образования фосфодиэфирных связей у них противоположны – в одной 3’→5’, в другой 5’→3’. Остатки пуриновых и пиримидиновых оснований направлены внутрь спирали. Вторичная структура стабилизируется водородными связями между нуклеиновыми основаниями двух цепей. Каждый виток спирали содержит 10 пар оснований.
214

Рис. 7. Вторичная структура ДНК.
Водородные связи возникают между пуриновым основанием одной цепи и пиримидиновым – другой. Такие пары оснований называются комплементарными. В молекуле ДНК аденину комплементарен тимин, гуанину – цитозин:
|
|
|
|
|
|
NH |
: |
|
|
|
|
|
|
|
|
|
|
O: |
|
|
|
H N |
||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
N |
|
|
|
|
|
N : |
|
|
|
|
|
|
N |
|
|
|
|
|
|
N H |
:N |
|||||||
|
|
|
|
|
HN |
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
N |
O N |
|
|
|
|
|
|
N N |
|
NH2 :O N |
||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|||||||||
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
A |
|
|
|
|
T |
|
|
|
|
|
Г |
|
|
|
Ц |
|||||||||
Комплементарность цепей составляет химическую основу важнейшей функции ДНК – хранения и передачи наследственной информации. Сохранность нуклеотидной последовательности является залогом безошибочной передачи генетической информации. Однако нуклеотидная последовательность ДНК под действием некоторых факторов может изменяться – происходят мутации.
215




Если в структуре жира преобладают остатки насыщенных карбоновых кислот, то жир твердый, если преобладают остатки ненасыщенных кислот, то жир жидкий (масло). Как правило, животные жиры твердые, растительные – жидкие.
Жиры, включающие остатки одинаковых кислот, называют простыми, остатки разных жирных кислот – смешанными.
Жиры называют по тривиальной номенклатуре, заменяя суффикс «-овая» в названии кислоты на «-ин» (тристеарин, трипальмитин), и по систематической номенклатуре как сложные эфиры глицерина, используя суффикс «-оил» (тристеароилглицерин, трипальмитоилглицерин). Например:
|
CH2-O-CO-C 17 H35 |
|
|
CH2-O-CO-C 15 H31 |
||
|
|
|||||
|
CH -O-CO-C 17 H35 |
|
|
|
|
CH -O-CO-C 17 H33 |
|
|
|
|
|
||
|
|
|||||
|
|
|
|
|
|
|
CH2-O-CO-C 17 H35 |
CH2-O-CO-C 17 H31 |
|||||
тристеарин |
α-пальмито-β-олео-α'-линолеин |
|||||
(тристеароилглицерин) |
(1-пальмитоил-2-олеоил- |
|||||
|
|
3-линолеоилглицерин) |
||||
Так как жиры являются сложными эфирами, то для них характерны реакции гидролиза как в кислой, так и в щелочной среде.
Кислотный гидролиз обратим, в результате образуются глицерин и соответствующие карбоновые кислоты:
|
CH2-O-CO-C 17 H35 |
H O, H+ |
|
|
CH2-OH |
|
|||
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH -O-CO-C 17 H35 |
2 |
|
|
|
|
CH -OH |
+ 3 C17 H35 -COOH |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
стеариновая кислота |
CH2-O-CO-C 17 H35 |
|
CH2-OH |
|||||||
|
|
||||||||
|
|
тристеарин |
|
глицерин |
|
||||
При щелочном гидролизе жиров образуются глицерин и соли высших карбоновых кислот:
|
CH2-O-CO-C 17 H33 |
H2O, NaOH |
|
CH2-OH |
|
||||
|
|
|
|||||||
|
|
CH -O-CO-C 17 H33 |
|
|
|
||||
|
|
|
|
|
|
|
CH -OH + 3 C17 H35 -COONa |
||
|
|
|
|||||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
олеат натрия |
CH2-O-CO-C 17 H33 |
|
CH2-OH |
|||||||
|
|
||||||||
|
|
триолеин |
|
глицерин |
|
||||
Соли высших карбоновых кислот нзываются мылами. Вот почему жиры относят к омыляемым липидам. Натриевые и кали-
219



 N
N  N
N





 NH
NH