
posobie_hirurg_sepsis
.pdf
&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
|
|
|
|
Продолжение табл. 18 |
|
|
|
|
|
|
|
1 |
2 |
|
3 |
|
4 |
Причина сепсиса |
Enterobacter |
(>50%), |
АМП/СБ |
или |
Фторхинолоны; |
– деструктивный |
Enterococcus |
spp. |
АМО/КК |
|
ЦС-3 + клинда- |
холецистит (хо- |
(10-20%), Ps. aerugi- |
|
|
мицин; цефтриак- |
|
лангит) |
nosa (10%), |
анаэро- |
|
|
сон + АГ; АСпен |
|
бы (НАИ – 15%) |
|
|
+ АГ; ПИП/ТАЗ |
|
|
|
|
|
|
или ТК/КК; ме- |
|
|
|
|
|
ронем или тиенам |
Обозначения: АГ – аминогликозиды; АС – антибиотики - синтетические пе- нициллины; НАИ – неклостридиальная анаэробная инфекция; ЦС – цефа- лоспорины (соответственно 2, 3, 4 поколения); АМП/СБ – ампициллин + сульбактам (сульбактам – блокатор β-лактамной активности микроорганиз- мов); АМО/КК – амоксициллин + клавулановая кислота (клавулановая ки- слота – блокатор β-лактамной активности микроорганизмов); ПИП/ТБ – пи- перациллин + тазобактам; ТК/КК – тикарциллин + клавулановая кислота.
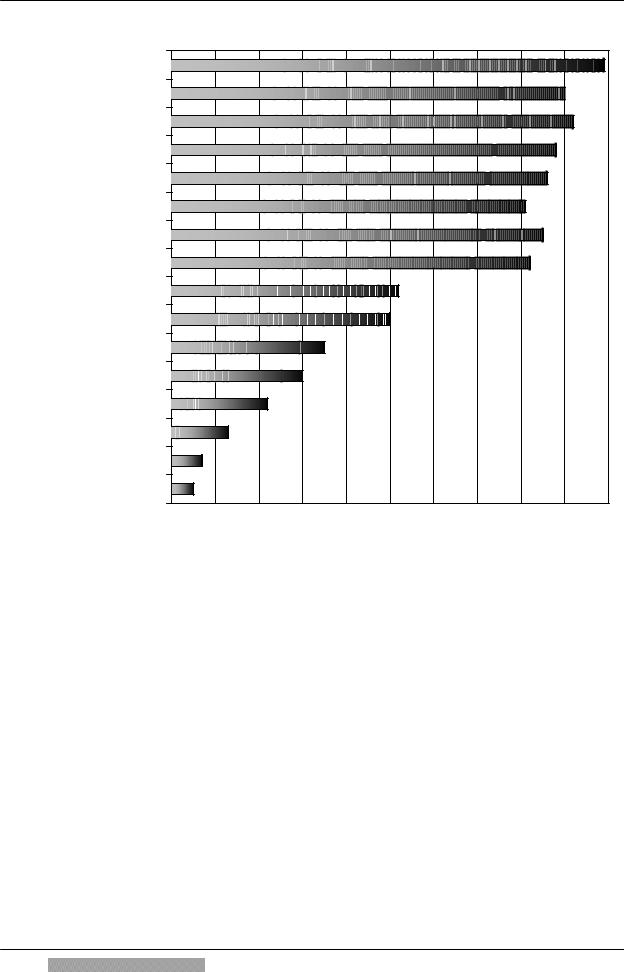
антибиотикоиндуцированной токсемии препараты антимикробного действия неравнозначны (рис.23). Среди них наибольшую опасность представляют β- лактамные антибиотики (среди них особая роль принадлежит пенициллинам и цефалоспоринам, особенно, 1-2-го поколения). Самым низким токсикоин- дуцирующим потенциалом обладают карбапенемы (тиенам, меронем). Про- межуточную позицию занимают современные аминогликозиды (3-й генера- ции) и фторхинолоны.
Высокая вероятность того, что назначенная эмпирическая комбина-
ция будет эффективно воздействовать на все основные возбудители сепсиса при назначении:
vцефалоспоринов 3-4-й генерации (цефотаксима, роцефина, цеф- пирома, цефепима и др.) в сочетании с аминогликозидами последних поко- лений (амикацин, сизомицин, нетромицин) и тейкопланином (для усиления
антианаэробного спектра этой комбинации она может сочетаться с введением метронидазола);
vцефалоспоринов 3-4-й генерации в сочетании с фторхинолонами (норфлоксацин, офлоксацин, ципрофлоксацин) и метронидазолом;
vполусинтетических пенициллинов последних поколений (пипе- рациллин, назоцин, азлоциллин, тикарциллин) в сочетании с аминогликози- дами и метронидазолом;
vаминогликозидов в комбинации с синтетическими пенициллина- ми/ингибиторами β-лактамаз (аугментин, бетабактил, уназин, тиментин и др.);
116
&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
Пенициллин
Ампицилин
Карбенициллин ЦС-1 ЦС-2 Азактам
Стрептомицин
Канамицин
Левомицетин
Гентамицин
Ципрофлоксацин
Офлоксацин ЦС-3-4
Амикацин
Тиенам
Меронем













 Токсикоиндуцирующий потенциал
Токсикоиндуцирующий потенциал
Рис. 23. Способность препаратов антимикробного действия к токсикоиндуцированной токсемии.
v цефалоспоринов 3-4-й генерации в сочетании с клиндамицином и ряд других комбинаций.
Высокой эффективностью при проведении антимикробной терапии хирургического сепсиса различного генеза обладает применение карбапене- мов – тиенама (имипенема/цилостатина) или меронема. В настоящее время доказано, что, несмотря на высокую стоимость карбапенемов, их высокая эффективность при лечении сепсиса экономически более выгодна, чем ис- пользование лекарственных комбинаций. Эти антибиотики являются препа- ратами выбора при молниеносном течении сепсиса, септическом шоке, от- сутствии эффекта от проводимого антибактериального лечения, прогресси- рующем нарастании признаков эндотоксикоза и полиорганной недостаточно- сти. Так, по данным Б.Р. Гельфанда с соавт. (1999) клиническая эффектив-
117

&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
ность меронема у больных сепсисом (с тяжестью состояния 20-25 баллов по шкале SAPS, при прогнозируемой летальности 61-67%) составила 81%!
Для усиления антимикробного эффекта совместно с антибиотиками применяют растворы антисептиков (хлоргексидин, димексид), гранулоцит- колониестимулирующий фактор, гамма-интерферон, иммуноглобулины, а также озонсодержащие растворы. Среди последних наибольшее применение получили оксигенированные жидкости и гипохлорит натрия, получаемый электрохимическим способом из физиологического раствора поваренной со- ли (100-600 мг/л). При этом гипохлорит натрия используется при лечении хирургического сепсиса для внутривенного введения (проведения непрямого электрохимического окисления крови с целью детоксикации организма), для местной санации гнойных очагов и серозных полостей (брюшины, плевры), для блокирования феномена бактериальной кишечной транслокации (при ин- тестинальном использовании препарата).
Согласно В.М. Бахир (1994), основным принципиальным моментом
синтеза электрохимически активированных растворов является разделение катода и анода полупроницаемой мембраной (диафрагмой), в силу чего в межэлектродной среде на границе «диафрагма-раствор» создается феномен
неоднородного распределения поверхностного натяжения с возникновением пространственно-временных диссипативных структур электрохимического реактора (эффекты Бенара-Релея и Марангони). В результате создания межэ- лектродной среды процессы мегафазного электро- и массопереноса ускоря- ются, позволяя реализовывать важные условия электрохимической актива- ции раствора при минимальных затратах энергии и времени. Получаемые
при этом среды отличаются малой концентрацией действующих агентов и не содержат чужеродных организму химических элементов. Все это придает им сходство с исходным веществом (чаще всего - физиологическим раство- ром NaCl), что делает их применение безопасным для людей и окружающей среды. В то же время, они являются мощными регуляторами окислительно- восстановительных биокаталитических процессов в живом организме. В ре- зультате электролиза солевых растворов образуются: анолит, содержащий следующие активные элементы – СlO2, HClO, ClO-, ClO*, Cl*, HO2, HO2*, O2,
HO2*, O3, O2*, 3O2, 1O2, O*, H3O+, Cl*, H*, Н2О2, Cl2O, ClO2, HCl, Cl2O7, S2O82-, C3O62-, HClO, H2SO4, HSO3Cl; и католит, включающий HO-, H3O2-
, O2*, HO2*, H2O2-, H2, HO, H2-, NaOH, KOH, Ca(OH)2, Mg(OH)2. В результате преобразования в аппаратах электрохимической активации (ЭДО-3М, ЭДО- 4, СТЭЛ и др.) происходит смешивание компонентов анолита и католита с получением так называемого раствора «щелочного анолита», самым главным действующим началом которого является гипохлорит натрия (NaClO). Гипо- хлорит натрия - это соединение с небольшой молекулярной массой и малы- ми структурными размерами, что обеспечивает его свободное проникнове- ние через биологические мембраны. Освобождая «активный кислород», со- держащийся в его молекуле, гипохлорит натрия окисляет имеющиеся в тка-
118

&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
нях и крови токсины и балластные вещества. Окисленные соединения хоро- шо растворяются в воде и значительно легче, чем исходные вещества, выво- дятся из организма. Окисление ксенобиотиков гипохлоритом приводит к об- разованию конечных продуктов, аналогичных получаемым с участием ци- тохрома Р-450, т.е. эти реакции напоминают механизм, с помощью которого печень человека обезвреживает ядовитые соединения гидрофобной приро- ды. С применением гипохлорита натрия запускается механизм оксигеназного пути окисления, т.е. реакция прямого присоединения кислорода к органиче- ским веществам. Самое главное преимущество использования гипохлорита натрия как переносчика «активного кислорода» заключается в обходе эффек- та «белковой защиты» токсических метаболитов. Гипохлорит натрия образу-
ется в организме человека в макрофагах во время фагоцитоза при адгезии и обездвиживании микробных клеток. Это говорит о физиологичности этого вещества и патогенетической целесообразности его применения при гнойно- воспалительных процессах микробной этиологии. Изучение антимикробных
свойств гипохлорита натрия показало высокую его активность в отношении многих микроорганизмов, обусловленную воздействием препарата на мик- робную стенку. Доказано, что он оказывает бактерицидное действие как на штаммы, чувствительные к антибактериальным препаратам, так и на штаммы с хромосомной и R-плазмидной устойчивостью ко многим антибиоти- кам (Лопаткин Н.А. и др., 1989;Горчаков В.Д. и др., 1989; Петросян Э.А., 1988, 1989, 1994). Обработанные гипохлоритом натрия микроорганизмы ста- новятся на 16-24% более восприимчивыми к действию ряда антибиотиков (аминогликозидов, полимиксина и др.). Механизм этого действия кроется в
изменении под влиянием гипохлорита натрия проницаемости микробной стенки для ионов калия и белково-липидного взаимодействия (Петросян Э.А., 1988, 1989, 1993) В соответствии с Рекомендациями ВНИИ профилак- тической токсикологии и дезинфекции Российской Федерации, электроак- тивированный раствор нейтрального анолита (при уменьшенной концентра- ции действующих веществ в 160 раз), оказывает в 3-4 раза более выраженное антимикробное действие по сравнению с таким эффективным дезинфектан- том, как «Сайдекс» [щелочной глутаровый альдегид] (Бахир В.М., 1994). Яв-
ляясь озонсодержащим раствором и обладая слабым фибринолитическим действием, гипохлорит натрия хорошо санирует гнойный очаг, уменьшает степень тканевой гипоксии, улучшает микроциркуляцию и стимулирует ме- стный.
При проведении антибактериальной терапии хирургического сепсиса учитываются характер и тяжесть органной дисфункции. При органной не-
достаточности по двум и более системам (прогнозируемая летальность 30% и более, наличие септического шока или индекс по шкале АРАСНЕ-II более 15 баллов, по шкале SAPS более 12 баллов или по шкале SOFA более 5 баллов)
предпочтение следует отдавать препаратам широкого спектра действия с наибольшей антимикробной активностью в отношении потенциально воз-
119

&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
можных патогенов и низким токсикоиндуцирующим потенциалом. В этом плане наиболее всего таким требованиям соответствуют карбапенемы и гли- копептиды. Добавление аминогликозидов в схемы антибактериальной тера-
пии в таких ситуациях должно быть строго обосновано и аргументировано (особенно в случаях почечной недостаточности). При таком назначении до- зировка препарата должна быть индивидуальной, скоррегированной по кли- ренсу креатинина. При наличии коагулопатии или дисфункции печени следу- ет воздержаться от использования цефаперазона и антисинегнойных пени- циллинов из-за риска развития геморрагического синдрома.
Особое значение при проведении антибактериальной терапии сепсиса имеют пути и способы введения препаратов антимикробного действия:
vвнутриартериальный (внутриаортальный, в нижнюю чревную ар- терию, периферические артерии конечностей);
vпутём направленного подведения антибиотиков в гнойно- воспалительный очаг (раневой антибактериальный диализ, короткие ново- каиновые блокады с антибиотиками, лекарственный тканевой электрофорез, экстракорпоральное депонирование антибиотиков в клетках крови с после- дующей их реинфузией больному сепсисом);
vэндолимфатическое введение препаратов – непрямым (лимфо- тропным) способом и прямым методом (через дренированный паховый лим- фоузел или лимфатический проток); преимуществами такого введения явля- ются: минимальная инактивация препарата, эффект депонирования антибио- тиков с уменьшением дозы, уменьшение эндотоксемии и вероятности реак- ций аллергического типа);
vпутём комбинации антибактериальной терапии с фотомодифика- цией крови (внутрисосудистым лазерным и ультрафиолетовым облучением крови), воздействием ультразвуком на иммунокомпетентные зоны и органы, гипербарической оксигенацией.
Беталактамные антибиотики, имеющие зависимую от времени дейст- вия бактерицидность, целесообразно вводить внутривенно (внутриартери- ально) с помощью дозирующих устройств (инфузоматов), позволяющих под- держивать необходимую постоянную концентрацию, в 4-5 раз превышаю- щую их минимальную подавляющую концентрацию в отношении большин- ства возбудителей сепсиса. Эффект от их применения может быть оценен не ранее, чем через 48-72 часа.
Длительность антимикробной терапии без изменения комбинации ан- тибиотиков (или монотерапии) не должна превышать 7-10 дней, поскольку при более коротком курсе может быть не достигнут положительный бакте- рицидный эффект, приводя к рецидиву болезни и селекции устойчивых штаммов микроорганизмов. Вместе с тем, она должна решить задачу регрес- са воспалительного процесса в первичном очаге, купирования ССВО, восста- новления функциональной полноценности повреждённых органов и систем.
При более длительных курсах может наступить развитие суперинфекции
120

&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
(кандидозной или бактериальной), что потребует использования дополни- тельных препаратов для её коррекции (дифлюкана, амфотеррицина), либо приведёт к ослаблению антиинфекционной защиты организма.
После получения данных бактериограммы начинается этап целена-
правленной (этиотропной) антибактериальной терапии. При этом осуще-
ствляется переход на препараты узконаправленного действия, менее токсич- ные и менее дорогостоящие. При положительной клинической динамике и
отсутствии данных об этиологии сепсиса ранее назначенная эмпирическая терапия может быть продолжена до полного излечения больного. Не целесо- образно менять при этом первичную терапию, если очаг инфекции локализо- ван в брюшной полости, эндокарде, костно-суставной системе, ЦНС, при на- личии бактериемии или при сохраняющемся критическом состоянии пациен- та. В случае отрицательной динамике заболевания и отсутствии данных об этиологии сепсиса, решение о смене программы антибактериальной терапии необходимо принимать не ранее 48-72 часов после адекватной хирургиче- ской санации очага инфекции и начала антимикробного лечения.
Оценка клинического эффекта от проводимой антибактериальной те- рапии проводится с учётом характера обратного развития клинических при-
знаков сепсиса и исчезновения патогенной микрофлоры из крови и других биологических сред организма. Выделяют ранние, поздние и оконча-
тельные критерии, указывающие на положительную динамику развития болезни (её инволюцию) либо излеченность сепсиса:
v Ранние (48-72 часа): положительная динамика со стороны клинической картины, стабилизация состояния, уменьшение признаков эндо- генной интоксикации; отсутствие бактериемии с отрицательными результа- тами бактериологического исследования крови; улучшение местного статуса со стороны раны (гнойного очага).
vПоздние (10-14 сутки): стойкая положительная клиническая
динамика; отсутствие рецидивов заболевания; постоянно отрицательные ре- зультаты бактериологического исследования через 3-4 дня после отмены препаратов антимикробного действия; тенденция к заживлению первичного септического очага.
vОкончательные (6-12 недель после окончания лече-
ния): отсутствие рецидива болезни или вторичных гнойных (септикопиеми- ческих) очагов при неоднократных целенаправленных исследованиях; стаби- лизация показателей гомеостаза и антиинфекционной защиты.
Причины неудач при проведении антибактериальной терапии
сепсиса могут быть разделены на следующие группы:
1). Микробиологические (различия условий in vitro и целостного ор- ганизма);
121

&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
2). Фармакологические (низкая концентрация препарата в очаге из-за увеличения объёма распределения и снижения его биодоступности, межме- дикаментозная инактивация);
3). Связанные с особенностями инфекционно-воспалительного очага (депо гноя, нерадикальная хирургическая санация, конкременты, некротиче- ские ткани, инородные тела);
4). Прогрессирование генерализованного медиаторного воспаления, органо-системной недостаточности (Руднов В.А., 2000).
7.2.2. ИММУНОКОРРЕКЦИЯ ПРИ СЕПСИСЕ
Это лечебное направление является важным патогенетическим зве- ном в коррекции тяжёлых изменений гомеостаза при сепсисе. Группа меро-
приятий включает рациональное использование лекарственных препаратов иммунотропного действия, а также способов немедикаментозного воздейст-
вия на организм больного с целью повышения функциональной активности органов и систем иммуногенеза и естественной резистентности.
Проведение иммунокорригирующей терапии при хирургическом сеп- сисе должно строиться, исходя из следующих принципов:
1.Назначение иммуномодуляторов должно проводиться только после радикального устранения источника сепсиса и главных источников эндогенной интоксикации.
2.Иммунокорригирующие средства не должны противопостав- ляться основному лечению, так как они являются его составной частью.
3.Назначение антибиотиков и других антибактериальных веществ должно сочетаться с одновременным использованием иммуномодуляторов, за счёт чего потенцируется эффект антимикробного воздействия.
4.Иммунотропная терапия должна строиться исключительно на выявленных иммунологических нарушениях и стадии септического процесса.
5.При отсутствии клинико-иммунологических критериев, свиде- тельствующих об эффективности проводимой иммунотропной терапии, должна быть пересмотрена программа использования иммуномодуляторов (с отменой, заменой препаратов, их комбинаций или доз).
6.Чем более выражен вторичный иммунодефицит при хирургиче- ском сепсисе, тем более рационально должна быть составлена программа иммунотерапии.
7.Комбинированное использование иммуномодуляторов должно предусматривать изменения в их иммунотропности в сторону потенцирова- ния иммунологических эффектов.
122

& Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
8.Подбор схем и лечебных доз иммунокорректоров должен учиты- вать, при прочих условиях, возраст больного, характер сопутствующей пато- логии и циркадность вариаций (зависимость активности препарата от вре- мени суток).
9.Необходимо использовать сочетанное применение иммуномоду-
ляторов с немедикаментозными способами воздействия на органы и системы антимикробной резистентности (ультразвуком, лазеротерапией, ультрафио- летовым и лазерным облучением крови, иглорефлексотерапией и др.), повы- шающими эффективность иммунотропной терапии.
10.При использовании иммуномодуляторов, наряду с парентераль- ными способами назначения, необходимо применять эндолимфатический путь введения (прямой и непрямой); подведение препаратов непосредственно
всептический очаг, что обеспечивает высокую и длительную концентрацию препаратов в указанной зоне, прямой их контакт с иммуноцитами при сни- жении общей лечебной дозы (Буянов В.М., Алексеев А.А., 1990).
11.При лечении тяжёлых форм сепсиса в комплекс мероприятий це- лесообразно включать экстра- и интракорпоральные методы иммуности- муляции [экстракорпоральную иммунофармакотерапию, ксеносорбцию, эн- теросорбцию, нейроакупунктурную иммуностимуляцию, клеточно-опосре-
дованный транспорт иммуностимуляторов совместно с антибиотиками в очаг воспаления и др.].
12.Иммунологический контроль эффективности проводимого лече- ния должен выполняться до операции, в течение первых 2-3 суток после неё и через каждые 6-8 суток до стабилизации показателей, что позволяет про- гнозировать течение заболевания и результативность иммунокоррекции.
Для проведения иммунокоррекции у больных сепсисом могут быть использованы как специфические защитные факторы 9относительно кон- кретного возбудителя заболевания), так и неспецифические средства (за счёт стимуляции фагоцитоза, факторов клеточного иммунитета и процесса анти- телообразования). При этом все средства, используемые для иммунокоррек- ции, можно разделить на препараты, вызывающие выработку собственных антител и клеточных факторов в ответ на их введение (т.н. «активная имму- низация»), и препараты пассивной иммунизации, содержащие уже готовые защитные факторы. Поскольку для развития специфического адаптивного ответа требуется определённое время (3-4 суток и более), то широкого при-
менения препараты специфической активной иммунотерапии в лечении острого периода сепсиса не получили.
Среди средств пассивной специфической иммунотерапии наи-
большее значение имеют препараты гипериммунной плазмы или иммуногло- булина. Их использование зависит от преобладающего микроорганизма в бактериальной ассоциации, выделенной из септического очага или крови. При этом могут применяться антистафилококковая, антипротейная, антиси- негнойная, антиэшерихиозная плазмы, которые содержат спектр антител раз-
123

&  Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
ных классов против конкретных инфекционных агентов, а также компоненты комплемента и ферментные системы.
Период полураспада введенных антител при этом составляет 2 не- дели. Оптимальный курс – 3-5 иммунотрансфузий по 250-500 мл гиперим- мунной плазмы или 3-7 мл иммуноглобулина ежедневно. Использование лю- бой гипериммунной плазмы (по принципу доступности) малоэффективно –
по своему лечебному действию оно не отличается от переливания обычной нативной плазмы.
Ксредствам пассивной неспецифической иммунотерапии относят инфузии свежеприготовленной донорской плазмы, альбумина, протеина, аминокровина, сывороточных препаратов (иммуноглобулина, интраглобина, веноглобина, пентаглобина, сандоглобина, цитотекта), лейкоцитарного кон- центрата и др.
Ксредствам активной неспецифической иммунотерапии отно-
сятся:
1. Активаторы естественной иммунорезистентности и моноци- тарно-макрофагальной системы:
1.1.микробного происхождения (пирогенал, продигиозан, полибио- лин, нуклеинат натрия, гликопин или ликопид, ромуртид, пицибанил, кре- стин, лентинин, а также препараты эубиотического действия – бификол, ко- либактерин, нормофлор, солкоуровак, флонидин-БС, бифидумбактерин, бак- тисубтил и др.);
1.2.производные дрожжей (сальмозан, ридостин, зимозан и др.);
1.3.бактериофаги (бактериофаг стрептококковый, бактериофаг эше- рихиозный жидкий, бактериофаг клебсиелёзный поливалентный очищенный, бактериофаг коли-протейный жидкий, бактериофаг протейный жидкий и др.);
1.4.препараты крови и тканевые производные (альбумин, протеин, аминокровин, гидролизин (Л-103), гидролизат казеина, аминопептид, препа- рат АСД, солкосерил, актовегин, церебролизин, фибриносол и др.);
1.5.анатоксины (стафилококковый жидкий анатоксин, анатоксин си- негнойной палочки);
1.6.сыворотки и производные иммуноглобулинов (иммуноглобулин, иммуноглобулин человеческий, интраглобин, веноглобулин, пентаглобин, сандоглобулин, цитотект, иммуноглобулин стафилококковый, комплексный иммуноглобулиновый препарат, нативная и антистафилококковая плазма, поливалентная жидкая противогангренозная сыворотка и др.);
1.7.адаптогены (алоэ, ФИБС, торфот, эсберитокс, апилак, сапарал, иммунал, растительные настойки женьшеня, элеутерококка, аралии манжур- ской, китайского лимонника, бисед, ромазулон и др.);
1.8.препараты аминокислот (глутаминовая кислота, метионин, цис- теин, вицеин, оротат калия, аминолон, гамалон, гипофенат и др.);
124

& Хирургический сепсис. Учебное пособие
Хирургический сепсис. Учебное пособие
1.9.витамины (С, Е, А, В1, В2, В6, В12) и микроэлементы (медь, селен, цинк), а также препараты комплексного действия;
1.10.гепатопротекторы (ЛИВ-52, эссенциале, сирепар, легалон и др.);
1.11.производные пурина и пиримидина (метилурацил, пентоксил, поли-АИ, полудан и др.);
1.12.производные диазепинов (фенозепам, диазепам и др.).
2.Активаторы преимущественно Т-клеточного звена иммуни-
тета:
2.1. препараты тимуса (пептидные экстракты, синтетические произ- водные):
∙1-го поколения (тималин, тактивин, тим-увакол);
∙2-го поколения (тимоген, α-тимозин, тимоптин, тимостимулин, тимомодулин, вилон);
∙3-го поколения (тимунокс, тимопентин-ТР-5);
∙4-го поколения (имунофан, бестим);
2.2.соединения имидазола (левамизол или декарис, диуцифон и др.);
2.3.нейропептиды (эпиталамин, гемалин, соматостатин или сандоста-
тин и др.);
2.4.препараты, производные различных групп (ретиноиды, ноотро- пил или пирацетам, циннаризин, натрия лобензерит, димексид, гепарин и др.);
3.Активаторы естественной иммунорезистентности и адаптивного иммунного ответа (антителозависимой формы и клеточной цитотоксичности)
3.1.препараты цитокинов:
3.1.1.Рекомбинатные интерфероны (α-реаферон, альфаферон, ре- альдирон, виферон, роферон, β-интрон, берофор, бетаферон, фрон, гамма- ферон, лейкинферон) и их индукторы (низкомолекулярные - циклоферон, амиксин; полимерные – полудан; производные госсипола – кагоцел, сав- рац, рагосин; производные РНК – ларифан, ридостин и др.);
3.1.2.Рекомбинантные колониестимулирующие факторы (ГМ-КСФ
–лейкомакс, молграстим; Г-КСФ – нейкоген, ленограстим и др.);
3.1.3.Рекомбинатные интерлейкины (ИЛ-1 – беталейкин или ре- комбинантный интерлейкин-1-человека; ИЛ-2 – ронколейкин или пролей-
кин, ИЛ-2 «Cetus»);
3.1.4.Препараты, повышающие внутриклеточное содержание цГМФ, цАМФ (холиномиметики, ионосодержащие полиэлектролиты, макроэргические препараты – АТФ, фосфаден и др.);
4.Ингибиторы цитокиногенеза, синтеза эйкозаноидов, кининов, системы комплемента и других реакций
4.1.ингибиторы синтеза эйкозаноидов, простагландинов, эндотели- нов, кининов:
125
