
Ч 2
.pdfразвивается редко. Встречаются железодефицитные анемии, развивающиеся вследствие кровотечений в закрытые полости при отсутствии последующей реутилизации железа (гемосидероз лёгких, эктопический эндометриоз, гломусные опухоли). В некоторых случаях кровопотери различной локализации, являющиеся причиной железодефицитной анемии, связаны с гематологическими заболеваниями (коагулопатиями, тромбоцитопениями и тромбоцитопатиями), а также с поражением сосудов при васкулитах, коллагенозах, болезни Рандю–Вебера–Ослера, гематомах. Дефицит железа алиментарного происхождения может развиться у детей и взрослых при недостаточном его содержании в пищевом рационе, что наблюдается при хроническом недоедании и голодании, ограничении питания с лечебной целью, однообразном питании (потребление пищи, содержащей преимущественно жиры и углеводы). У детей может наблюдаться недостаточное поступление железа из организма матери как следствие железодефицитной анемии во время беременности, преждевременных родов, при многоплодности и недоношенности, преждевременной перевязке пуповины до прекращения пульсации. К нарушению всасывания железа могут приводить воспалительные, рубцовые или атрофические процессы в тонкой кишке и её резекция.
Клиника железодефицитных состояний зависит от степени дефицита железа и скорости его возникновения и включает признаки анемии и тканевого дефицита железа (сидеропении). Явления тканевого дефицита железа отсутствуют лишь при некоторых железодефицитных анемиях, обусловленных нарушением утилизации железа, когда депо переполнены железом. Железодефицитная анемия в своём течении проходит два периода: 1) период скрытого де - фицита железа; 2) период явной анемии, вызванной дефицитом железа.
Впериод скрытого дефицита железа появляются многие субъективные жалобы и клинические признаки, характерные для железодефицитных анемий, только менее выраженные. Пациенты отмечают общую слабость, недомогание, снижение работоспособности. Уже в этот период могут наблюдаться извращение вкуса, сухость и пощипывание языка, нарушение глотания с ощущением инородного тела в горле (синдром Пламмера–Винсона), сердцебиение, одышка. У пациентов обнаруживаются «малые симптомы дефицита железа»: атрофия сосочков языка, хейлит (заеды), сухость кожи и волос, ломкость ногтей, жжение и зуд вульвы. Все эти признаки нарушения трофики эпителиальных тканей связаны с их сидеропенией и гипоксией.
Впериод явной анемии отмечаются общая слабость, быстрая утомляемость, затруднение в сосредоточении внимания, сонливость, головная боль после переутомления, головокружение, обмороки (при тяжёлой анемии). Эти жалобы, как правило, зависят не от степени малокровия, а от продолжительности заболевания и возраста пациентов. Железодефицитная анемия характеризуется изменениями кожи, ногтей и волос. Кожа, обычно бледная, иногда
слёгким зеленоватым оттенком (хлороз) или с легко возникающим румянцем на щеках, становится сухой, дряблой, шелушится, на ней появляются трещины.
101
Волосы теряют блеск, сереют, истончаются, легко ломаются, редеют и рано седеют. Ногти становятся тонкими, матовыми, уплощаются, легко расслаиваются и ломаются, появляется их исчерченность. При выраженных изменениях ногти приобретают вогнутую, ложкообразную форму (койлонихия). Атрофические изменения наблюдаются в слизистых оболочках пищеварительного канала, органов дыхания, половых органов. У большинства пациентов с железодефицитной анемией снижается аппетит, развивается потребность в кислой, острой или солёной пище. В более тяжёлых случаях наблюдаются извращения обоняния, вкуса (pica chlorotica) – употребление в пищу мела, извёстки, сырых круп, погофагия (влечение к употреблению льда). В 25 % случаев отмечаются глоссит и изменения полости рта. У пациентов снижаются вкусовые ощущения, появляется покалывание, жжение и чувство распирания в языке (особенно в его кончике). Выявляются атрофические изменения слизистой языка, трещины на кончике и по краям, в более тяжёлых случаях – участки покраснения неправильной формы («географический язык») и афтозные изменения. Атрофический процесс также захватывает слизистую оболочку губ
иполости рта. Появляются трещины губ и заеды в углах рта (хейлоз), изменения зубной эмали. Характерен сидром сидеропенической дисфагии (синдром Пламмера–Винсона), проявляющийся затруднением при глотании, чувством першения и ощущением наличия инородного тела в глотке, что вынуждает некоторых пациентов принимать только жидкую пищу. Наблюдаются признаки изменения функции желудка – отрыжка, ощущение тяжести в животе после еды, тошнота (связаны с атрофическим гастритом и ахилией). У пациентов с железодефицитной анемией отмечаются одышка, сердцебиение, боль в груди, отёки. Определяются расширение границ сердечной тупости влево, анемический систолический шум на верхушке сердца и лёгочной артерии, «шум волчка» на яремной вене, тахикардия и гипотензия. На ЭКГ обнаруживаются изменения фазы реполяризации. У лиц пожилого возраста тяжёлое течение железодефицитной анемии может вызвать сердечно-сосудистую недостаточность. Иногда отмечается лихорадка (температура обычно не превышает 37,5 °С и исчезает после лечения железом).
При постановке диагноза железодефицитной анемии решающее значение имеют данные лабораторных исследований крови, костного мозга и обмена железа. В крови отмечаются признаки гипохромной микроцитарной анемии, обнаруживается снижение концентрации гемоглобина. Количество эритроцитов вначале может быть нормальным, но при значительном дефиците железа оно также уменьшается (но в меньшей степени, чем уровень гемоглобина). Отмечаются низкий цветовой показатель (0,5–0,7) и снижение средней концентрации гемоглобина в эритроцитах. Уменьшаются размер эритроцитов (микроциты) и их насыщенность гемоглобином (гипохромия). В мазках крови преобладают небольшие гипохромные эритроциты, аннулоциты (эритроциты без гемоглобина в центре, в виде колец), эритроциты неодинакового размера
иформы (анизоцитоз, пойкилоцитоз) (рис. 3.5). При тяжёлых анемиях могут
102
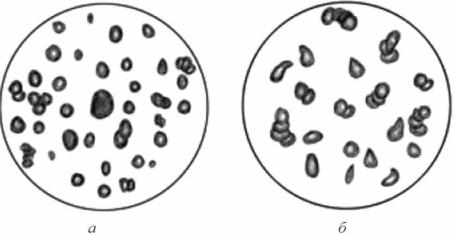
Рис. 3.5. Анизоцитоз (а) и пойкилоцитоз (б) при железодефицитной анемии Приведено по: Г. Е. Ройтберг, А. В. Струтынский (1999)
появляться отдельные эритробласты. Количество ретикулоцитов не изменено. Только при анемии, развившейся на фоне кровопотери, количество ретикулоцитов непосредственно после кровотечения повышается, что является важным признаком кровотечения. Осмотическая резистентность эритроцитов мало изменена или несколько повышена. Количество лейкоцитов имеет нерезко выраженную тенденцию к снижению. Лейкоцитарная формула мало изменена. Уровень тромбоцитов остается нормальным, а при кровотечениях несколько повышен. В костном мозге при железодефицитной анемии можно обнаружить эритробластическую реакцию с задержкой созревания и гемоглобинизации эритробластов на уровне полихроматофильного нормоцита. Костный мозг в большинстве случаев гиперпластичен. Увеличивается соотношение клеток белого и красного ряда, количество последних преобладает. Эритробласты составляют 40–60 % от всех клеток (во многих из них появляются дегенеративные изменения в виде вакуолизации цитоплазмы, пикноза ядер, отсутствует цитоплазма – «голые ядра»). Лейкопоэз характеризуется некоторым увеличением количества незрелых гранулоцитов.
В12-фолиеводефицитные анемии развиваются вследствие недостаточного поступления витамина В12 в организм с продуктами питания и нарушения его усвоения. Данные анемии протекают тяжело, трудно поддаются лечению (именно в связи с этим указанные формы мегалобластических дефицитных анемий называют пернициозными анемиями, типичный пример – анемия Ад- дисона–Бирмера). Дефицит в организме витамина В12 любого происхождения обусловливает нарушение синтеза нуклеиновых кислот в эритрокариоцитах, а также обмена жирных кислот в них и клетках других тканей. Витамин В12 имеет две коферментные формы: метилкобаламин и 5-дезоксиаденозилкоба- ламин.
103

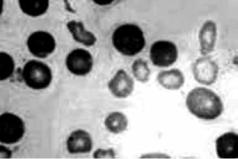
При развитии данного вида анемии в костном мозге обнаруживают мегалобласты диаметром более 15 мкм, а также мегалокариоциты. Мегалобласты характеризуются десинхронизацией созревания ядра и цитоплазмы. Быстрое образование гемоглобина (уже в мегалобластах) сочетается с замедленной дифференциацией ядра. Указанные изменения в клетках эритрона сочетаются с нарушением дифференцировки и других клеток миелоидного ряда – мегакариобласты, миелоциты, метамиелоциты, палочко- и сегментоядерные лейкоциты также увеличены в размерах, а их ядра имеют более нежную, чем в норме, структуру хроматина. В периферической крови значительно снижено (иногда до (0,7–0,8)1012/л) число эритроцитов. Они большого размера – до 10–12 мкм, часто овальной формы, без центрального просветления. Как правило, встречаются мегалобласты. Во многих эритроцитах обнаруживаются остатки ядерного вещества (тельца Жолли) и нуклеолеммы (кольца Кебота) (рис. 3.6). Характерны анизоцитоз (преобладают макро- и мегалоциты), пойкилоцитоз, полихроматофилия, базофильная пунктация цитоплазмы эритроцитов. Последние избыточно насыщены гемоглобином. Цветовой показатель, как правило, составляет более 1,1–1,3. При этом общее содержание гемоглобина в крови существенно снижено в связи со значительным уменьшением числа эритроцитов. Количество ретикулоцитов обычно понижено, в редких случаях – нормальное. Наблюдаются лейкопения (за счёт нейтрофилов), сочетающаяся с наличием полисегментированных гигантских нейтрофилов, а также тромбоцитопения. В связи с повышенным гемолизом эритроцитов (в основном в костном мозге) развивается билирубинемия. В12-дефицитная анемия, как правило, сопровождается изменениями в желудочно-кишечном тракте в связи с нарушением деления (при этом выявляются признаки атипичного митоза) и созревания клеток (наличие мегалоцитов), особенно в слизистой оболочке. Наблюдаются глоссит, формирование «полированного» языка (в связи с атрофией его сосочков), стоматит, гастроэнтероколит (усугубляющий течение анемии в связи с нарушением всасывания витамина В12), неврологический синдром (развивающийся вследствие изменений в нейронах). Эти откло-
Рис. 3.6. Тельца Жолли (а) и кольца Кебота (б) при В12-фолиеводефицитной анемии Приведено по: Г. Е. Ройтберг, А. В. Струтынский (1999)
104
нения в основном являются следствием нарушения обмена высших жирных кислот. Последнее связано с тем, что другая метаболически активная форма витамина В12 – 5-дезоксиаденозилкобаламин (помимо метилкобаламина) регулирует синтез жирных кислот, катализируя образование янтарной кислоты из метилмалоновой. Дефицит 5-дезоксиаденозилкобаламина обусловливает нарушение образования миелина, оказывает прямое повреждающее действие на нейроны головного и спинного мозга (особенно задних и боковых его столбов), что проявляется психическими расстройствами (бредом, галлюцинациями), признаками фуникулярного миелоза (шаткой походкой, парестезиями, болевыми ощущениями, онемением конечностей и др.).
Фолиеводефицитные анемии. Фолиевая кислота – сложное соединение, состоящее из трёх компонентов – глутаминовой кислоты, парааминобензойной кислоты и птеридинового кольца. Соединения фолиевой кислоты (фолаты) содержатся в большом количестве в некоторых пищевых продуктах (печени, мясе, дрожжах, шпинате), однако при кулинарной обработке более половины из них разрушается. При дефиците поступления запасы фолиевой кислоты в организме исчерпываются в течение 3–4 мес. Всасывается фолиевая кислота в основном в верхнем отделе тонкой кишки. Метаболически активной (коферментной) формой фолиевой кислоты является тетрагидрофолиевая кислота. Последняя необходима для регуляции образования тимидинмонофосфата, входящего в структуру ДНК, синтеза глутаминовой кислоты, пиримидиновых и пуриновых оснований.
Факторами развития фолиеводефицитных анемий (так же как и витамин В12-дефицитных) являются недостаточное поступление фолиевой кислоты в организм с пищей, нарушение усвоения фолиевой кислоты в организме и доставки её клеткам гемопоэтической ткани. Недостаточность фолиевой кислоты обусловливает нарушение синтеза и структуры ДНК, учитывая, что эта кислота в своей метаболически активной форме (в виде тетрагидрофолиевой кислоты) необходима для синтеза тимидинмонофосфата, а также для включения в молекулу ДНК уридина и оротовой кислоты. Это сопровождается переходом с нормобластического на мегалобластический тип кроветворения.
Гемолитические анемии представляют собой обширную группу заболеваний, различающихся по этиологии, патогенезу, клинической картине, методам лечения. Основными их признаками являются повышенный распад эритроцитов и укорочение продолжительности их жизни. В физиологических условиях продолжительность жизни эритроцитов составляет 100–120 дней. «Стареющие» эритроциты подвергаются секвестрации в синусах селезёнки, а также в костном мозге. Формирующийся в результате физиологического распада эритроцитов пигмент (билирубин) циркулирует в крови в виде свободного (неконъюгированного) билирубина, который транспортируется в печёночную клетку, где при участии ферментов (глюкуронилтрансферазы) соединяется с глюкуроновой кислотой. Образовавшийся билирубин-глюкуронид (конъюгированный или связанный билирубин) проникает из печёночных кле-
105
ток в желчные ходы и выделяется вместе с желчью в кишечник. Продолжительность жизни эритроцитов при гемолитических анемиях укорачивается до 12–14 дней вследствие их усиленного разрушения. Патологический гемолиз может носить преимущественно внутрисосудистый характер. В ретикулогистиоцитарной системе (преимущественно в селезёнке) происходит внутриклеточный распад эритроцитов, который сопровождается повышением в сыворотке крови свободного билирубина, увеличением экскреции уробилина с мочой и калом, а кроме того, развивается склонность к образованию камней в желчном пузыре и протоках. При внутрисосудистом гемолизе гемоглобин поступает в повышенном количестве в плазму и выделяется с мочой в неизменённом виде или в виде гемосидерина, который может откладываться во внутренних органах (гемосидероз).
По течению гемолиз может быть острым или хроническим. Все гемолитические анемии делятся на две большие группы: наследственные и приобретённые.
Наследственные гемолитические анемии являются следствием различных генетических дефектов в эритроцитах, которые становятся функционально неполноценными и нестойкими (например, наследственный микросфероцитоз или синдром Минковского–Шоффара).
Приобретённые гемолитические анемии обусловлены воздействием различных факторов, способствующих разрушению эритроцитов (образование антител, гемолитические яды, механические воздействия и т. д.).
Клиническая картина всех анемий характеризуется наличием следующих основных синдромов (изолированно или в сочетании).
Анемический синдром. Бледность кожных покровов и слизистых, обед - нение капиллярного рисунка склер глаз; слабость, повышенная утомляемость и потливость; снижение и извращение аппетита; одышка и сердцебиение; головокружение, шум в ушах; обмороки; усиление тяжести хронической патологии (например, утяжеление приступов стенокардии при наличии ишемической болезни сердца). Ряд авторов в рамках данного симптомокомплекса выделяет отдельные синдромы: изменения окраски кожи и склер (чаще – бледность, реже – желтуха при гемолизе), астеновегетативный синдром (слабость, эмоциональная лабильность, снижение интеллектуальных способностей и т. п.), кардиальный синдром (боли в области сердца, тахикардия, систолический шум при аускультации и т. п.), синдром сосудистых нарушений (артериальная дистония, головные боли, обмороки и т. п.), синдром обменных нарушений (отставание в физическом и половом развитии, явления костномышечного дисморфизма и т. п.).
Синдром неэффективного эритропоэза (все тяжёлые формы анемий вне зависимости от причин, анемии при хронических заболеваниях, некоторые формы наследственных анемий, клональные анемии). Характеризуется состоянием, при котором активность костного мозга увеличена, но выход созревших эритроцитов в кровь снижен из-за повышенного разрушения в костном
106
мозге эритробластов. При длительном существовании данного синдрома возможно развитие костных деформаций вследствие расширения «плацдарма» кроветворения.
Синдром дизэритропоэза (тяжёлые формы любых анемий, мегалобластные анемии, талассемия, сидеробластные анемии). Проявляется нетяжёлым гемолизом, сопровождающим другие проявления анемии. Характеризуется морфологическим признаками нарушенного созревания эритроцитов в костном мозге с наличием косвенных указаний на существенный неэффективный эритропоэз (в крови определяются многоядерные эритробласты и эритробласты с дольчатыми ядрами, хроматиновыми мостиками, клетками в состоянии кариорексиса).
Синдром гемолиза (вследствие врождённых и приобретённых дефектов оболочки эритроцитов, деструкции клеток антителами, внутриклеточной деструкции, неиммунного повреждения и других причин). Проявляется желтушным окрашиванием кожи и склер глаз, наличием тёмной (бурой) мочи, увеличением печени и селезёнки. В гемограмме отмечается снижение гемоглобина и эритроцитов, увеличение СОЭ, ретикулоцитоз, повышение билирубина и лактатдегидрогеназы, реакция на стеркобилин в кале и уробилин в моче положительны. В миелограмме отмечается раздражение эритроидного ростка кроветворения.
Синдром сидеропении и состояние латентного дефицита железа. Про-
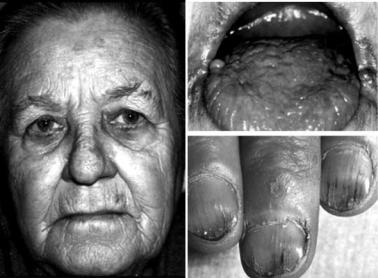
является дистрофией кожи и её придатков, извращением вкуса и обоняния, мышечной гипотонией (одним из проявлений которого может стать недержание мочи), мышечными болями, ухудшением памяти, снижением внимания и другими изменениями (рис. 3.7).
Рис. 3.7. Внешний вид лица, языка и пальцев пациентки с сидеропеническим синдромом Приведено по: http://www.primamedica.ru/present/Anemii/anemii1.ppt#34
107
Земного шара, обусловлены эпизодически возникшими мутациями. Поскольку гомозиготные особи погибают, не достигнув детородного возраста, отбор идёт в пользу гетерозигот.
Талассемия начинается в раннем |
|
детском возрасте и характеризуется |
|
триадой симптомов – прогрессирую- |
|
щей анемией с наличием эритробла- |
|
стов в периферической крови, увели- |
|
чением печени и селезёнки, повы- |
|
шенным гемолизом и желтухой (зем- |
|
листо-жёлтая окраска кожи, уробили- |
|
нурия), остеопорозом со своеобраз- |
|
ным изменением лица и увеличением |
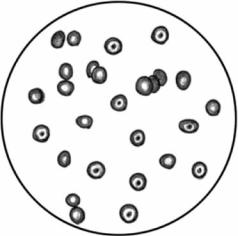
Рис. 3.9. Мишеневидные эритроциты при та- |
черепа (лицо пациента с анемией Ку- |
лассемии |
ли – башенный череп, увеличение |
Приведено по: Г. Е. Ройтберг, А. В. Струтын- |
верхней челюсти, монголоидный раз- |
ский (1999) |
рез глаз, выступание резцов и клыков |
|
с нарушением прикуса). Рентгенологически определяется симптомом «волосатого черепа», или «ёжика», так называемый игольчатый периостоз. В длинных трубчатых костях расширены костномозговые полости, кортикальный слой истончён, часто наблюдаются патологические переломы. Гепатомегалия является проявлением гемосидероза и заканчивается фиброзом, формированием цирроза печени. Фиброз поджелудочной железы осложняется развитием сахарного диабета. Может возникнуть калькулёзный холецистит. Развивающееся снижение концентрационной способности почек усугубляет гипоксическую дистрофию. Даже после лечения пациенты умирают в возрасте до 17 лет. Однако при хорошем диспансерном наблюдении и периодическом введении десферала (дефероксамина – комплексного препарата, способствующего снижению патологических отложений железа и алюминия в органах и тканях), срок их жизни может быть продлён.
Описана американским педиатром-гематологом Т. В. Cooley (1871–1845).
Анемия Фанкони (синоним – синдром Фанкони I). Наследственное за-
болевание человека с ломкой и рекомбинацией хромосом; одна из форм гипопластической анемии, которая сочетается с тромбоцитопенией, выражающейся в общем угнетении кроветворных функций костного мозга, обусловленном наличием хромосомных аберраций различного типа (как правило, обменов между негомологичными хромосомами) вследствие нарушения процессов репарации ДНК. Один из вероятных локусов (FA1) сцеплен с длинным плечом хромосомы 20 человека. Характеризуется гипоплазией костного мозга, панцитопенией, а также аномалиями развития кожи (гиперпигментация в 51 % случаев), костной системы (недоразвитие I пястной или лучевой кости в 40 % на-
109
блюдений) и/или внутренних органов (почек, селезёнки), умственным и половым недоразвитием. Нередко отмечаются множественные хромосомные нарушения. В типичных случаях развивается в возрасте 4–6 лет. Наследуется по аутосомно-рецессивному типу.
Описана в 1927 г. швейцарским педиатром G. Fanconi.
Анемия Эстрена–Дамешека. Наследственная гипопластическая анемия у детей с неэффективностью всех трёх ростков кроветворения в костном мозге. Отличается от анемии Фанкони отсутствием других аномалий развития.
Описана в 1951 г. американскими педиатрами S. Estren и W. Dameshek. Анемия Якша–Гайема. Алиментарная анемия, связанная с недостаточным поступлением веществ в организм (в первую очередь веществ, необходимых для синтеза гемоглобина). Встречается у детей в возрасте 6–18 мес. Характеризуется очень бледной кожей, значимым истощением, геморрагическими проявлениями. В крови отмечается рост цветного показателя, появляется значительное количество эритробластов и нормобластов. Выявляются сплено- и гепатомегалия. На рентгенограмме отмечаются утолщение костей свода черепа с расширением его губчатого вещества (диплоэ), а также остео-
пороз трубчатых костей.
Описана чешским врачом R. R. Jaksch (1855–1947) и французским врачом
G. Hayem (1841–1933).
Болезнь (анемия) Аддисона–Бирмера (синонимы – злокачественное малокровие, прогрессирующая пернициозная анемия). Эндогенный В12-ави-
таминоз. Одной из этиологических форм заболевания является наследственный фактор, связанный с генетически детерминированным недостатком витамин В12-связывающего фактора крови (белка транскобаламина-II: ген TCN2 локализован на длинном плече хромосомы 22), обусловливающего выработку гастромукопротеина. Тип наследования при этом не установлен.
Клинические признаки: бледность, субиктеричность, слабость, одышка, сердцебиение, боль в области сердца, головокружение, жжение в языке и пищеводе, периодический понос, иногда атаксия, отёчность лодыжек и стоп. Могут быть асцит и гидроторакс, систолический шум в сердце, стенокардия аноксемического характера, гунтеровский глоссит. При анализе желудочного сока определяют гистаминоустойчивую ахилию (вследствие атрофии фундальных желёз). Печень увеличена, мягкая. При значительном снижении количества эритроцитов может возникнуть лихорадка. Возможны спинальные параличи (псевдотабес). В крови – гиперхромная анемия, при обострении количество ретикулоцитов в крови уменьшается.
Впервые в 1849 г. эту разновидность дефицитных анемий описал англий-
ский врач Т. Addison (1793–1860), а затем в 1872 г. – немецкий врач А. Biermer (1827–1892), назвавший её «прогрессирующей пернициозной» (гибельной, злокачественной) анемией.
Болезнь Гайема–Видаля. Приобретённая аутоиммунная гемолитическая анемия, обусловленная образованием тепловых аутоантител.
110
