
- •3.10.3.7. Неврологические осложнения
- •3.10.3.8. Острая почечная недостаточность
- •3.10.4. Особенности ведения больных при различных оперативных вмешательствах
- •3.10.4.1. Операции по поводу аневризм восходящего, грудного и торакоабдоминалъного отделов аорты
- •3.10.4.2. Операции при коарктации аорты
- •3.10.4.3. Каротидная эндартерэктомия
- •3.10.4.4. Операции по поводу ишемической болезни сердца
- •3.10.4.5. Реконструктивные операции на почечных артериях
- •3.10.4.6. Операции на брюшном отделе аорты и аортобедренное шунтирование
- •3.10.4.7. Операции реваскуляризации артерий нижних конечностей
- •3.11. Диспансеризация больных с сосудистыми заболеваниями в условиях поликлиники
- •3.11.1. Физиотерапевтическое лечение
- •3.11.2. Хроническая венозная недостаточность нижних конечностей
- •3.11.3. Лимфедема
- •Глава 4
- •4.1. Транслюминальная баллонная ангиопластика
- •4.2.1. Имплантация кава-фильтров
- •4.2.2. Транскатетерная тромбоэмболэктомия
- •4.2.3. Лечение обструкций полых и других крупных вен
- •4.2.4. Баллонная ангиопластика и стентирование обструкций при артериовенозных фистулах у пациентов, находящихся на гемодиализе
- •Глава 5
- •5.1.1. Стабильная стенокардия напряжения
- •5.1.2. Нестабильная стенокардия
- •5.2. Аортокоронарное шунтирование
- •5.2.1. Техника аортокоронарного шунтирования с искусственным кровообращением
- •5.2.2. Техника маммарокоронарного шунтирования в условиях искусственного кровообращения
- •5.2.3. Операции прямой реваскуляризации миокарда на работающем сердце без искусственного кровообращения — малоинвазивная коронарная хирургия
- •5.2.4. Трансмиокардиалышя реваскуляризация миокарда
- •5.3. Синдром Марфана
- •5.3.1. Этиология (генетические предпосылки развития синдрома Марфана)
- •5.3.2. Патогенез и патоморфология
- •5.3.3. Диагностические критерии
- •Диагностические критерии синдрома Марфана
- •Диагностические критерии синдрома Марфана
- •Диагностический указатель
- •Костно-суставная система
- •Орган зрения
- •Сердечно-сосудистая система
- •Респираторная система
- •Кожа и наружные покровы
- •Твердая мозговая оболочка (dura mater)
- •Семейный/Генетический анамнез
4.2.1. Имплантация кава-фильтров
Внутрипросветная установка кава-фильтра в нижней полой вене была разработана Mobin-Uddin и соавт. в 1967 г. и применяется чтобы защитить легочно-сосудистое русло от эмболии из полых вен и их притоков. Продолжаются дискуссии относительно показаний для этого
вмешательства. Имплантация показана, если:
▲ при илиокавографии или при дуплексном сканировании в просвете нижней полой вены или в подвздошных венах обнаружены флотирующие тромбы;
▲ у больного с тромбозом нижней полой вены начало или продолже-
496
антикоагулянтная терапия не предупредила повторную эмболию;
в случае венозного тромболизи-са, так как у 20 % больных имеется опасность эмболии в течение первых трех суток лечения.
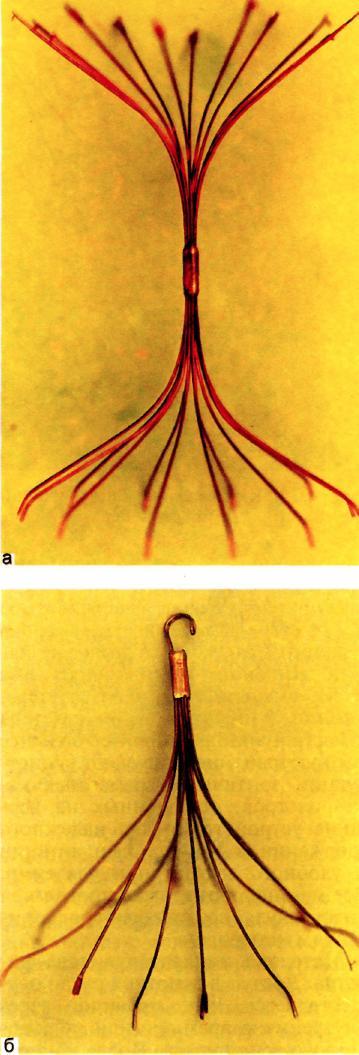
В настоящее время применяют 2 типа кава-фильтров — постоянные и временные. Постоянные фильтры имеют конструкцию, которая не позволяет удалить их из сосудистого русла. Эти конструкции выпускаются фирмами COOK, Cordis, Mansfild, КОМЕД. Постоянные ка-ва-фильтры просты в применении, надежно фиксируются к стенкам нижней полой вены, хорошо улавливают тромбоэмболы. Повторные эмболии при правильно установленных кава-фильтрах не описаны. Однако известно определенное количество осложнений, связанных с постояными кава-фильтрами. Наиболее тяжелым из них является поздний первичный тромбоз фильтра (не эмболия!), встречающийся в 15—50 % наблюдений (по данным разных авторов). К сожалению, это осложнение запрограммировано самой конструкцией фильтра. Длина любого постоянного фильтра 40—55 мм. Металлические лучи, или проволочное сплетение, выполняющие роль ловушки, значительно нарушают ламинарность кровотока в данном сегменте нижней полой вены. Это неминуемо приводит со временем к нарастанию тромботических масс на конструкции фильтра и окончательному тромбозу последнего (рис. 4.14).
Логичным решением этой проблемы явилась разработка временных кава-фильтров, которые могут быть удалены из сосудистого русла через 7—15 сут после завершения тромболизиса, удаления тромба из просвета нижней полой вены. Существует несколько конструкций временных кава-фильтров — фильтр-катетер — устройство, имп-
Рис. 4.14. Кава-фильтры.
а — постоянный; б — временный.
497
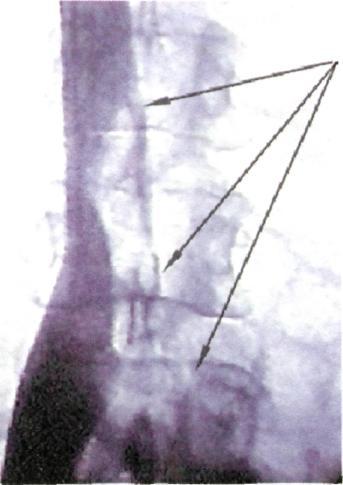
Рис. 4.15. Кавография. Флотирующий тромб в нижней полой вене.
лантируемое в просвет нижней полой вены через яремную или подключичную вену, и удерживаемое на катетере в течение всего срока терапии. Эти конструкции не нашли широкого применения из-за риска смещения фильтра-катетера, опасности инфицирования катетера и места пункции вены. Все большее распространение получают конструкции зонтичных временных ка-ва-фильтров, оснащенных на вершине устройствами для надежного удержания в момент имплантации и удобного захвата при удалении. Все манипуляции также проводятся эндоваскулярно, под флюороскопи-ческим контролем.
Методика имплантации кава-фи-льтра. Доступ в венозное русло осуществляется, как правило, через внутреннюю яремную или подключичную вену справа. После измерения давления в легочной артерии, ангиопульмонографии и илиокаво-графии (см. выше) диагностический катетер устанавливают в про-
498
екции устьев почечных вен и выполняют илиокавографию (рис. 4.15). Все манипуляции производят под флюороскопическим контролем. Катетеризируя и контрастируя поочередно каждую вену, уточняют их количество, уровень впадения в нижнюю полую вену, скелетото-пию. Это необходимо для правильной имплантации кава-фильтра, который должен быть распложен так, чтобы его лучи фиксировались к стенкам нижней полой вены тотчас ниже устьев почечных вен или тотчас ниже нижнего устья, а вершина фильтра находилась в потоке крови, оттекающей из почечных вен. Это позволяет защитить почечные вены от эмболии тромбами из нижних отделов нижней полой вены и предупреждает формирование тромбов на центральной части фильтра, так как эта часть постоянно омывается кровью.
Для достижения этого проводящую канюлю устанавливают в нижней полой вене дистальнее устьев почечных вен. Буж с проводником удаляют. В просвет открытого крана канюли устанавливают металлическую гильзу с заранее фиксированным к захвату катетера-толкателя кава-фильтром «Зонтик». В гильзу поступальным движением вводят катетер-толкатель, который с небольшим усилием проталкивает кава-фильтр внутрь проводящей канюли. Под рентгеновским контролем с помощью катетера-толкателя кава-фильтр устанавливают на уровне дистального торца проводящей канюли. В этом положении кава-фильтр удерживают катетером-толкателем неподвижно, а канюлю медленно подтягивают вверх так, чтобы контролировать первоначальное раскрытие более длинных центрирующих, а затем более коротких фиксирующих лучей. Последние оснащены фиксаторами и обеспечивают надежное удержание фильтра в просвете нижней полой вены. На заключительном этапе
имплантации нажатием на пружинную ручку катетера-толкателя освобождают кава-фильтр. Катетер-толкатель и доставляющую канюлю удаляют, выполняют контрольную кавографию (рис. 4.16). После имплантации кава-фильтра продолжают антикоагулянтную и антиагре-гантную терапию в течение 3—6 мес. Состояние нижней полой вены и ее притоков, состояние кава-фильтра и кровотока в нем контролируют периодическим ультразвуковым дуплексным сканированием [26].
Следует указать на осложнения, общие для временных и постоянных кава-фильтров. Эти осложнения включают миграцию и эмболию фильтра в легочные магистрали, перфорацию вены, структурную фрагментацию фильтра, повреждения мочеточников. К счастью, это довольно редкие осложнения, частота которых не превышает 0,5— 1 %. Более частым и также общим осложнением имплантации кава-фильтра является болевой корешковый синдром. Он развивается при имплантации неверно подобранного по диаметру фильтра, когда ножки последнего, слишком глубоко внедряясь в ткань стенки нижней полой вены, вызывают реактивное воспаление Окружающих тканей и нервных окончаний [28].
