
- •С.В. Іванов, п.С. Борсук, н.М. Манчук загальна хімічна технологія
- •Передмова
- •Теоретичні основи хімічної технології вступ
- •1. Основи хіміко-технологічних процесів
- •1.1 Хіміко-технологічний процес і його зміст
- •1.2. Класифікація хімічних реакцій, які покладені в основу промислових хіміко-технологічних процесів.
- •1.3. Технологічні критерії ефективності хіміко-технологічного процесу
- •2. Структура хімічного виробництва
- •3. Хіміко-технологічні системи
- •3.1. Поняття хіміко-технологічної системи (хтс)
- •3.2. Моделі хіміко-технологічних систем
- •3.3. Технологічні зв'язки в хтс
- •4. Поняття про синтез хіміко-
- •4.1. Texнологічні концепції створення хтс
- •4.2. Аналіз хтс
- •5. Матеріальні і теплові баланси хіміко-технологічних систем
- •5.1. Баланс співвідношень
- •5.1.2. Приклади розрахунку балансів
- •5.2 Основні поняття ексергетичного аналізу хтс
- •6. Термодинамічні розрахунки хіміко-технологічних процесів
- •6.1. Рівновага хімічних реакцій
- •6.2. Константа рівноваги й енергія Гіббса. Рівняння ізотерми Вант-Гоффа
- •6.3. Хімічна рівновага в гетерогенних реакціях
- •7. Вибір технологічних режимів проведення хтп
- •7.1. Способи зміщення рівноваги
- •7.2. Залежність константи рівноваги від температури
- •7.3. Розрахунок рівноваги за термодинамічними даними
- •8. Використання законів хімічної кінетики при виборі технологічного режиму.
- •8. 1. Швидкість гомогенних хімічних реакцій
- •8.2. Залежність швидкості хімічних реакцій від концентрації реагентів; кінетичні рівняння
- •8.3. Способи зміни швидкості простих і складних реакцій
- •9. Кінетика хіміко-технологічних процесів
- •9.1. Вплив різних чинників на швидкість хімічних процесів, які перебігають на мікрорівні
- •9.2. Кінетика хтп, що ґрунтується на оборотних хтп
- •9.3 Швидкість хтп, що ґрунтується на паралельних та послідовних гомогенних реакціях
- •9.3.2. Вплив технологічних параметрів на швидкість гомогенних процесів
- •9.3.3. Методи інтенсифікації гомогенних процесів
- •9.4. Кінетика гетерогенних некаталітичних процесів
- •9.4.2. Швидкість гетерогенних процесів
- •9.4.4. Визначення лімітуючої стадії гетерогенного процесу
- •9.4.5. Способи збільшення швидкості процесу
- •9.5 Типи реакторів для гетерогенних процесів
- •9.5.1 Реактори для проведення реакцій в системах г-т і р-т
- •9.5.2 Реактори для проведення реакцій в системах г—р і р—р
- •10. Каталітичні процеси.
- •10.2. Технологічні характеристики каталізаторів
- •10.3. Гомогенний і гетерогенний каталіз
- •10.4. Властивості твердих каталізаторів і їхнє виготовлення
- •10.5. Апаратурне оформлення каталітичних процесів
- •10.5.3 Апарати зі зваженим (киплячим, псевдокиплячим) шаром каталізатора
- •11. Хімічні реактори
- •11.1 Класифікація реакторів
- •11.2. Вимоги до хімічних реакторів
- •11.3. Структура математичної моделі хімічного реактора
- •10.4. Реактор ідеального змішування періодичний
- •11.5 Реактори безперервної дії
- •11.5.1 Реактор ідеального витіснення (рів)
- •11.5.2. Реактор ідеального змішування безперервний (різ–б)
- •11.5.3 Загальне проектне рівняння реактора
- •11.6 Каскад реакторів ідеального змішання (к-різ)
- •11.7 Графічний метод розрахунку к – різ
- •11.8. Вплив кінетики на вибір типу реактора
- •11.9. Селективність, вихід, ступінь перетворення
- •11.9.2. Залежність селективності від ступеня перетворення
- •11.10. Хімічні реактори з неідеальною структурою потоків
- •11.11. Моделі ректорів з неідеальною структурою потоку
- •11.12. Ячеїста модель.
11.5.2. Реактор ідеального змішування безперервний (різ–б)
РІЗ-Б являє собою апарат(рис.11.4), у який безперервно надходять реагенти і безперервно виводяться продукти реакції, при цьому відбувається безперервне перемішування реагентів за допомогою мішалки. Вхідна суміш, що надходить у такий реактор, миттєво змішується з реакційною масою, що вже знаходиться у реакторі, де концентрація вхідного реагенту нижче, ніж у суміші, що надходить.
Для виведення характеристичного рівняння складемо рівняння матеріального балансу. Число молів вхідної речовини А, що надходить з потоком, V0СА,0dτ, де V0 – об'ємна швидкість вихідних

Рис.11.4 РІЗ-Б
реагентів, СА,0 – концентрація реагенту А в потоці, τ−час перебування реагентів в реакторі. Число молів, що відводиться з реактора, − VкСАdτ, де Vк – об'ємна швидкість, СА– концентрація реагенту А в потоці, що відводиться з реактора. Число молів реагенту А, що витрачається в результаті хімічного перетворення: Vr dτ, , де Vr – робочий об'єм реактора, −швидкість реакції.
Накопичення реагенту А дорівнює зміні його кількості в реакційному просторі за період часу dτ. Вміст речовини в даний момент складає VrCA, а його зміна – d(VrCA).
Об'єднаємо всі частини балансу:
![]() ,
,
![]()
11.5.3 Загальне проектне рівняння реактора
повного змішування
Крім періодів зупинення і пуску, реактор безперервної дії працює в сталому режимі. Проектне рівняння в такому випадку приводиться до вигляду:
![]()
Якщо
реакція відбувається в рідкій фазі, то
зміна об'єму мала і V0
= Vк
= V. Тоді
![]() ,
,
CА,0
– СА
=
![]() А
,
А
,
де
![]() і
τ- умовний час перебування реагентів в
реакторі.
і
τ- умовний час перебування реагентів в
реакторі.
Після введення ступеня перетворення:
CА,0 - СА,0 (1 – ХА) =τ А,
CА,0 XА = τ А ,
![]() ,
,
![]() .
.
Для простої необоротної реакції n – го порядку:
![]() ,
,
 ,
,
![]() ,
,
 .
.
Для реакцій нульового порядку:
![]() .
.
Для
реакцій першого порядку:
![]() .
.
Якщо реакція перебігає зі зміною об’єму:
![]() ,
,
 .
.
Для реакція нульового порядку:
![]() ,
,
для реакції першого порядоку:
![]() .
.
11.6 Каскад реакторів ідеального змішання (к-різ)
В одиничному реакторі ідеального змішання (РІЗ – Б) внаслідок того, що концентрація реагентів миттєво знижується до кінцевої величини, швидкість реакції при великому ступені перетворення невелика, тому для досягнення високого ступеня перетворення потрібний реактор великого об’єму. Тому дуже часто застосовують ряд послідовно розташованих РІЗ – Б, тобто К – РІЗ.
Каскад являє собою декілька послідовно з'єднаних проточних реакторів (секцій) ідеального змішування.
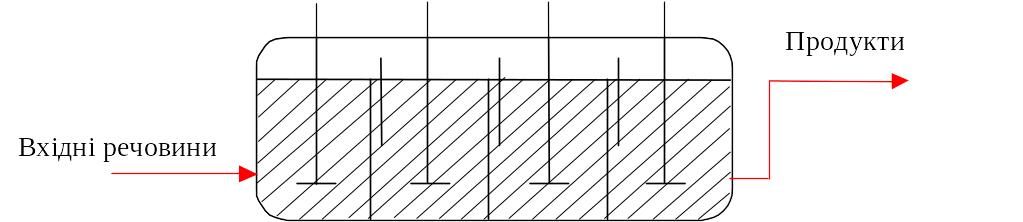

Рис. 11.6 Принципові схеми каскадів реакторів змішання
Концентрація вихідного реагенту в такій системі знижується до кінцевого значення не відразу, а поступово від реактора до реактора.
Математична модель каскаду реакторів ідеального змішання, що працює в ізотермічному режимі, являє собою систему рівнянь матеріального балансу за якимось учасником реакції, що включає, щонайменше, j рівнянь за числом секцій каскаду.

Рис. 11.8. Зміна концентрації вихідного реагенту за ступенями каскаду
.
У розрахунку каскаду для кожного ступеня використовується проектне рівняння проточного безперервного діючого реактора ідеального змішування.
в
Пронумеруємо послідовно ступені каскаду від 1 до m. Позначимо через СJ,0 концентрацію вихідного реагенту J у суміші, концентрацію реагенту, що відводиться з цього ступеню СJ,i у наступну ступінь. Якщо припустити, що в трубопровідах, що з'єднують апарати каскаду, хімічне перетворення мінімальне, то можна вважати концентрацію реагенту J у суміші на виході з j – го реактора рівною концентрації цієї речовини в суміші на вході в (j + 1) реактор.
Використовуючи рівняння:
![]() ,
,
![]() .
.
Послідовно для розрахунку окремих ступенів каскаду одержуємо:
![]()
![]()
![]()
![]() ,
,
де τ1, τ2...…τi – середній час перебування реагентів в окремих ступенях каскаду.
Таким
чином утворилася система
![]() рівнянь з
рівнянь з
![]() невідомими СJ,1,
CJ,2,
…CJ,n
, оскільки швидкості реакції
J,1=f(CJ),
J,i=f(CJ,i)
також є функціями цих концентрацій.
Концентрації в окремих реакторах
обчислимо шляхом послідовного рішення
проектних рівнянь, починаючи з першого
ступеня каскаду.
невідомими СJ,1,
CJ,2,
…CJ,n
, оскільки швидкості реакції
J,1=f(CJ),
J,i=f(CJ,i)
також є функціями цих концентрацій.
Концентрації в окремих реакторах
обчислимо шляхом послідовного рішення
проектних рівнянь, починаючи з першого
ступеня каскаду.
У деяких простих випадках, наприклад для реакції першого порядку, можна установити безпосередню залежність між концентраціями на вході в каскад і виході з нього:
![]() ,
,
де Vр – реакційний об’єм; ϊ – кількість секцій; τ – середній час перебування реакційної суміші у ϊ -й секції; СJ,i – концентрація компонента на виході з ϊ – ої секції.
Розрахунок каскаду звичайно зводиться до визначення числа секцій заданого об’єму, необхідного для досягнення заданого ступеня перетворення, чи до визначення складу реакційної суміші на виході з ϊ – ої секції каскаду. Вихідні параметри для першої секції є вхідними для другої і т. ін.
Розглянемо визначення концентрації реагенту А на виході з каскаду, що має ϊ секцій рівного об’єму V1=V2… Vj при проведенні реакції першого порядку:
![]()
Одержуємо систему рівнянь
![]()
![]()
![]()
![]() .
.
З першого рівняння знаходимо концентрацію реагенту J, у першому ступені каскаду:
![]() (11.18)
(11.18)
Концентрація реагенту J у другому реакторі:
![]() і т.ін. (11.19)
і т.ін. (11.19)
Визначимо з рівнянь (11.18) і (11.19) СJ, :
![]() .
.
Таким же чином визначаємо наступні концентрації:
![]()
![]() , (11.20)
, (11.20)
Якщо при перебіганні реакції обєм реакційної суміші не змінюється, то СА=СА,0(1-ХА), звідки:
![]()
Якщо константи швидкості і час перебування однакові, то рівняння (11.18) можна записати:
![]()
 (11.21)
(11.21)
Рівняння (11.21) дозволяє не тільки визначити концентрацію на виході з будь-якого реактору каскаду, але і знайти число послідовно з'єднаних реакторів, якщо задані зміни концентрації чи ступінь перетворення:
![]() .
.
Аналітичне
рішення рівнянь для визначення
концентрацій реакцій більш високого
порядку дуже складне. Тому в цьому
випадку кращий менш точний, але більш
простий графічний метод. Так як рівняння
матеріального балансу однотипні для
всіх секцій, можна скласти алгоритм
рішення цих рівнянь для
![]() –ої
секції і послідовно застосовувати його
раз.
–ої
секції і послідовно застосовувати його
раз.
У кожному реакторі концентрація вихідного реагенту в об’ємі стала і дорівнює його концентрації на виході з реактора. Зміна концентрації вихідної речовини відбувається так само, як і в РІЗ – Б, тобто стрибком при вході реакційної суміші в реактор. Однак концентрація СА в каскаді вище, ніж в одиничному реакторі, і при збільшенні числа наближається до значення концентрації в РІВ.
Завданням розрахунку К – РІЗ є визначення числа ступенів (числа реакторів) , необхідних для досягнення заданого ступеня перетворення. Для визначення числа ступенів каскаду використовують графічний чи алгебраїчний метод.
