
- •С.В. Іванов, п.С. Борсук, н.М. Манчук загальна хімічна технологія
- •Передмова
- •Теоретичні основи хімічної технології вступ
- •1. Основи хіміко-технологічних процесів
- •1.1 Хіміко-технологічний процес і його зміст
- •1.2. Класифікація хімічних реакцій, які покладені в основу промислових хіміко-технологічних процесів.
- •1.3. Технологічні критерії ефективності хіміко-технологічного процесу
- •2. Структура хімічного виробництва
- •3. Хіміко-технологічні системи
- •3.1. Поняття хіміко-технологічної системи (хтс)
- •3.2. Моделі хіміко-технологічних систем
- •3.3. Технологічні зв'язки в хтс
- •4. Поняття про синтез хіміко-
- •4.1. Texнологічні концепції створення хтс
- •4.2. Аналіз хтс
- •5. Матеріальні і теплові баланси хіміко-технологічних систем
- •5.1. Баланс співвідношень
- •5.1.2. Приклади розрахунку балансів
- •5.2 Основні поняття ексергетичного аналізу хтс
- •6. Термодинамічні розрахунки хіміко-технологічних процесів
- •6.1. Рівновага хімічних реакцій
- •6.2. Константа рівноваги й енергія Гіббса. Рівняння ізотерми Вант-Гоффа
- •6.3. Хімічна рівновага в гетерогенних реакціях
- •7. Вибір технологічних режимів проведення хтп
- •7.1. Способи зміщення рівноваги
- •7.2. Залежність константи рівноваги від температури
- •7.3. Розрахунок рівноваги за термодинамічними даними
- •8. Використання законів хімічної кінетики при виборі технологічного режиму.
- •8. 1. Швидкість гомогенних хімічних реакцій
- •8.2. Залежність швидкості хімічних реакцій від концентрації реагентів; кінетичні рівняння
- •8.3. Способи зміни швидкості простих і складних реакцій
- •9. Кінетика хіміко-технологічних процесів
- •9.1. Вплив різних чинників на швидкість хімічних процесів, які перебігають на мікрорівні
- •9.2. Кінетика хтп, що ґрунтується на оборотних хтп
- •9.3 Швидкість хтп, що ґрунтується на паралельних та послідовних гомогенних реакціях
- •9.3.2. Вплив технологічних параметрів на швидкість гомогенних процесів
- •9.3.3. Методи інтенсифікації гомогенних процесів
- •9.4. Кінетика гетерогенних некаталітичних процесів
- •9.4.2. Швидкість гетерогенних процесів
- •9.4.4. Визначення лімітуючої стадії гетерогенного процесу
- •9.4.5. Способи збільшення швидкості процесу
- •9.5 Типи реакторів для гетерогенних процесів
- •9.5.1 Реактори для проведення реакцій в системах г-т і р-т
- •9.5.2 Реактори для проведення реакцій в системах г—р і р—р
- •10. Каталітичні процеси.
- •10.2. Технологічні характеристики каталізаторів
- •10.3. Гомогенний і гетерогенний каталіз
- •10.4. Властивості твердих каталізаторів і їхнє виготовлення
- •10.5. Апаратурне оформлення каталітичних процесів
- •10.5.3 Апарати зі зваженим (киплячим, псевдокиплячим) шаром каталізатора
- •11. Хімічні реактори
- •11.1 Класифікація реакторів
- •11.2. Вимоги до хімічних реакторів
- •11.3. Структура математичної моделі хімічного реактора
- •10.4. Реактор ідеального змішування періодичний
- •11.5 Реактори безперервної дії
- •11.5.1 Реактор ідеального витіснення (рів)
- •11.5.2. Реактор ідеального змішування безперервний (різ–б)
- •11.5.3 Загальне проектне рівняння реактора
- •11.6 Каскад реакторів ідеального змішання (к-різ)
- •11.7 Графічний метод розрахунку к – різ
- •11.8. Вплив кінетики на вибір типу реактора
- •11.9. Селективність, вихід, ступінь перетворення
- •11.9.2. Залежність селективності від ступеня перетворення
- •11.10. Хімічні реактори з неідеальною структурою потоків
- •11.11. Моделі ректорів з неідеальною структурою потоку
- •11.12. Ячеїста модель.
9.2. Кінетика хтп, що ґрунтується на оборотних хтп
Для простої оборотної ендотермічної реакції типу:
А R -Q характер залежності υ=f(T) також може бути встановлений на основі рівняння (9.5). За підвищення температури швидкість реакції зростає за рахунок збільшення як члена е-Е/RT так і значення КС. При збільшенні ХА (за інших рівних умов) загальна швидкість реакції знижується (рис. 9.3).
Встановимо залежність XА=f(T) для тих же реакцій. Ця залежність є дуже важливою, оскільки ступінь перетворення характеризує відносну кількість переробленого вихідного реагенту.
Для простої необоротної реакції A R±Q залежність XА=f(T) виражається S-зворотною кривою (рис. 9.4). Така залежність пояснюється тим, що за низької температури швидкість процесу мала, тому за проміжок часу в реакцію вступає лише незначна частина вихідного реагенту А, а тому невеликий підйом кривої ХА=f(T) (рис. 9.4). У міру підвищення температури швидкість реакції збільшується експоненціально відповідно до рівняння (9.3), що призводить до різкого підйому кривої. Але зі збільшенням ХА концентрація вихідного реагенту зменшується і відповідно знижується зростання швидкості реакції, тому функціональна залежність ХА=ƒ(Т) асимптотично наближається до одиниці.
Для простої оборотної екзотермічної реакції типу: А R+Q залежність XА=f(T) за деякий час спочатку зростає, досягає максимального значення, а потім знижується, оскільки процес обмежений рівноважним ступенем перетворення X* (рис. 9.5). Крива, відповідна 2> 1, розташується вище кривої 1, крива 3>τ2 розташується ще вище і т. ін. (рис. 9. 5). Крива АВ, що сполучає максимуми, відображає залежність X=f(T) і являється лінією оптимальної температури (ЛОТ). Її іноді називають лінією оптимальної температурної послідовності. Остання показує, що для простої оборотної екзотермічної реакції існує не якась оптимальна температура, а температурна послідовність, що забезпечує максимальну швидкість процесу.
Р
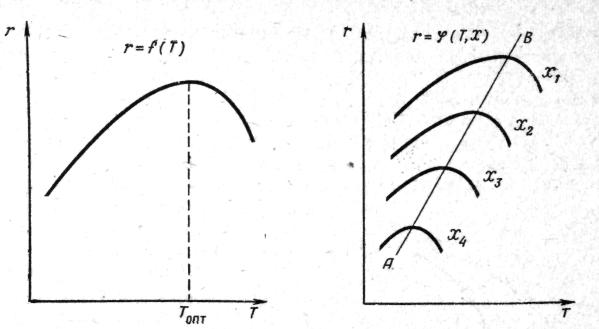
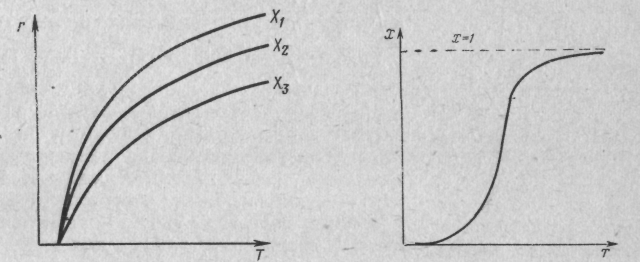
Рис. 9.3 Залежність швидкості υ простої оборотної ендотермічної реакції А R-Q від температури Т (Х1>Х2>Х3).
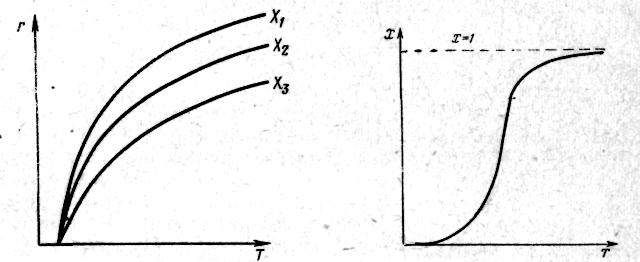
Рис.
9.4 Залежність ступеня перетворення Х
від температури Т для простої необоротної
реакції А
R![]() Q
Q
Щоб створити такі оптимальні умови, процес слід спочатку вести при високій температурі, коли швидкість υА велика і із-за низького значення ХА не може бути досягнута висока Х*А Для збільшення ХА необхідно знизити температуру { підвищувати Х*А) і вести процес по ЛОТ.
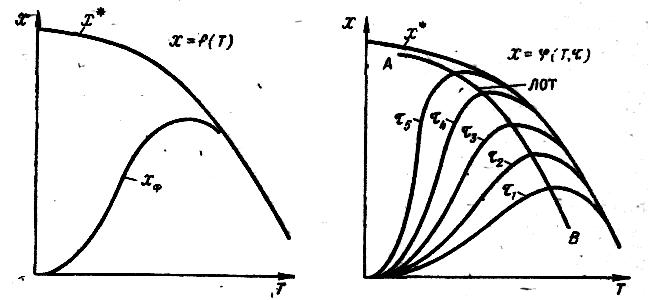
Рис. 9.5 Залежність ступеня перетворення X від температури Т для простої оборотної екзотермічної реакції А : R+Q ( 1< 2< 3< 4<τ5)
Для простої оборотної ендотермічної реакції типу:
А
R—Q
питання
про вплив температури вирішується
однозначно і з погляду термодинаміки
(тобто з погляду умов рівноваги), і з
погляду кінетики процесу, тому
що
при підвищенні температури збільшується
і рівноважний X*
і фактичний ступінь перетворення ХФ
(рис. 9. 6.). Проте і в цьому випадку існує
оптимальна температура ТОПТ.,
при якій досягаються найбільш вигідні
умови для проведення технологічного
процесу, оскільки при підвищенні
температури зменшується нахил кривої,
тобто похідна dXА/dT![]() 0.
Тому невигідно сильно збільшувати
температуру, оскільки значення ХА
мало зростає. Проте в деяких випадках
підвищення температури чинить
і негативний вплив на хіміко-технологічний
процес.
0.
Тому невигідно сильно збільшувати
температуру, оскільки значення ХА
мало зростає. Проте в деяких випадках
підвищення температури чинить
і негативний вплив на хіміко-технологічний
процес.
Щоб скласти загальне уявлення про залежність X=f(T) для всіх типів розглянутих реакцій, проаналізуємо рис. 9. 7.
З рис. 9.7 видно, що за малих значень X характер кривих X=f(Т) у всіх випадках однаковий, при підвищенні температури величина X різко зростає. Така залежність пояснюється тим, що з підвищенням температури збільшується швидкість реакції, а вплив термодинамічних чинників (тобто зворотної реакції) незначний. З рис. 9.7 також слідує, що для досягнення ступеня перетворення Х1 температура повинна бути тим вище, чим менше тривалість процесу.
З підвищенням X вплив термодинамічних чинників збільшується. Ступінь цього впливу залежить від типу реакції, що і визначає характер кривих, наведених на рис. 9. 7. Для необоротних реакцій криві залежності ХА = f(Т) асимптотично наближаються до одиниці. Для оборотних реакцій криві залежності ХА= f (Т) обмежуються кривою рівноважного ступеня перетворення X*, яка, як ми вже знаємо, для екзотермічної реакції з підвищенням температури зменшується, а для ендотермічних реакцій зростає.
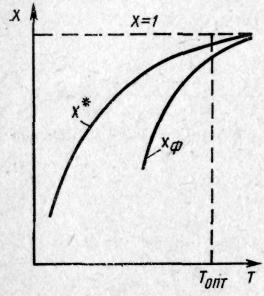
Рис. 9.6. Залежність ступеня перетворення X від температури Т для простої зворотної ендотермічної реакції А R—Q(X*, ХФ — ступінь перетворення відповідно рівноважна і фактична)
З приведених даних виходить, що температура чинить не лише позитивний, але і негативний вплив на показники ХТП. Негативний вплив температури полягає в наступному:
1. збільшення втрат цільового продукту внаслідок його випаровування і утворення побічних продуктів;
2. зниження міцності і хімічної стійкості матеріалів;
3. зменшення величини X* у екзотермічних реакціях;
4. можливе зниження селективності складних реакцій.
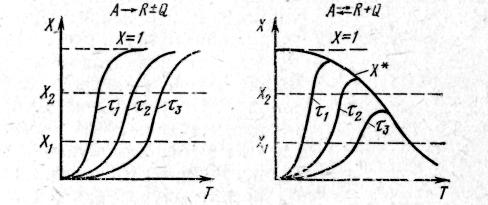
Рис. 9. 7. Залежність ступеня перетворення Х від температури для різної тривалості процесу ( 1> 2> 3)
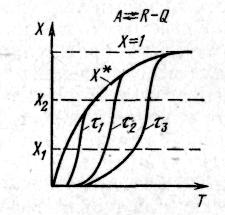
Рис. 9.8. Залежність ступеня перетворення X від температури Т за різної тривалості процесу ( 1> 2> 3)
