
- •Общая и неорганическая химия
- •Часть 2 свойства элементов и их соединений
- •Содержание
- •2.1 Введение.………………………….…..……………….………….30
- •3.1 Введение…………………………………………………………...41
- •4.1 Введение …………………………………………………………..47
- •5.1 Введение…………….….…………….………….….….….………56
- •6.1 Введение.…..…………………….………………………….……..70
- •7.1 Введение…………………………………………………………..77
- •9.1 Введение.…...…..………………………………….…..…….……83
- •Периодическая система химических элементов. Строение атомов и молекул
- •1.1 Введение
- •1.2 Постулаты теории Бора
- •1.3 Квантовомеханическое описание состояния электрона в атоме
- •1.3.1 Элементарные представления о квантовой механике
- •1.3.2 Главное квантовое число
- •1.3.3 Орбитальное квантовое число
- •1.3.4 Магнитное квантовое число
- •1.3.5 Атомные орбитали
- •1.3.6 Спиновое квантовое число
- •1.3.7 Принцип Паули
- •1.4 Периодическая система химических элементов
- •1.4.1 Элементы первого периода (h, He)
- •1 .4.2 Элементы второго периода (Li – Ne)
- •1.4.3 Элементы III периода (Na – Ar)
- •1.4.4 Элементы IV периода (k – Kr)
- •1.4.5 Элементы V, VI и VII периодов
- •1.5 Химическая связь и строение молекул
- •1.5.1 Механизмы образования ковалентной связи
- •1.5.2 Направленность ковалентной связи
- •1.5.3 Гибридизация атомных орбиталей
- •1.5.4 Металлическая связь
- •Комплексные соединения
- •2.1 Введение
- •2.2 Основные положения координационной теории
- •2.3 Природа химической связи в комплексных соединениях
- •2.4 Классификация комплексов
- •2.4.2 Классификация по типу лигандов
- •2.5 Номенклатура комплексных соединений
- •2.6 Диссоциация комплексных соединений в растворах
- •2.7 Образование и разрушение комплексов
- •2.8 Геометрия комплексных ионов
- •2.9 Изомерия комплексных соединений
- •Галогены
- •3.1 Введение
- •3.2 Физические свойства галогенов
- •3.3 Химические свойства галогенов
- •3.4 Получение галогенов
- •3.5 Водородные соединения галогенов
- •3.6 Получение галогеноводородов
- •3.7 Кислородсодержащие соединения галогенов
- •3.8 Применение галогенов
- •4.1 Введение
- •4.2 Кислород
- •4.3 Сера
- •4.3.1 Свойства серы – простого вещества
- •4.3.2 Сероводород, сульфиды, полисульфиды
- •4.3.3 Диоксид серы. Сернистая кислота
- •4.3.4 Триоксид серы. Серная кислота
- •4.3.5 Олеум. Дисерная кислота
- •4.3.6 Мононадсерная и пероксодисерная кислоты
- •4.3.7 Тиосерная кислота и тиосульфаты
- •4.4 Селен. Теллур
- •4.5 Сравнение свойств водородных соединений p-элементов VI группы
- •5.1 Введение
- •5.2 Азот
- •5.2.1 Свойства азота – простого вещества
- •5.2.2 Аммиак и соли аммония. Гидразин. Гидроксиламин
- •5.2.3 Оксиды азота
- •5.2.4 Азотистая кислота и её соли
- •5.2.5 Азотная кислота и её соли
- •5.2.6 «Царская водка»
- •5.3 Фосфор
- •5.3.1 Свойства фосфора – простого вещества
- •5.3.4 Соединение фосфора с водородом
- •5.3.5 Галогениды фосфора
- •5.4 Мышьяк
- •5.5 Сурьма
- •5.6 Висмут
- •6.1 Введение
- •6.2 Углерод и его соединения
- •6.2.1 Свойства углерода – простого вещества
- •6.2.2 Оксид углерода (IV). Угольная кислота и её соли
- •6.2.3 Оксид углерода (II)
- •6.2.4 Карбиды
- •6.2.5 Соединения углерода с азотом
- •6.3 Кремний
- •6.4 Германий. Олово. Свинец
- •7.1 Введение
- •7.3 Алюминий
- •7.4 Индий. Галлий. Таллий
- •Обзор химических свойств соединений d-элементов
- •9.1 Введение
- •9.4 Хром
- •9.5 Марганец
- •9.6 Элементы триады железа
- •9.6.1 Железо
- •9.6.2 Кобальт
- •9.6.3 Никель
- •Литература
- •Часть 2. Свойства элементов и их соединений
2.8 Геометрия комплексных ионов
Если внутреннюю сферу комплексного соединения образуют одинаковые лиганды, то они располагаются симметрично вокруг центрального атома.
Комплексы, образованные центральными ионами, координационное число которых равно 2 имеют линейное строение (рисунок 2.2 а). Такая геометрия соответствует sp-гибридному состоянию атомных орбиталей комплексообразователя.
При координационном числе комплексообразователя равном 4 комплексный ион может иметь либо квадратное строение (состояние sp2d- гибридизации орбиталей комплексообразователя), либо тетраэдрическое (sp3-гибридизация атомных орбиталей центрального иона) (рисунок 2.2 б, в).
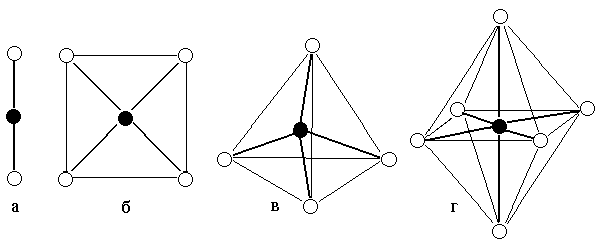
Рисунок 2.2 – Геометрия комплексных
ионов: а)
координационное число комплексообразователя
равно 2; б)
и в) координационное число
комплексообразователя равно 4; г)
координационное число комплексообразователя
равно 6
Шестикоординированные комплексы имеют геометрию октаэдра (рисунок 2.2 г). Октаэдрическое строение комплекса соответствует sp3d2-гибридному состоянию атомных орбиталей комплексообразователя.
2.9 Изомерия комплексных соединений
Изомерией называют явление, которое заключается в существовании соединений с одинаковым составом, но различным строением, вследствие чего эти соединения (изомеры) обладают различными свойствами.
Одним из важнейших видов изомерии комплексных соединений является геометрическая изомерия. К этому виду изомерии относится цис-транс изомерия, которая возможна в случае комплексов квадратного или октаэдрического строения, если внутренняя сфера этих комплексов образована лигандами разного типа. Цис-транс изомерия обусловлена различным пространственным расположением лигандов относительно центрального атома. Если одинаковые лиганды располагаются в соседних вершинах квадрата или октаэдра, то такой изомер называется цис-изомером, если в противоположных – транс-изомером (рисунок 2.3).
К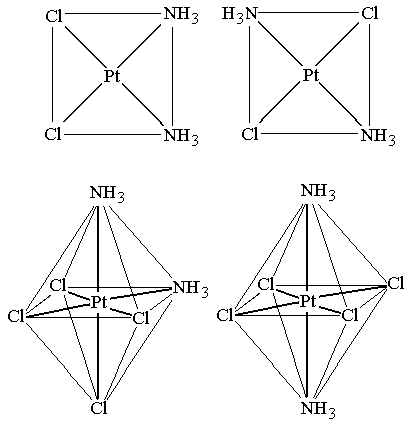 геометрической изомерии следует отнести
и оптическую изомерию.
геометрической изомерии следует отнести
и оптическую изомерию.
Э
транс-изомер
цис-изомер
цис-изомер
транс-изомер
Кроме геометрической
и
Рисунок
2.3 –
Цис-транс изомерия
Гидратная изомерия имеет место при переходе молекул воды из внутренней сферы во внешнюю:
[Cr(H2O)6]Cl3 ⇆ [Cr(H2O)5Cl]Cl2H2O ⇆ [Cr(H2O)4Cl2]Cl2H2O .
Ионизационная изомерия связана с различным распределением ионов между внутренней и внешней сферами:
[Co(NH3)5Br]SO4 и [Co(NH3)5SO4]Br; [Pt(NH3)4Cl2]Br2 и [Pt(NH3)4Br2]Cl2 .
Координационная изомерия связана с переходом лигандов от одного комплексообразователя к другому: [Co(NH3)6][Cr(CN)6] ⇆ [Cr(NH3)6][Co(CN)6] .
Л Е К Ц И Я 3
