
- •Методичні вказівки
- •Загальні вказівки до проведення та оформлення студентами лабораторних робіт
- •Лабораторна робота № 1 Методи та засоби вимірювання термодинамічних параметрів. Похибки вимірювань та їх оцінка
- •Формули визначення похибки
- •Засоби вимірювання температури
- •Засоби вимірювання тиску
- •Засоби вимірювання швидкостей і витрат рідин
- •Похибки вимірювань і їх оцінка
- •Лабораторна робота № 2 дослідження процесу, що протікає при постійному об'ємі
- •Опис лабораторної установки
- •Підготовка лабораторної установки до роботи
- •Робота з установкою
- •Теоретичні відомості та обробка результатів досліджень
- •Лабораторна робота №3 Дослідження процесу, що протікає при постійній температурі
- •Робота з установкою
- •Етапи роботи
- •Теоретичні відомості і обробка результатів досліджень
- •Лабораторна робота №4 Дослідження процесу, який протікає при постійному тиску
- •Теоретичні відомості і обробка результатів досліджень
- •Лабораторна робота № 5 Експериментальна перевірка закону стану ідеального газу
- •Короткі теоретичні відомості
- •Порядок проведення експериментальних досліджень
- •Обробка результатів досліджень
- •Лабораторна робота № 6 Визначення теплоти пароутворення
- •Основні поняття і визначення
- •Опис лабораторної установки
- •Порядок проведення роботи
- •Лабораторна робота № 7 Визначення залежності температури насичення від тиску
- •Опис лабораторної установки
- •Порядок проведення роботи
- •Лабораторна робота № 8 Визначення показників адіабати
- •Методика експериментального визначення показника адіабати
- •Порядок проведення досліду
- •Лабораторна робота № 9 визначення ізобарної теплоємності повітря
- •Теоретичні основи
- •Опис дослідної установки
- •Методика проведення і обробка результатів вимірювань
- •Лабораторна робота №10 визначення питомої теплоємності речовини
- •Коротка теорія
- •Опис установки
- •Порядок виконання і етапу роботи
- •Облік теплоти, яка йде на нагрівання калориметра
- •Облік теплових витрат
- •Порядок виконання II етану роботи
- •Порядок роботи
- •Результати вимірювань і розрахунків шуканих величин
- •Коротка теорія
- •Опис установки
- •Порядок виконання роботи
- •(Титульний лист)
- •Лабораторна робота №...
- •II. Коротка теорія
- •III. Таблиця вимірів і розрахунку величин, що визначаються
- •Параметри стану
- •Співвідношення між різними одиницями вимірювання тиску
- •Співвідношення між одиницями роботи і тепла
- •Література:
Лабораторна робота №10 визначення питомої теплоємності речовини
Мета роботи: Визначення питомої теплоємності невідомої рідини і надбання навичок з проведення науково-дослідних робіт.
Приладдя: два електрокалориметра, вольтметр, амперметр, термометри, дослідні рідини, терези, мензурка.
Робота виконується у два етапи: 1 етап теоретичний, а другий практичний. За результатами другого етапу згідно порядку виконання роботи обчислюються всі значення шуканих величин.
Коротка теорія
При розрахунку теплової апаратури, найбільш важливим моментом є визначення кількості теплоти, яка приймає участь у процесі. Точне її визначення забезпечує правильну оцінку роботи апарата з економічної точки зору, що є особливо цінним при порівняльних експериментах.
Надання тілу теплоти у якому-небудь процесі викликає зміну його стану і в загальному випадку супроводжується зміною температури. Відношення теплоти dq, яке отримане одиницею кількості речовини при нескінченно малій зміні його стану, до зміни температури dt називається питомою теплоємністю тіла у даному процесі:
![]() .
(10.1.)
.
(10.1.)
Величина q у рівнянні (10.1.) залежить не тільки від інтервалу температур, але і від виду процесу підвода теплоти, який характеризується деяким постійним параметром х, яким може бути об'єм тіла V, тиск Р та інші.
Загальна кількість теплоти, яка одержана у даному процесі, визначається виразом:
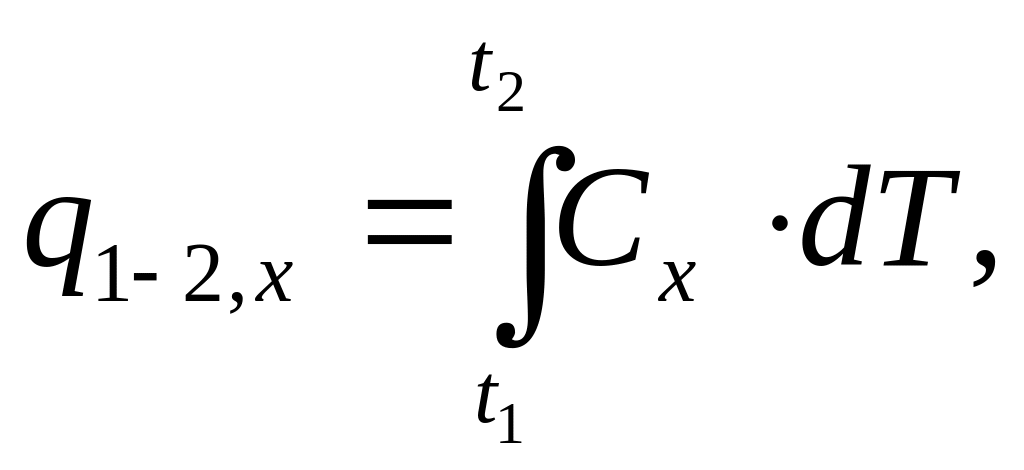 (10.2.)
(10.2.)
де інтеграл береться від початкового стану 1 до заданого кінцевого стану 2. Так як кількість теплоти q1-2,х залежить від характеру процесу, то і теплоємність системи Сх також залежить від умов протікання процесу.
Одна і таж система в залежності від характеру процесу має різні теплоємності, чисельна величина яких може змінюватись в межах від -∞ до +∞.
Теплоємність речовин залежить від температури і характеризує теплоаккумуляційні властивості речовини.
Одним з методів визначення теплоємності є калориметричний. Калориметрія отримала значний розвиток і дозволяє в теперішній час робити вимірювання кількостей теплоти від 10-6 калорій до тисяч калорій; тривалість теплових процесів від долей секунди до декількох днів, а температурний діапазон охоплює від 0,1 до 4000 К.
Основними частинами калориметра є калориметрична система і калориметрична оболонка.
Опис установки
Велике поширення отримали калориметри змінної температури з ізотермічною оболонкою. їм властива проста будова, надійність у використанні і широта експериментальних можливостей.
На рис. 10.1 зображено схему непроточного калориметра. Калориметр з ізотермічною оболонкою складається з наступних основних частин: калориметричної посудини, виготовленої з високотеплопровідного металу 1, оболонки З, ізоляційних розкладок. Для забезпечення постійної температури калориметричної системи оболонку разом з калориметричною посудиною поміщають у термостат. Повітряний прошарок між калориметричною посудиною і оболонкою утрудняє теплообмін калориметричної системи з оточуючим середовищем. Для зменшення теплообміну підвищують властивості відбиття поверхні оболонки. Завдяки цьому збільшується точність вимірювання кількості теплоти.
Калориметрична посудина заповнюється калориметричною рідиною (2), частіше всього дистильованою водою. Всередині калориметричної посудини розміщують електричний нагрівач (4), мішалку (5) і точний калориметричний термометр (7). Для зниження теплових втрат калориметр оточений теплоізоляційним шаром (6). У багатьох випадках при визначенні теплоємності підвід теплоти здійснюється за допомогою електричного нагрівача, який живиться від мережі постійного і змінного струму.
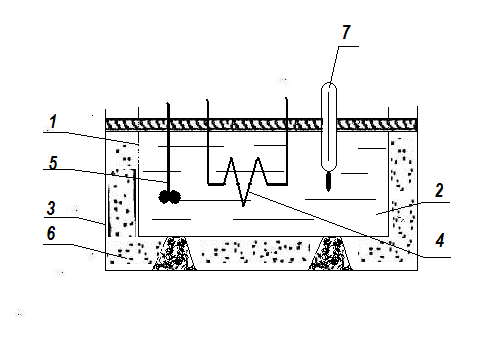
Рис. 10.1. Схема непроточного калориметра
