
- •Методичні вказівки
- •Загальні вказівки до проведення та оформлення студентами лабораторних робіт
- •Лабораторна робота № 1 Методи та засоби вимірювання термодинамічних параметрів. Похибки вимірювань та їх оцінка
- •Формули визначення похибки
- •Засоби вимірювання температури
- •Засоби вимірювання тиску
- •Засоби вимірювання швидкостей і витрат рідин
- •Похибки вимірювань і їх оцінка
- •Лабораторна робота № 2 дослідження процесу, що протікає при постійному об'ємі
- •Опис лабораторної установки
- •Підготовка лабораторної установки до роботи
- •Робота з установкою
- •Теоретичні відомості та обробка результатів досліджень
- •Лабораторна робота №3 Дослідження процесу, що протікає при постійній температурі
- •Робота з установкою
- •Етапи роботи
- •Теоретичні відомості і обробка результатів досліджень
- •Лабораторна робота №4 Дослідження процесу, який протікає при постійному тиску
- •Теоретичні відомості і обробка результатів досліджень
- •Лабораторна робота № 5 Експериментальна перевірка закону стану ідеального газу
- •Короткі теоретичні відомості
- •Порядок проведення експериментальних досліджень
- •Обробка результатів досліджень
- •Лабораторна робота № 6 Визначення теплоти пароутворення
- •Основні поняття і визначення
- •Опис лабораторної установки
- •Порядок проведення роботи
- •Лабораторна робота № 7 Визначення залежності температури насичення від тиску
- •Опис лабораторної установки
- •Порядок проведення роботи
- •Лабораторна робота № 8 Визначення показників адіабати
- •Методика експериментального визначення показника адіабати
- •Порядок проведення досліду
- •Лабораторна робота № 9 визначення ізобарної теплоємності повітря
- •Теоретичні основи
- •Опис дослідної установки
- •Методика проведення і обробка результатів вимірювань
- •Лабораторна робота №10 визначення питомої теплоємності речовини
- •Коротка теорія
- •Опис установки
- •Порядок виконання і етапу роботи
- •Облік теплоти, яка йде на нагрівання калориметра
- •Облік теплових витрат
- •Порядок виконання II етану роботи
- •Порядок роботи
- •Результати вимірювань і розрахунків шуканих величин
- •Коротка теорія
- •Опис установки
- •Порядок виконання роботи
- •(Титульний лист)
- •Лабораторна робота №...
- •II. Коротка теорія
- •III. Таблиця вимірів і розрахунку величин, що визначаються
- •Параметри стану
- •Співвідношення між різними одиницями вимірювання тиску
- •Співвідношення між одиницями роботи і тепла
- •Література:
Порядок виконання II етану роботи
У даній роботі теплоємність досліджуваної речовини вимірюється методом порівняння з відомою теплоємністю води. Установка (Рис. 10.3.) складається з двох однакових калориметрів, один з яких заповнений досліджуваною рідиною, наприклад, трансформаторним маслом, інший - водою. У кожний калориметр за-нурені однакові калориметричні нагрівачі, опір яких однаковий. Тому при послідовному з'єднанні спіралей і відповідно до закону Ленца-Джоуля, в них виділяється однакова кількість тепла. Для вирівнювання температури у всьому об'ємі рідини в кожному калориметрі є мішалка.
Нехай:
т
- маса
досліджуваної рідини у першому калориметрі
(трансформаторне масло), кг;
т1
- маса
води у другому калориметрі, кг;
ω
- водяний
еквівалент 1-го калориметра, кг;
ω1
- водяний еквівалент ІІ-го калориметра,
кг;
Сх
- питома
теплоємність трансформаторного масла,
![]()
4

Рис. 10.3. Установка для визначення теплоємності рідини.
1-термометр; 2-електронагрівач; 3- мішалка; 4-калориметр;5-термостат;
6- кожух; А - амперметр; У - вольтметр;U - джерело живлення.
С1
=
4187
![]() -
питома теплоємність води;
t
- початкова
температура І-го калориметра
(трансформаторного масла), °С;
t1
-
початкова температура ІІ-го калориметра
(води), °С.
-
питома теплоємність води;
t
- початкова
температура І-го калориметра
(трансформаторного масла), °С;
t1
-
початкова температура ІІ-го калориметра
(води), °С.
Кількість теплоти, отримана І-им калориметром від нагрівача:
![]() .
(10.14.)
.
(10.14.)
За цей час ІІ-й калориметр отримує тепло:
![]() .
(10.15.)
.
(10.15.)
Враховуючи, що Q1=Q2 отримаємо:
![]() .
(10.16.)
.
(10.16.)
Водяний еквівалент калориметра ω дорівнює масі води, яка поглинає при нагріванні на один градус таку ж кількість теплоти, яка необхідна для нагрівання на один градус „порожнього" калориметра з мішалкою. Тоді:
![]() (10.17.)
(10.17.)
де:
![]() -
маса калориметра з мішалкою, кг; С1
=389
-
питома теплоємність латуні, із якої
виготовлений калориметр і мішалка; V
– об’єм зануреної частини термометра
(м3),
визначається за допомогою мензурки;
-
маса калориметра з мішалкою, кг; С1
=389
-
питома теплоємність латуні, із якої
виготовлений калориметр і мішалка; V
– об’єм зануреної частини термометра
(м3),
визначається за допомогою мензурки;
![]() -
теплоємність одиниці об’єму термометра.
-
теплоємність одиниці об’єму термометра.
Порядок роботи
Вивчивши перший етап роботи і засвоївши навички вимірювання і обчислення шуканої величини, переходять до вивчення, а потім до виконання другого етапу роботи.
Згідно схеми установки (рис. 10.3.) виконують прямі вимірювання величин: т (маси досліджуваної рідини), т1 - (маси води); температур t, t1, Q, Q1, V (об’єм зануреної частини термометра), І, U.
Використовуючи формули (10.16.) і (10.17.) і підставивши в них виміряні величини, обчислюють значення питомої теплоємності.
Для зменшення теплообміну з навколишнім середовищем бажано, щоб початкова температура води t1, буда на 3-4 0С нижче, а кінцева Q1 на 3-4 0С вище кімнатної.
При нагріванні рідини її періодично помішують мішалкою.
Відлік температур рідини, що нагріваються, робити через 2 0С і нагрівати їх не вище, ніж на 10 оС навколишнього середовища, а потім вимкнути установку і зробити заміри температур рідини, які охолоджуються.
За результатами дослідів і проведення розрахунків визначають середнє значення
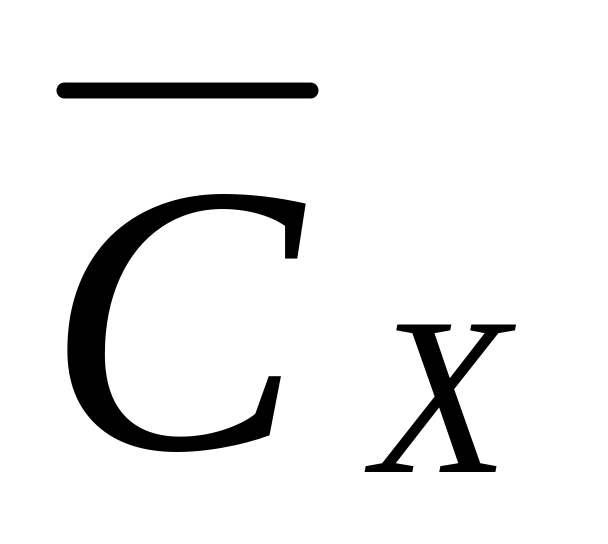 ,
а також обчислюють похибки вимірювань
цієї величини
,
а також обчислюють похибки вимірювань
цієї величини
 .
.За формулою визначають дійсне значення питомої теплоємності:
![]() .
.
9. Результати вимірів і розрахунків заносять до табл. 10.1.
10. Роблять висновки по І і ІІ частині роботи.
11. За формулою (10.2.) обчислюють загальну кількість теплоти, одержану у даному процесі досліджуваною рідиною і водою і пояснюють отриманий результат.
12. За
заміряними значеннями температури для
води і досліджуваної рі-дини будують
функціональну залежність
![]() (рис. 10.2.).
(рис. 10.2.).
13. За формулою (10.13.) обчислюють температуру і знаходять значення (t2 - t1)0 для кожної рідини.
14. За формулою (10.11.) обчислюють значення СРх, порівнюють його з результатом (Сх) обчисленим за формулою (10.16.) і роблять висновки.
15. Отримане значення (Сх) порівнюють з табличним і роблять висновки.
Увага: при виникненні ускладнень при знятті показань з приладів установки і її неполадках звертатися до лаборанта або викладача.
