
- •Введение
- •Электронное строение элементов-органогенов. Химическая связь в органических молекулах
- •Химическая связь в органических молекулах
- •Классификация химических реакций. Химические свойства алканов, алкенов и алкадиенов
- •Реакционная способность алканов
- •Реакционная способность алкенов
- •Химические свойства алкенов
- •Общий механизм реакций электрофильного присоединения
- •Реакции электрофильного присоединения к несимметричным алкенам
- •Реакции присоединения к алкадиенам
- •Сопряжённые системы. Ароматичность. Электронные эффекты. Реакции электрофильного замещения в бензоле и его производных
- •Химические свойства бензола
- •Взаимное влияние атомов в молекулах органических соединений. Электронные эффекты
- •Реакции электрофильного замещения в нафталине
- •Реакции окисления гомологов бензола
- •Химические свойства галогеналканов, спиртов и фенолов
- •Медико-биологическое значение галогеналканов
- •Спирты и фенолы
- •Медико-биологическое значение спиртов и фенолов
- •Кислотные и основные свойства органических соединений. Реакционная способность аминов
- •Кислоты Бренстеда
- •Основания Бренстеда
- •Реакционная способность оксосоединений
- •Классификация и номенклатура оксосоединений
- •Названия алифатических альдегидов
- •Реакционные центры в молекулах оксосоединений
- •Примеры реакций нуклеофильного присоединения
- •Медико-биологическое значение альдегидов и кетонов
- •Химические свойства карбоновых кислот и их функциональных производных
- •Названия предельных алифатических монокарбоновых кислот
- •Реакционные центры в молекулах карбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Реакции нуклеофильного замещения
- •Реакции карбоновых кислот по радикалу
- •Названия насыщенных алифатических дикарбоновых кислот
- •Медико-биологическое значение карбоновых кислот и их производных
- •Гетерофункциональные соединения алифатического ряда – метаболиты и биорегуляторы
- •Аминоспирты
- •Аминокислоты
- •Гидроксикислоты (оксикислоты)
- •Оксокислоты
- •Медико-биологическое значение гетерофункциональных производных карбоновых кислот
- •Оптическая изомерия
- •Стереоизомерия молекул с несколькими центрами хиральности
- •Стереоизомерия и биологическая активность
- •Гетерофункциональные производные бензольного ряда
- •Производные сульфаниловой кислоты
- •Сульфаниламидные препараты
- •Салициловая кислота и ее производные
- •Гетероциклические соединения. Производные пятичленных гетероциклов
- •Пятичленные гетероциклы с одним гетероатомом
- •Свойства пиррола и его производных
- •Свойства фурана и его производных
- •Пятичленные гетероциклы с двумя гетероатомами
- •Шестичленные гетероциклические соединения
- •Шестичленные гетероциклы с двумя гетероатомами
- •Углеводы. Моносахариды
- •Цикло-оксо-таутомерия моносахаридов
- •Углеводы. Ди- и полисахариды
- •Природные α-аминокислоты. Пептиды, белки
- •Строение и классификация природных α-аминокислот
- •Стереоизомерия α-аминокислот
- •Химические свойства
- •Реакции α-аминокислот in vivo
- •Нуклеиновые кислоты
- •Нуклеиновые основания
- •Нуклеозиды
- •Названия нуклеозидов
- •Нуклеотиды
- •Нуклеиновые кислоты
- •Омыляемые липиды
- •Фосфолипиды
- •Неомыляемые липиды
- •Алкалоиды
- •Литература
- •Оглавление
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3. Заказ № 313.
Оксокислоты
К оксокислотам относятся альдегидо- и кетонокислоты.
П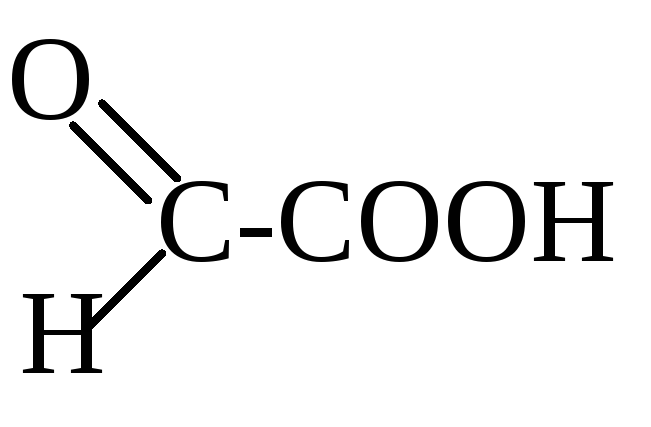 римером
альдегидокислоты является глиоксиловая
или глиоксалевая кислота (2-оксоэтановая
кислота):
римером
альдегидокислоты является глиоксиловая
или глиоксалевая кислота (2-оксоэтановая
кислота):
В ажную
роль в биохимических процессах играют
кетонокислоты, например:
ажную
роль в биохимических процессах играют
кетонокислоты, например:
О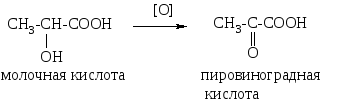 ни
участвуют в организме в цикле трикарбоновых
кислот (цикле Кребса) и образуются при
окислении соответствующих оксикислот:
ни
участвуют в организме в цикле трикарбоновых
кислот (цикле Кребса) и образуются при
окислении соответствующих оксикислот:

Подробнее остановимся на свойствах кетонокислот.
Для оксокислот характерны свойства карбоновых кислот, кетонов, а также специфические свойства.

Как карбоновые кислоты оксокислоты образуют соли, проявляя кислотные свойства, и функциональные производные, например, сложные эфиры (реакция SN). Как кетоны они вступают в реакции нуклеофильного присоединения и присоединения-отщепления (например, образуя оксимы, гидразоны и т.п.).
С пецифическим
свойством
β-кетокислот является их способность
к декарбоксилированию, например, при
ферментативном декарбоксилировании
ацетоуксусной кислоты образуется
ацетон:
пецифическим
свойством
β-кетокислот является их способность
к декарбоксилированию, например, при
ферментативном декарбоксилировании
ацетоуксусной кислоты образуется
ацетон:
Ацетоуксусная кислота и ацетон накапливаются в крови больных сахарным диабетом (т.н. «кетоновые тела»). К кетоновым телам относят также и предшественницу ацетоуксусной кислоты – β-оксимасляную кислоту.
Другим специфическим свойством β-кетонокислот (а точнее, их сложных эфиров) является их способность к существованию в двух таутомерных формах.
Таутомерия – равновесная динамическая изомерия. Это значит, таутомеры самопроизвольно превращаются друг в друга и существуют в подвижном равновесии. Таутомеры превращаются друг в друга за счет переноса какой-либо подвижной группы. Если такой группой является протон водорода, то таутомерию называют прототропной.
Рассмотрим это на примере этилового эфира ацетоуксусной кислоты (часто его называют просто ацетоуксусным эфиром).

За счет электронодонорного влияния сложноэфирной и кето-групп α-атом углерода становится CH-кислотным центром. Он отщепляет протон водорода, который присоединяется к неподеленной электронной паре кислорода оксо-групы (оксониевому основному центру). Кето-таутомер превращается в енольный (ен – двойная связь, -ол – гидроксильная группа). Енольная гидроксильная группа проявляет кислотные свойства, она отщепляет протон, который присоединяется к электронному облаку π-связи – енольный таутомер превращается в кето-таутомер. Эти превращения протекают самопроизвольно, и таутомеры существуют в динамическом равновесии.
При действии на ацетоуксусный эфир определенного реагента в реакцию вступает один из таутомеров. Так, кето-форма вступает в реакции, характерные для кетонов (нуклеофильного присоединения с синильной кислотой, присоединения-отщепления с гидразином или гидроксиламином):
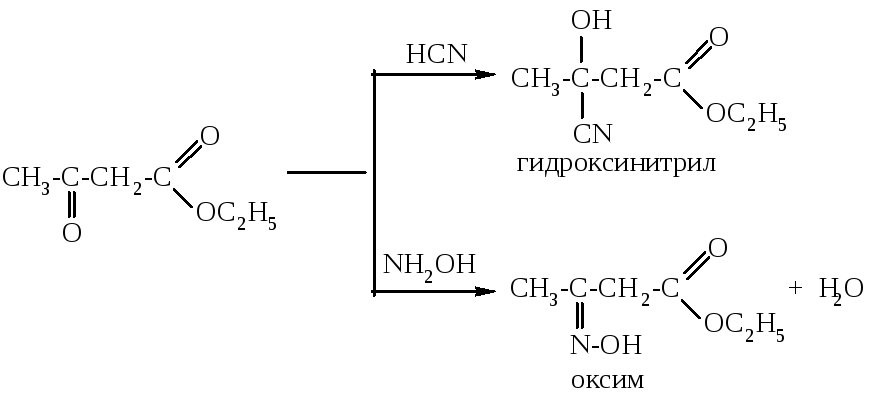
За счет енольной таутомерной формы ацетоуксусный эфир взаимодействует с хлоридом железа (III) (реакция, характерная для всех енолов), с бромной водой (реакция на двойную связь):
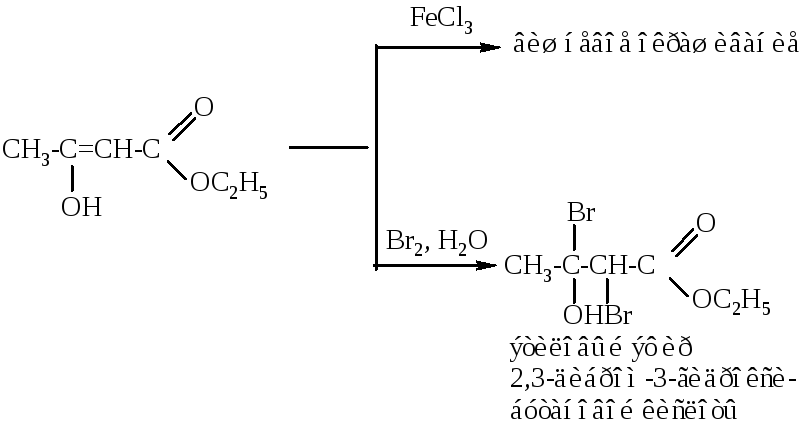
Обратите внимание, поскольку второй таутомер за счет равновесия восполняет убыль реагирующего таутомера, таутомерная смесь реагирует в данном направлении как единое целое.
О бычно
енольная форма менее устойчива, поэтому
доля её в таутомерном равновесии низкая.
Иногда более энергетически выгодным
является существование молекулы именно
в енольной форме, как, например, для
диэтилового эфира щавелевоуксусной
кислоты:
бычно
енольная форма менее устойчива, поэтому
доля её в таутомерном равновесии низкая.
Иногда более энергетически выгодным
является существование молекулы именно
в енольной форме, как, например, для
диэтилового эфира щавелевоуксусной
кислоты:
Это связано с тем, что енольная таутомерная форма представляет собой единую сопряженную систему.
