
- •Введение
- •Электронное строение элементов-органогенов. Химическая связь в органических молекулах
- •Химическая связь в органических молекулах
- •Классификация химических реакций. Химические свойства алканов, алкенов и алкадиенов
- •Реакционная способность алканов
- •Реакционная способность алкенов
- •Химические свойства алкенов
- •Общий механизм реакций электрофильного присоединения
- •Реакции электрофильного присоединения к несимметричным алкенам
- •Реакции присоединения к алкадиенам
- •Сопряжённые системы. Ароматичность. Электронные эффекты. Реакции электрофильного замещения в бензоле и его производных
- •Химические свойства бензола
- •Взаимное влияние атомов в молекулах органических соединений. Электронные эффекты
- •Реакции электрофильного замещения в нафталине
- •Реакции окисления гомологов бензола
- •Химические свойства галогеналканов, спиртов и фенолов
- •Медико-биологическое значение галогеналканов
- •Спирты и фенолы
- •Медико-биологическое значение спиртов и фенолов
- •Кислотные и основные свойства органических соединений. Реакционная способность аминов
- •Кислоты Бренстеда
- •Основания Бренстеда
- •Реакционная способность оксосоединений
- •Классификация и номенклатура оксосоединений
- •Названия алифатических альдегидов
- •Реакционные центры в молекулах оксосоединений
- •Примеры реакций нуклеофильного присоединения
- •Медико-биологическое значение альдегидов и кетонов
- •Химические свойства карбоновых кислот и их функциональных производных
- •Названия предельных алифатических монокарбоновых кислот
- •Реакционные центры в молекулах карбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Реакции нуклеофильного замещения
- •Реакции карбоновых кислот по радикалу
- •Названия насыщенных алифатических дикарбоновых кислот
- •Медико-биологическое значение карбоновых кислот и их производных
- •Гетерофункциональные соединения алифатического ряда – метаболиты и биорегуляторы
- •Аминоспирты
- •Аминокислоты
- •Гидроксикислоты (оксикислоты)
- •Оксокислоты
- •Медико-биологическое значение гетерофункциональных производных карбоновых кислот
- •Оптическая изомерия
- •Стереоизомерия молекул с несколькими центрами хиральности
- •Стереоизомерия и биологическая активность
- •Гетерофункциональные производные бензольного ряда
- •Производные сульфаниловой кислоты
- •Сульфаниламидные препараты
- •Салициловая кислота и ее производные
- •Гетероциклические соединения. Производные пятичленных гетероциклов
- •Пятичленные гетероциклы с одним гетероатомом
- •Свойства пиррола и его производных
- •Свойства фурана и его производных
- •Пятичленные гетероциклы с двумя гетероатомами
- •Шестичленные гетероциклические соединения
- •Шестичленные гетероциклы с двумя гетероатомами
- •Углеводы. Моносахариды
- •Цикло-оксо-таутомерия моносахаридов
- •Углеводы. Ди- и полисахариды
- •Природные α-аминокислоты. Пептиды, белки
- •Строение и классификация природных α-аминокислот
- •Стереоизомерия α-аминокислот
- •Химические свойства
- •Реакции α-аминокислот in vivo
- •Нуклеиновые кислоты
- •Нуклеиновые основания
- •Нуклеозиды
- •Названия нуклеозидов
- •Нуклеотиды
- •Нуклеиновые кислоты
- •Омыляемые липиды
- •Фосфолипиды
- •Неомыляемые липиды
- •Алкалоиды
- •Литература
- •Оглавление
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3. Заказ № 313.
Аминокислоты
Аминокислоты – гетерофункциональные соединения, содержащие амино- и карбоксильную группу. По их взаимному расположению аминокислоты классифицируют на α-, β-, γ-, δ-, ε- аминокислоты. Например:

А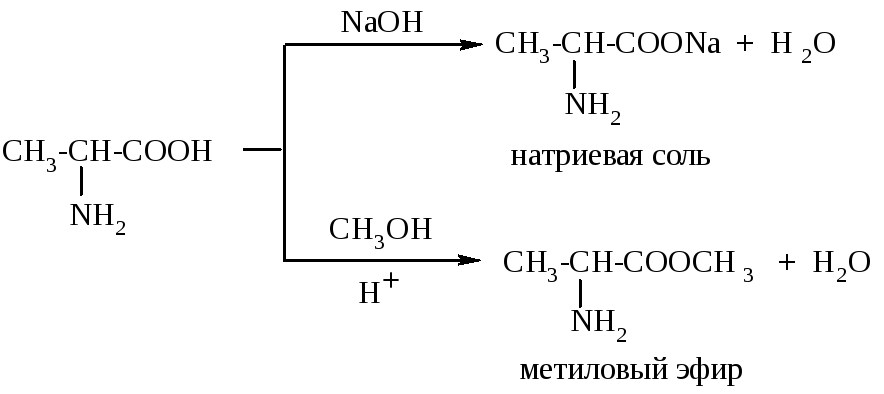 минокислоты
обладают всеми свойствами карбоновых
кислот - они способны образовывать соли,
сложные эфиры и другие функциональные
производные:
минокислоты
обладают всеми свойствами карбоновых
кислот - они способны образовывать соли,
сложные эфиры и другие функциональные
производные:
А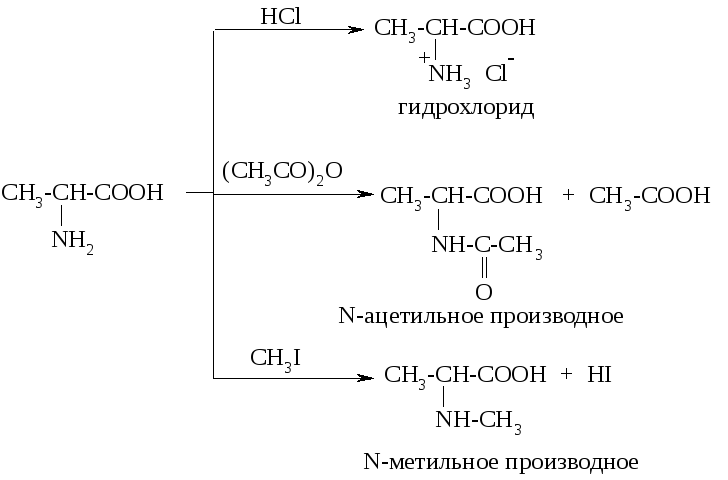 минокислоты
проявляют также свойства аминов (основные
свойства, способность к реакциям
ацилирования и алкилирования):
минокислоты
проявляют также свойства аминов (основные
свойства, способность к реакциям
ацилирования и алкилирования):
А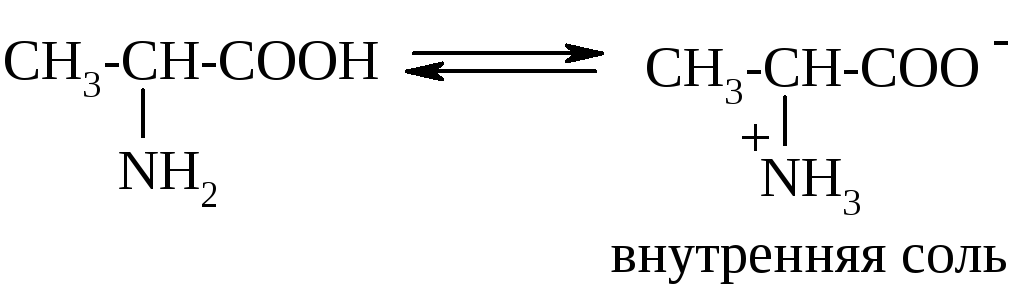 мфотерность
аминокислот приводит к тому, что они
могут существовать в виде внутренних
солей:
мфотерность
аминокислот приводит к тому, что они
могут существовать в виде внутренних
солей:
Специфические свойства аминокислот зависят от взаимного расположения амино- и карбоксильной групп.
α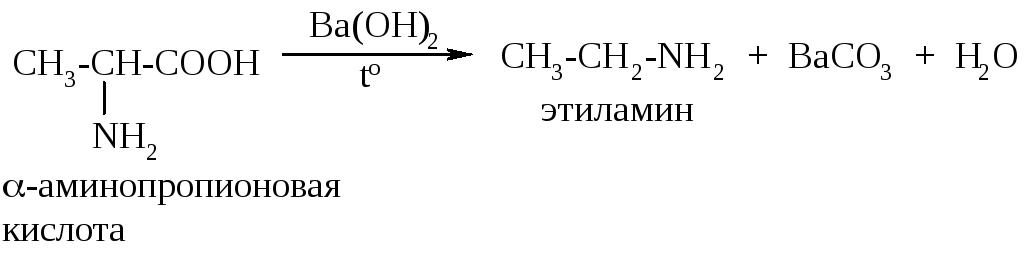 -Аминокислоты
вступают в реакции декарбоксилирования
при нагревании с гидроксидом бария с
образованием соответствующих аминов,
например:
-Аминокислоты
вступают в реакции декарбоксилирования
при нагревании с гидроксидом бария с
образованием соответствующих аминов,
например:
Сходным образом декарбоксилирование природных α-аминокислот протекает и in vivo с участием ферментов, например, при декарбоксилировании серина образуется коламин:
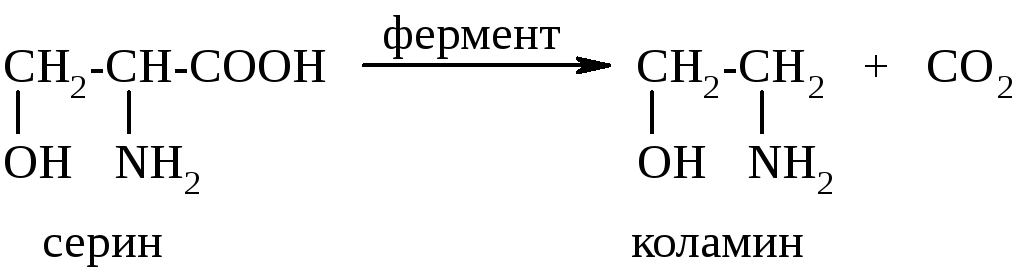
Другим специфическим свойством α-аминокислот является их способность к образованию межмолекулярных циклических амидов (дикетопиперазинов):
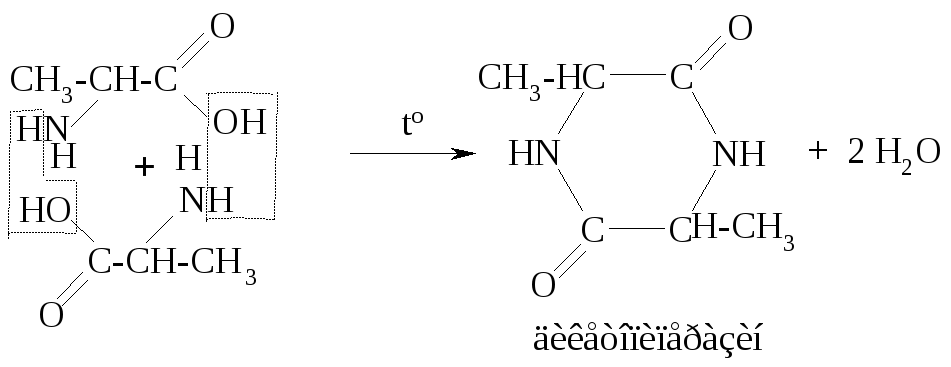
Так как дикетопиперазины фактически являются амидами, они способны к гидролизу и в кислой, и в щелочной среде.
Характерной особенностью β-аминокислот являются реакции внутримолекулярного элиминирования: при нагревании они отщепляют молекулу аммиака. Например, при нагревании β-аминомасляной кислоты образуется кротоновая (бутен-2-овая) кислота:
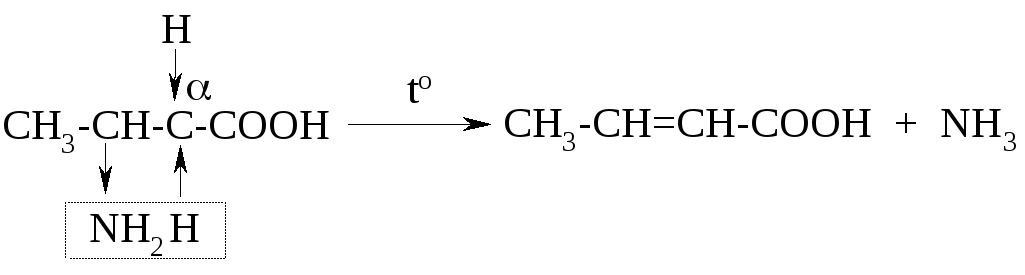
Способность к этой реакции связана с подвижностью протона водорода при α-углеродном атоме из-за электроноакцепторного влияния двух функциональных групп.
З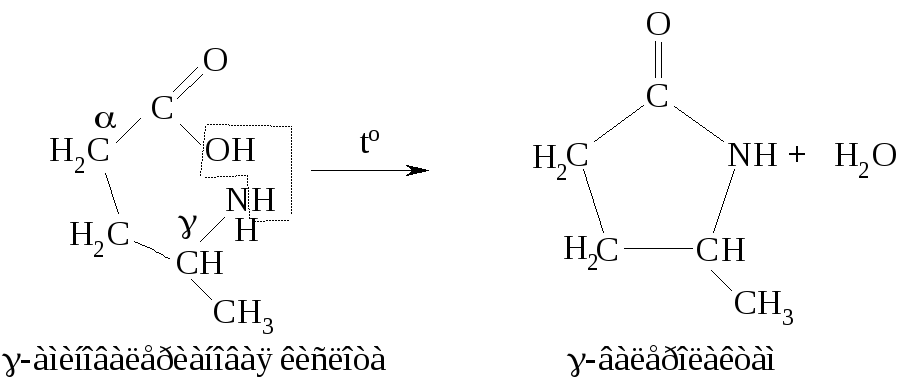 а
счет существования молекул γ-аминокислот
в клешневидной конформации функциональные
группы оказываются пространственно
сближенными, и между ними может происходить
взаимодействие с образованием циклического
внутримолекулярного амида (лактама):
а
счет существования молекул γ-аминокислот
в клешневидной конформации функциональные
группы оказываются пространственно
сближенными, и между ними может происходить
взаимодействие с образованием циклического
внутримолекулярного амида (лактама):
Пятичленные циклы устойчивы, поэтому реакция протекает достаточно легко.
К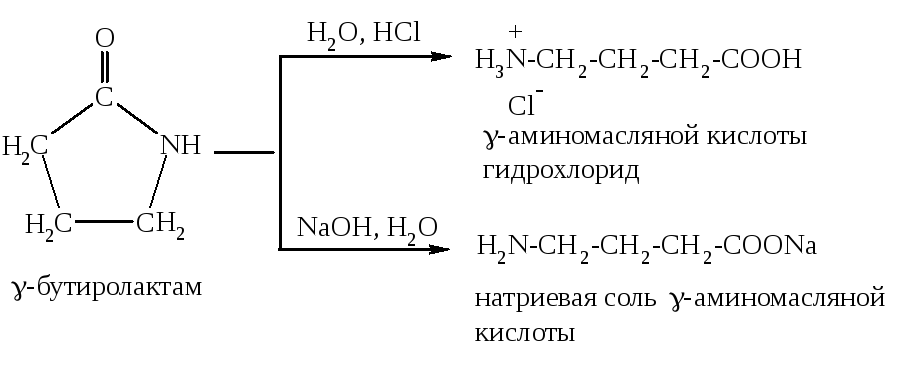 ак
амиды лактамы подвергаются гидролизу
и в кислой, и в щелочной среде:
ак
амиды лактамы подвергаются гидролизу
и в кислой, и в щелочной среде:
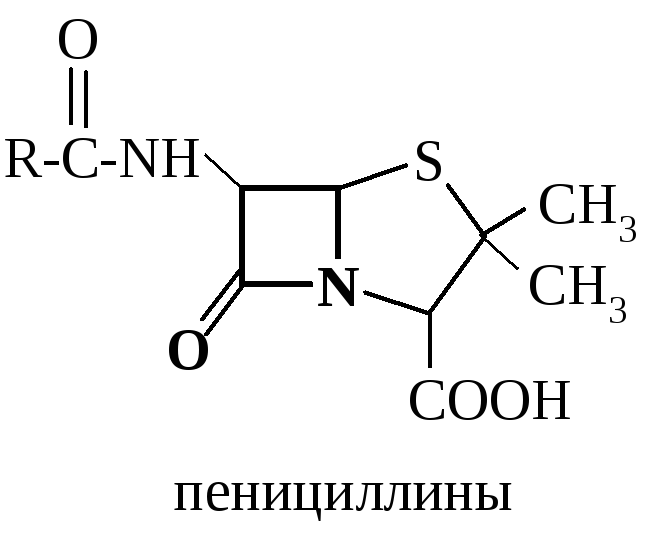
Некоторые природные соединения и синтетические лекарственные средства содержат в своей структуре лактамный цикл. Например, четырехчленный β-лактамный цикл присутствует в молекулах пенициллинов. Из-за его способности к гидролизу, что приводит к потере биологической активности, пенициллины не стерилизуют в водных растворах.
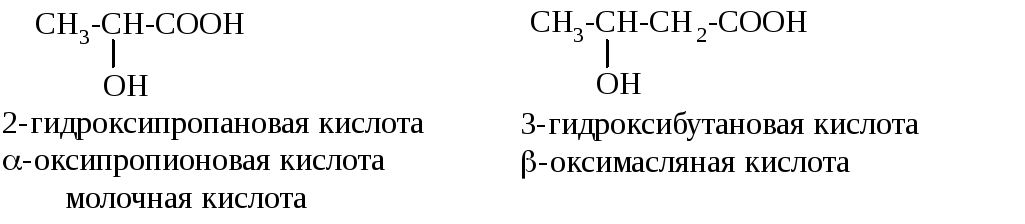
Гидроксикислоты (оксикислоты)
Примерами гидроксикислот являются:
Д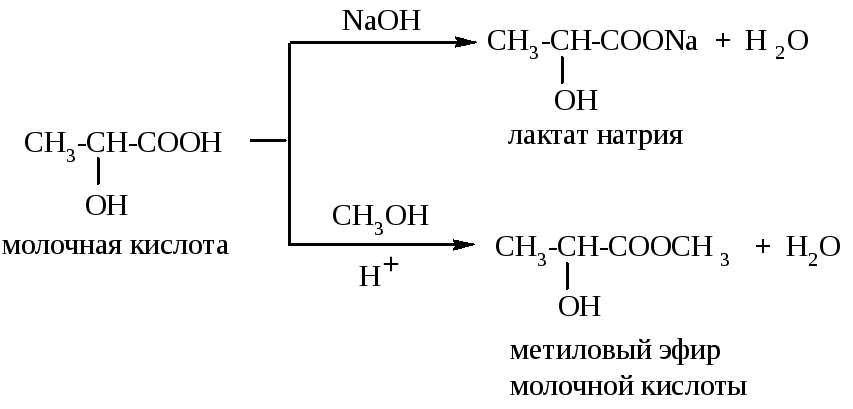 ля
гидроксикислот характерны свойства
карбоновых кислот и спиртов. Как
карбоновые кислоты они образуют соли
и сложные эфиры:
ля
гидроксикислот характерны свойства
карбоновых кислот и спиртов. Как
карбоновые кислоты они образуют соли
и сложные эфиры:
К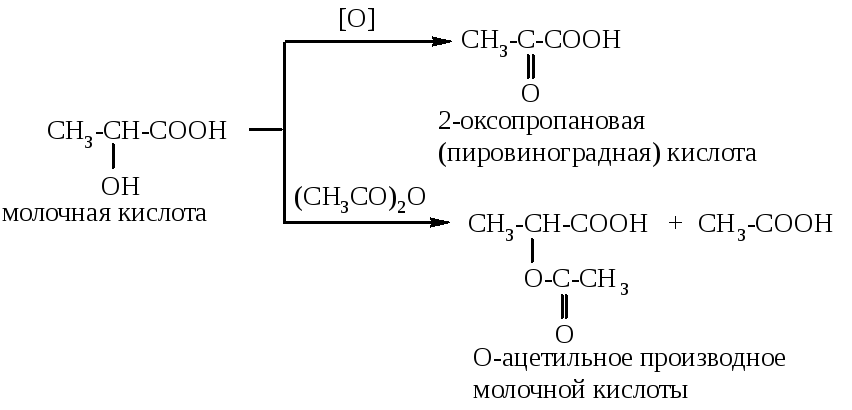 ак
спирты оксикислоты способны к реакциям
окисления и ацилирования:
ак
спирты оксикислоты способны к реакциям
окисления и ацилирования:
Специфические свойства α-оксикислот. α-Оксикислоты при нагревании в присутствии концентрированной серной кислоты разлагаются с образованием карбонильных соединений и муравьиной кислоты. Например:
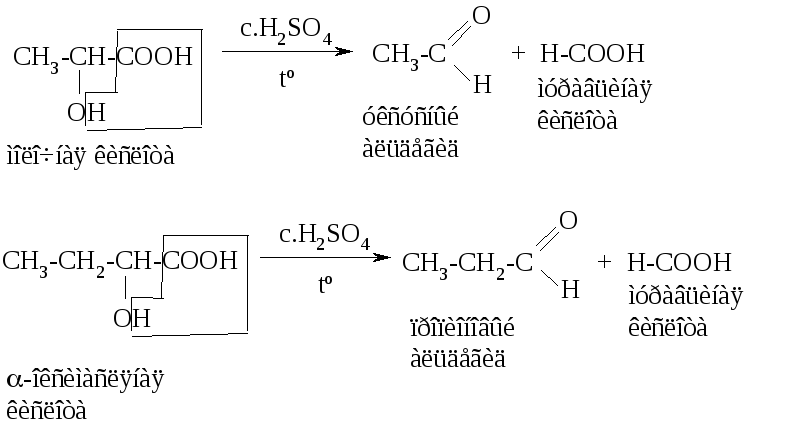
Другим специфическим свойством α-оксикислот является их способность к реакциям образования межмолекулярных циклических сложных эфиров – лактидов:
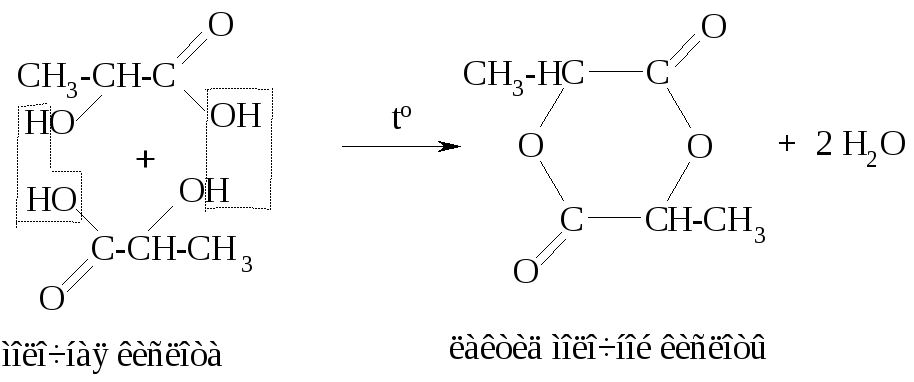
Лактиды способны к гидролизу и в кислой, и в щелочной среде.
Для β-оксикислот характерны реакции внутримолекулярного элиминирования, при нагревании они отщепляют воду:
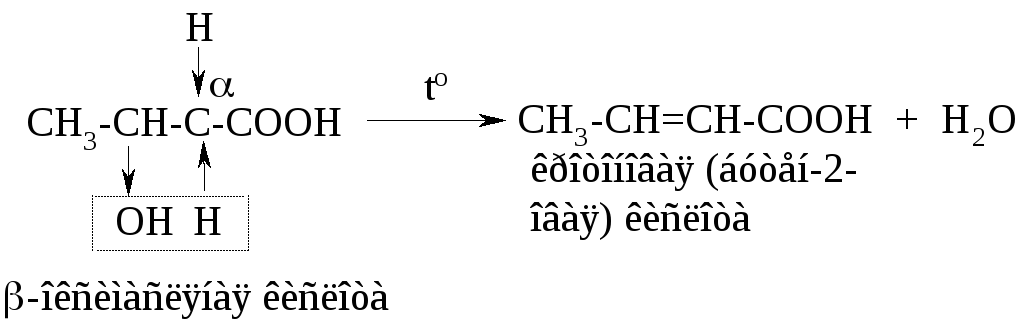
γ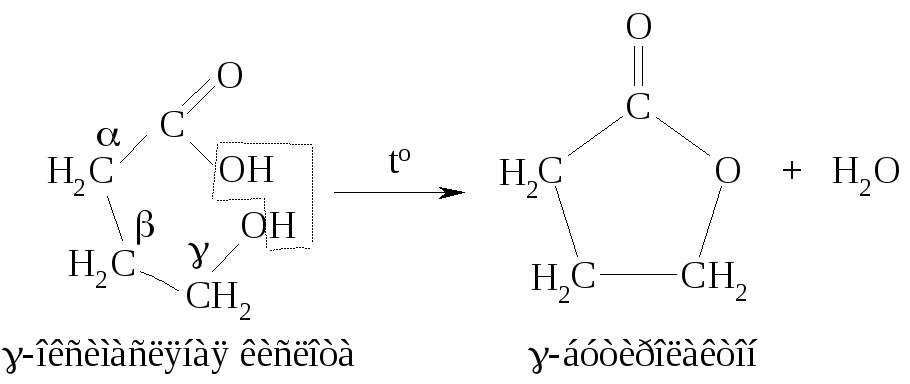 -Оксикислоты
способны к
реакциям внутримолекулярной этерификации,
приводящим к образованию циклических
сложных эфиров, например,
-Оксикислоты
способны к
реакциям внутримолекулярной этерификации,
приводящим к образованию циклических
сложных эфиров, например,
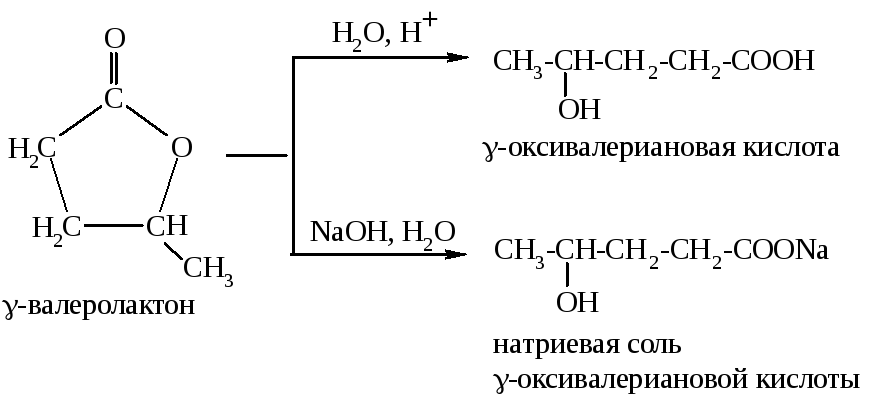
Как сложные эфиры лактоны гидролизуются и в кислой, и в щелочной среде:
П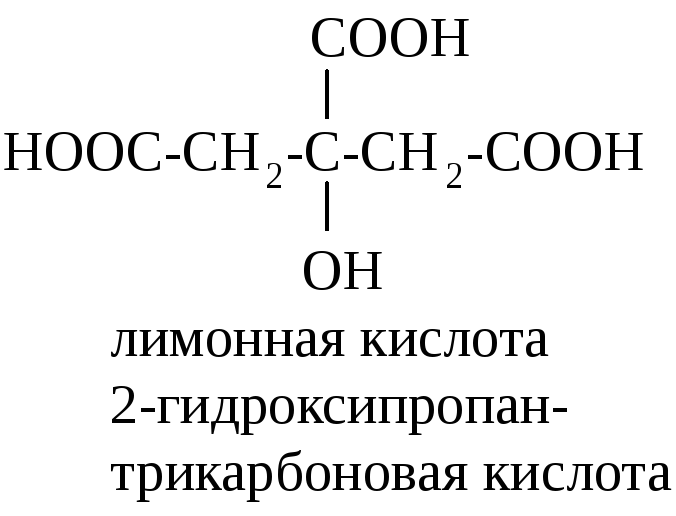 римерами
многоосновных оксикислот являются
яблочная (соли – малаты), винная (соли
– тартраты) и лимонная (соли – цитраты)
кислоты:
римерами
многоосновных оксикислот являются
яблочная (соли – малаты), винная (соли
– тартраты) и лимонная (соли – цитраты)
кислоты:

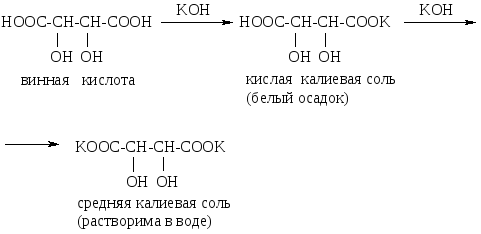
Как дикарбоновая кислота, винная кислота дает два ряда солей – кислые и средние, причем кислая калиевая соль нерастворима в воде, а средняя – растворима.
На этом основано качественное определение винной кислоты.
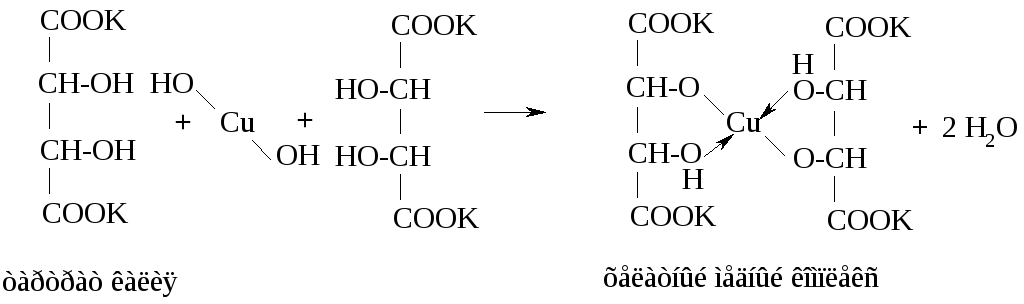
Второй качественной реакцией винной кислоты является ее взаимодействие с гидроксидом меди (II). Это реакция на диольный фрагмент молекулы (происходит растворение голубого осадка Cu(OH)2 с образованием ярко-синего раствора:
К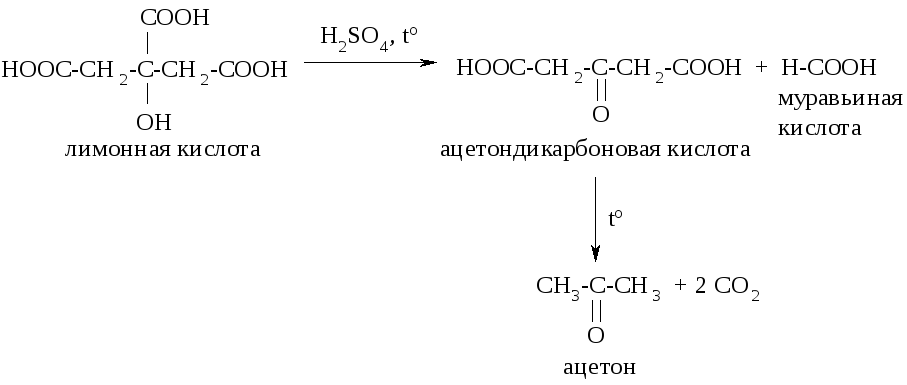 ак
α-оксикислота лимонная кислота разлагается
при нагревании в присутствии
концентрированной серной кислоты, давая
ацетондикарбоновую (3-оксопентандиовую)
кислоту и муравьиную кислоту. Для
β-кетонокислот характерны реакции
декарбоксилирования, поэтому
ацетондикарбоновая кислота превращается
в ацетон:
ак
α-оксикислота лимонная кислота разлагается
при нагревании в присутствии
концентрированной серной кислоты, давая
ацетондикарбоновую (3-оксопентандиовую)
кислоту и муравьиную кислоту. Для
β-кетонокислот характерны реакции
декарбоксилирования, поэтому
ацетондикарбоновая кислота превращается
в ацетон:
Ацетон можно обнаружить с помощью иодоформной пробы (см. стр. 85).
